Clear Sky Science · pl
Inżynierowane oksydazy alkoholi katalizują transestryfikację w środowisku wodnym bez konkurencyjnej hydrolizy
Dlaczego ta historia o enzymie ma znaczenie
Wiele codziennych produktów, od leków i aromatów spożywczych po biodiesel, zależy od prostego rodzaju wiązania chemicznego — estru. Wydajne, tanie i przyjazne dla środowiska wytwarzanie i modyfikacja tych estrów to ważny cel zielonej chemii. Problem w tym, że woda, będąca z punktu widzenia bezpieczeństwa i zrównoważenia idealnym rozpuszczalnikiem, zwykle sabotuje te reakcje, rozrywając estry równie szybko, jak powstają. W tej pracy odkryto zmodyfikowany enzym, który potrafi tworzyć estry w wodzie, niemal całkowicie ignorując otaczającą go wodę, otwierając tym samym drogę do czystszej chemii przemysłowej.
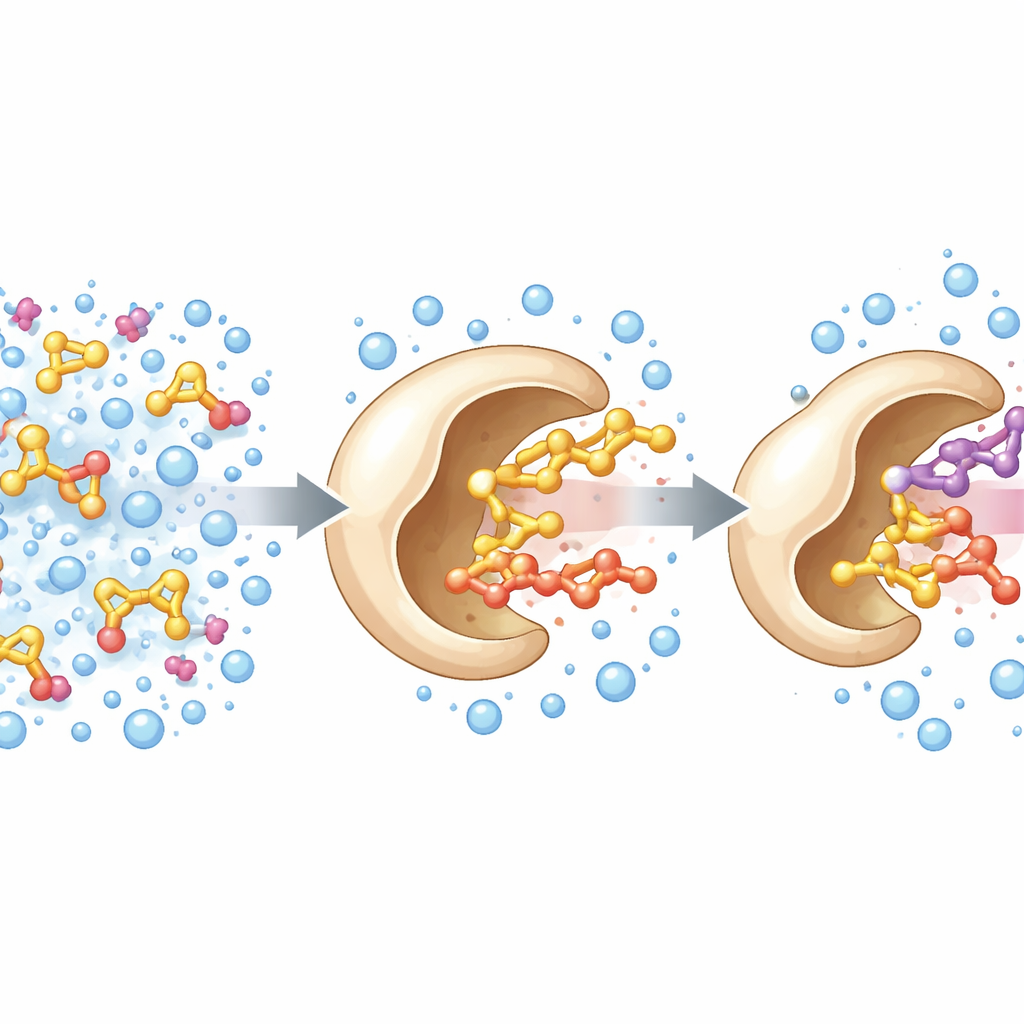
Przekierowanie znanego enzymu na nowe zadanie
Naukowcy zaczęli od znanego enzymu — oksydazy alkoholi z grzyba rozkładającego drewno. W naturze enzym ten wykorzystuje koenzym flawinowy do odbierania elektronów z małych alkoholi, takich jak metanol. Zespół postanowił poszerzyć jego zakres substratowy, aby mógł przerabiać większe alkohole, istotniejsze dla chemii precyzyjnej i aromatów. Korzystając z trójwymiarowej struktury enzymu jako mapy, skupili się na trzech aminokwasach tworzących swoisty „przejściowy” właz do miejsca aktywnego. Poprzez randomizację tych pozycji i przesiew wariantów odkryli potrójny mutant — nazwany PcAOx‑VPN — który efektywnie przetwarzał większe alkohole, takie jak alkohol benzylowy, tracąc przy tym znaczną część pierwotnej aktywności wobec drobnych alkoholi, np. metanolu.
Niespodziewany talent: tworzenie estrów w wodzie
Podczas testów PcAOx‑VPN w mieszaninach zaprojektowanych do rozpuszczania tłustych substratów zespół zauważył dodatkowe piki w analizie. Okazały się nimi produkty acetylacji: enzym przenosił grupę acylową z aktywnego donora estrowego na alkohole, reakcję znaną jako transestryfikacja. Co zaskakujące, zachodziło to w buforze na bazie wody — warunku, który zwykle sprzyja silnej konkurencyjnej hydrolizie, gdy woda atakuje i niszczy ester. Tutaj PcAOx‑VPN skutecznie łączył alkohole z donorami acylowymi, takimi jak octan winylu, tworząc nowe estry często z wydajnościami powyżej 80% i przy tylko umiarkowanych reakcjach ubocznych. Ten sam enzym działał na szeroką gamę alkoholi — łańcuchowe, aromatyczne, chiralne i zawierające siarkę — i w kilku przypadkach wykazywał wyraźne preferencje dla jednej z form enancjomerycznych.
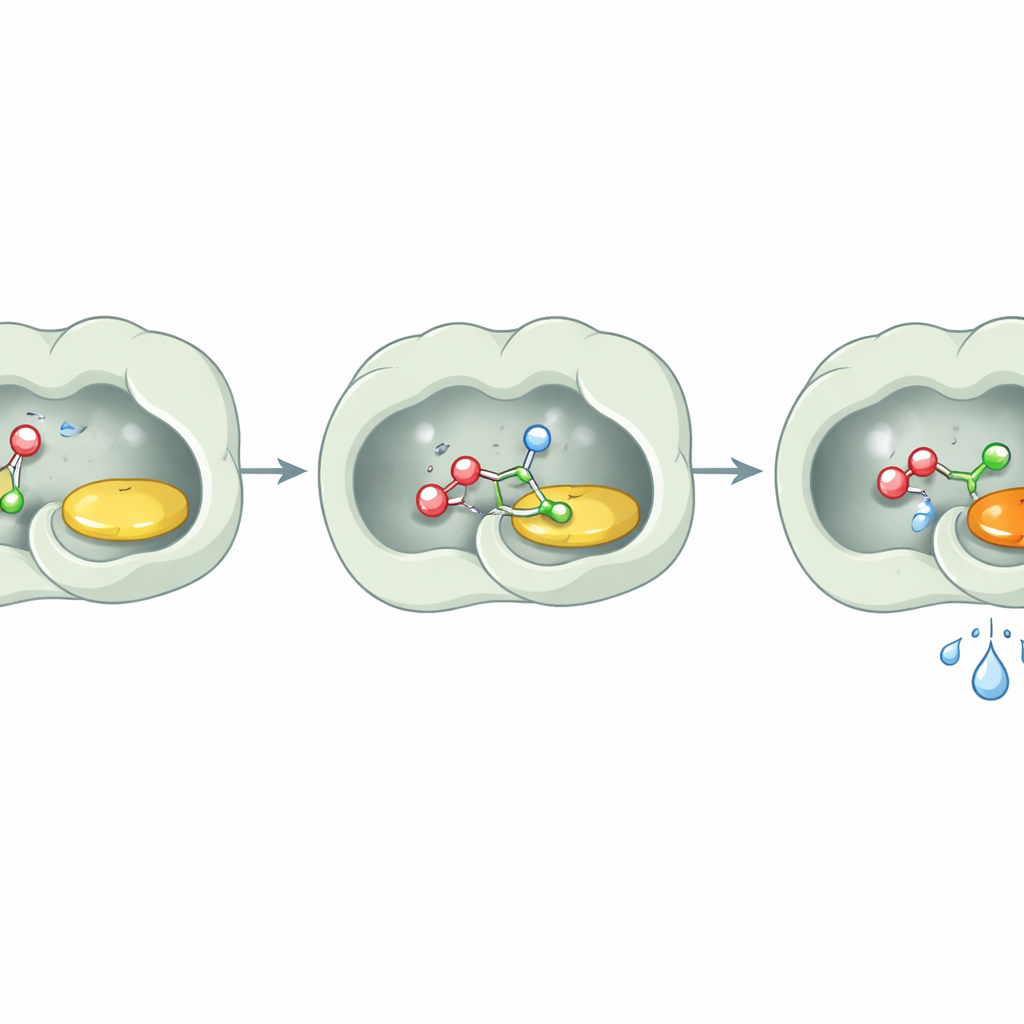
Jak trzymać wodę z dala
Kluczową niespodzianką było to, czego enzym nie robił: nie obserwowano istotnej hydrolizy estrów. Nawet po długich inkubacjach z substratami estrowymi i wodą, PcAOx‑VPN pozostawiał je w zasadzie nienaruszone, o ile nie dostarczono dodatkowego donora acylowego. Badania strukturalne dają proste wyjaśnienie. Miejsce aktywne jest wyścielone w większości oleistymi, aromatycznymi aminokwasami, które tworzą silnie hydrofobową kieszeń. Szczegółowa analiza nie wykazała cząsteczek wody blisko koenzymu flawinowego, a narzędzia obliczeniowe potwierdziły, że kanał prowadzący do miejsca aktywnego również nie sprzyja obecności wody. W istocie enzym tworzy malutki suchy pokój wewnątrz wodnego świata. Alkohole i aktywowane estry mogą wejść i zareagować, ale cząsteczki wody są odpychane, więc nie mają szansy rozbić powstałego produktu.
Jak prawdopodobnie przebiega reakcja wewnątrz
Eksperymenty mechanistyczne i analiza mutacji ujawniły, że dwa aminokwasy — histydyna i asparagina — są kluczowe zarówno dla naturalnej roli oksydacyjnej enzymu, jak i jego nowej umiejętności transestryfikacji. Histydyna działa jako zasada, pomagając odciągnąć proton z nadchodzącego alkoholu i uczynić go bardziej reaktywnym, podczas gdy asparagina stabilizuje powstały stan naładowany. Wspólnie sprzyjają atakowi alkoholu na donor acylowy, tworząc krótkotrwały intermediat, który zapada się do pożądanego estru. Wymagany jest także utleniony stan koenzymu flawinowego: w warunkach beztlenowych, gdy flawina ulega redukcji, transestryfikacja ustaje i wznawia się dopiero po ponownym wprowadzeniu powietrza. Co ważne, gdy ten sam zestaw trzech mutacji wprowadzono do pokrewnych oksydaz z innych grzybów, również zyskały one silną aktywność transestryfikacyjną, co sugeruje, że to zachowanie można uogólnić.
Co to oznacza dla bardziej zielonej chemii
Dla osób niebędących specjalistami kluczowy przekaz jest taki: autorzy nauczyli znany enzym nowej sztuczki — tworzenia użytecznych estrów bezpośrednio w wodzie, jednocześnie skutecznie ignorując skłonność wody do rozkładania produktu. Wycięli suchą, olejowoprzystępną kieszeń wewnątrz białka i dostroili kilka kluczowych aminokwasów, tworząc katalizator, który faworyzuje alkohole zamiast wody jako partnerów reakcji. Ponieważ ta zasada projektowa działa w pokrewnych enzymach, podejście to może zostać rozszerzone na rodzinę katalizatorów do produkcji aromatów, zapachów, substancji precyzyjnych, a być może także biopaliw w bezpieczniejszych, bardziej zrównoważonych procesach, które w mniejszym stopniu polegają na ostrych rozpuszczalnikach organicznych, a w większym — na wodzie.
Cytowanie: Wu, B., Ma, Y., Feng, C. et al. Engineered alcohol oxidases catalyse transesterification in aqueous media without competing hydrolysis. Nat Commun 17, 2183 (2026). https://doi.org/10.1038/s41467-026-68899-y
Słowa kluczowe: inżynieria enzymów, biokataliza, zielona chemia, synteza estrów, flawoproteiny