Clear Sky Science · pl
Hamowanie sygnalizacji TGF-β w mikrogleju stymuluje dorosłą neurogenezę w hipokampie i zmniejsza zachowania lękowe u dorosłych myszy
Dlaczego komórki układu odpornościowego mózgu mają znaczenie dla nastroju i pamięci
Większość z nas myśli o komórkach odpornościowych jako o patrolujących ciało, a nie kształtujących nasze myśli i uczucia. To badanie kwestionuje to podejście, pokazując, że mikroglej — komórki odpornościowe żyjące w mózgu — może znacząco wpływać na powstawanie nowych neuronów w hipokampie, regionie istotnym dla pamięci i emocji. Wyłączając określony szlak sygnalizacyjny w mikrogleju u dorosłych myszy, badacze zwiększyli produkcję i przeżywalność nowych neuronów i zaobserwowali mierzalne zmiany w zachowaniach przypominających lęk.
Ciche żłobki mózgu dla nowych neuronów
U dorosłych ssaków nowe neurony wciąż rodzą się w kilku wyspecjalizowanych „żłobkach”. Jednym z najważniejszych jest strefa podziarnista hipokampa, która pomaga rozdzielać podobne wspomnienia, wspiera uczenie się i przyczynia się do regulacji nastroju. W normalnych warunkach wiele z tych nowo narodzonych komórek obumiera zanim w pełni dojrzeje. Ich liczba może wzrastać lub maleć w odpowiedzi na ćwiczenia, wzbogacone środowisko, stres, udar czy epilepsję. Mikroglej nieustannie monitoruje to środowisko, ale pozostawało niejasne, czy jego reaktywny, „zapalny” stan pomaga, czy szkodzi dorosłej neurogenezie.
Wyłączenie kluczowego hamulca w mikrogleju
Zespół skupił się na cząsteczce sygnalizacyjnej zwanej TGF-beta, która zwykle utrzymuje mikroglej w spokojnym, homeostatycznym stanie. Korzystając z genetycznie zmodyfikowanych myszy, selektywnie wyłączyli sygnalizację TGF-beta w mikrogleju w okresie dorosłości — albo poprzez usunięcie samego liganda TGF-beta, albo receptorów (ALK5 lub TβRII), które go rozpoznają. Doprowadziło to do przejścia mikrogleju w reaktywny, prozapalny profil bez wywoływania rozległej utraty neuronów. W tym stanie mikroglej zwiększał liczbę i zmieniał kształt, co wskazywało na aktywację, podczas gdy sąsiednie komórki wspomagające, astrocyty, pozostały w dużej mierze niezmienione.
Więcej nowych neuronów, lepsze przeżycie i zmieniony lęk
Gdy sygnalizacja TGF-beta była zablokowana w mikrogleju, „żłobek” hipokampa wyprodukował falę niedojrzałych neuronów oznaczonych białkiem DCX. Ten wzrost pojawił się około trzech tygodni po genetycznym przełączeniu i doprowadził do trwałego wzrostu w pełni dojrzałych neuronów kilka tygodni później. Dokładne śledzenie dzielących się komórek wykazało, że główny efekt polegał na poprawie przeżywalności nowo narodzonych neuronów, a nie jedynie na szybszym podziale komórek. Usunięcie mikrogleju całkowicie za pomocą leku nie odtworzyło tego efektu, co sugeruje, że nie sama nieobecność mikrogleju ma znaczenie, lecz specyficzny reaktywny profil powstający po wyciszeniu TGF-beta. Behawioralnie myszy z mikroglejem pozbawionym TGF-beta spędzały więcej czasu na otwartych ramionach labiryntów uniesionych, co jest powszechnie interpretowane jako zmniejszenie zachowań lękowych lub odhamowanie. Zmiany te wygasały, gdy mikroglej w niektórych modelach powracał do bardziej normalnego stanu, ale utrzymywały się w innych, gdzie mikroglej pozostawał reaktywny.
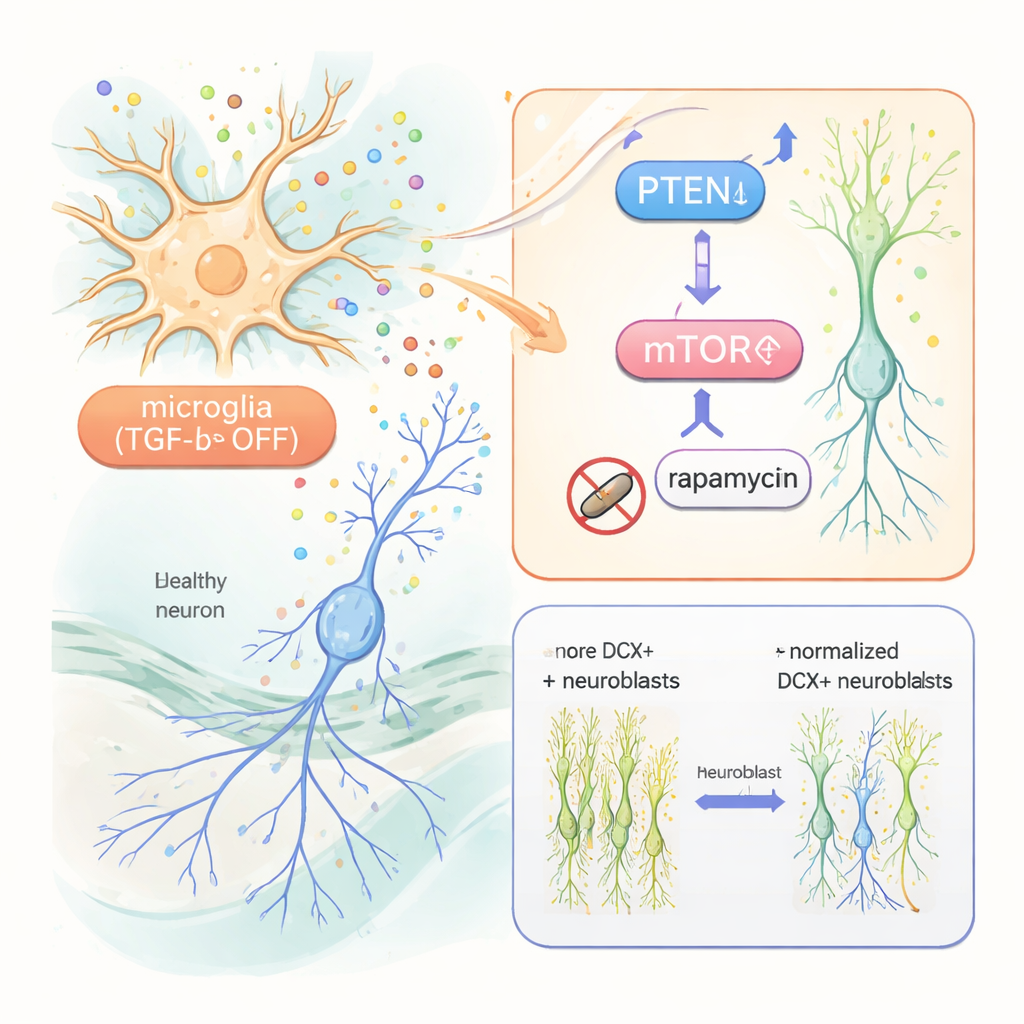
Odkrywanie szlaku w nowo narodzonych neuronach
Aby zrozumieć, jak zmieniony mikroglej komunikuje się z nowo narodzonymi neuronami, badacze użyli pojedynczo-komórkowego sekwencjonowania RNA na komórkach hipokampa. Znaleźli szerokie zmiany aktywności genów nie tylko w mikrogleju, ale także w niedojrzałych neuronach. Kluczowe wśród nich było obniżenie PTEN, białka które zwykle hamuje wzrost komórek, oraz oznaki zwiększonej aktywności szlaku mTOR, który sprzyja przeżyciu i wzrostowi komórek. Co ciekawe, dobrze znane czynniki wzrostu takie jak IGF‑1 i TNF‑alpha, choć podwyższone w reaktywnym mikrogleju, okazały się niekonieczne: nawet gdy zostały genetycznie usunięte, wzrost neurogenezy utrzymywał się. Natomiast kiedy badacze leczyli myszy rapamycyną, lekiem blokującym mTOR, nadmiar niedojrzałych neuronów i ich bujne rozgałęzienia wróciły do normy. Nowo narodzone neurony także wykazywały wyższe poziomy markera mTOR w dółszlaku, które rapamycyna zmniejszała.
Co to może znaczyć dla zdrowia mózgu
Podsumowując, wyniki sugerują, że wyłączenie sygnalizacji TGF-beta w mikrogleju powoduje przyjęcie przez te komórki reaktywnego stanu, który sprzyja przeżyciu i integracji nowo narodzonych neuronów hipokampa poprzez szlak PTEN–mTOR wewnątrz tych neuronów. To z kolei wiąże się z obniżonymi zachowaniami lękowymi u myszy, choć może też wiązać się ze zmianami w uczeniu się i pamięci. Dla laika kluczowe przesłanie jest takie, że własne komórki odpornościowe mózgu potrafią precyzyjnie regulować, ile nowych neuronów dołącza do naszych obwodów pamięciowych — i że ostrożne modulowanie tego systemu mogłoby pewnego dnia pomóc zwiększyć korzystną neurogenezę lub powstrzymać szkodliwe, nadmierne rozgałęzianie się neuronów w schorzeniach takich jak epilepsja czy po urazie mózgu.
Cytowanie: Ware, K., Peter, J., Yazell, J. et al. Inhibition of TGF-β signaling in microglia stimulates hippocampal adult neurogenesis and reduces anxiety-like behavior in adult mice. Nat Commun 17, 1440 (2026). https://doi.org/10.1038/s41467-026-68885-4
Słowa kluczowe: dorosła neurogeneza, mikroglej, hipokamp, zachowania lękowe, sygnalizacja TGF-beta