Clear Sky Science · pl
Adaptacja potranslacyjna zależna od PRMT3 podczas postu reguluje elastyczność metaboliczną
Dlaczego czas posiłków i paliwo ciała mają znaczenie
Wiele osób stosuje post lub ograniczone czasowo jedzenie, by schudnąć lub poprawić poziom cukru we krwi, ale efekty bywają różne. To badanie zagląda pod maskę naszego metabolizmu, by wyjaśnić dlaczego. Skupiając się na tłuszczu trzewnym u myszy i na próbkach ludzkich, badacze odkrywają molekularny przełącznik, który pomaga tkance tłuszczowej zdecydować, czy spalać czy magazynować paliwo, i pokazują, jak zarówno czas posiłków, jak i lek mogą przełączyć ten mechanizm na korzyść zdrowia.
Elastyczny silnik wewnątrz naszego tłuszczu
Nasze ciało działa najlepiej, gdy potrafi płynnie przełączać się między spalaniem tłuszczu podczas postu a spalaniem cukru po posiłkach. Tę „elastyczność metaboliczną” często tracimy przy otyłości, co utrudnia radzenie sobie ze zmianami w podaży i zapotrzebowaniu na energię. Zespół badał biały tłuszcz trzewny — głęboki tłuszcz brzuszny ściśle powiązany z cukrzycą i chorobami serca — i stwierdził, że określone chemiczne znaczniki na białkach, zwane grupami metylowymi, zmieniają się wraz z jedzeniem i postem. Zarówno u myszy, jak i u ludzi dwa takie znaczniki, MMA i ADMA, gromadzą się w tłuszczu trzewnym w miarę wzrostu masy ciała i indeksu masy ciała, co sugeruje, że są one wskaźnikami spowolnionego, mniej elastycznego metabolizmu.
Sygnał karmienia, który usztywnia metabolizm
Badacze skupili się na enzymie w komórkach tłuszczowych zwanym PRMT3, który dodaje te znaczniki metylowe. U myszy poziomy PRMT3 w tłuszczu trzewnym rosną w nocy, gdy zwierzęta jedzą, i spadają w ciągu dnia podczas postu, ściśle odzwierciedlając wzorzec MMA i ADMA. Ten rytm zależy od insuliny i kluczowego białka sygnałowego AKT: gdy pokarm lub wstrzyknięta insulina aktywuje AKT, PRMT3 zostaje włączony i bardziej modyfikowany, co z kolei zwiększa ilość metylowanych białek. Zablokowanie AKT lub bezpośrednie zahamowanie PRMT3 szybko wygładza ten sygnał metylacji, naśladując nawet efekt znacznie dłuższego postu.
Przeprogramowanie komórek tłuszczowych z magazynowania na spalanie
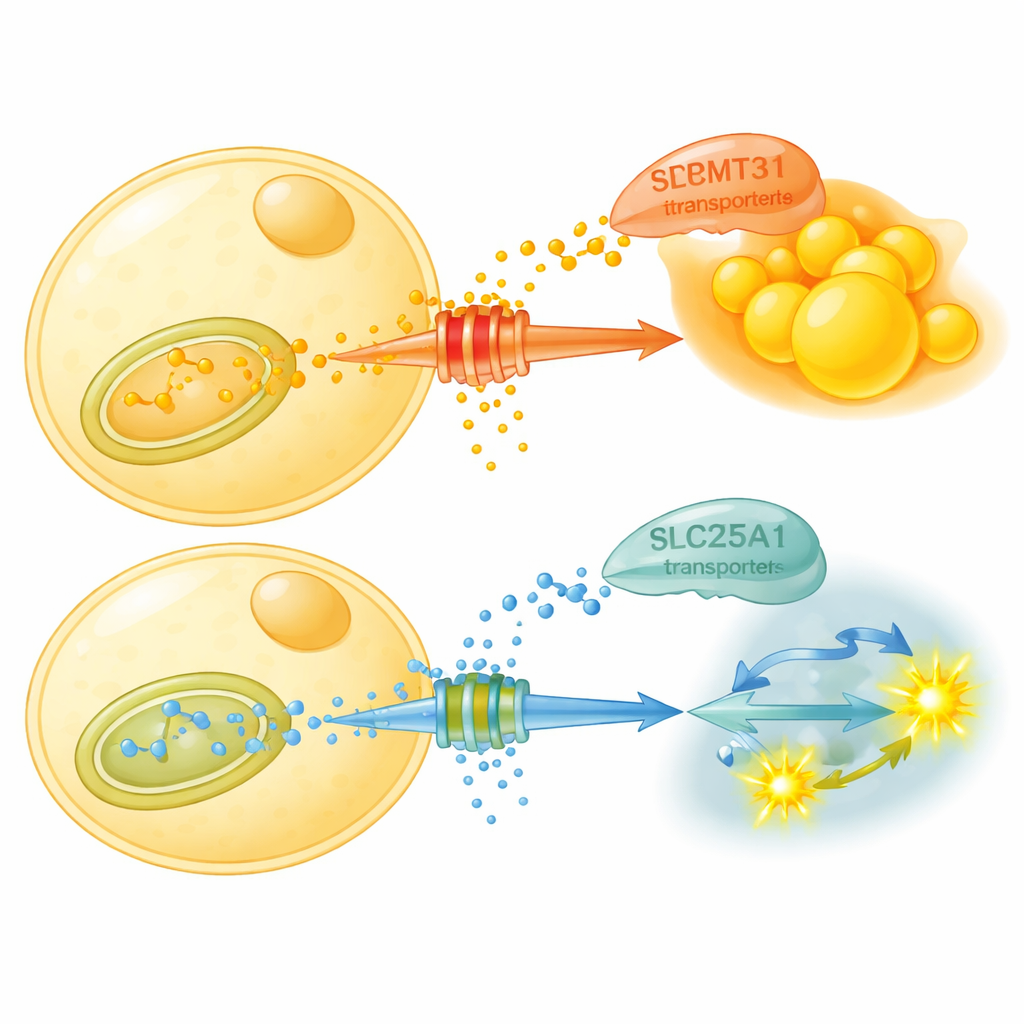
Co właściwie robi to chemiczne znakowanie? Badanie pokazuje, że PRMT3 stabilizuje białko transportowe o nazwie SLC25A1 w mitochondriach — fabrykach energetycznych komórki. SLC25A1 przenosi cytrynian, kluczowy metabolit, na zewnątrz mitochondriów do płynu komórkowego, gdzie zasila syntezę nowego tłuszczu. PRMT3 metyluje dwa konkretne miejsca argininowe na SLC25A1, co czyni transporter bardziej stabilnym i sprzyja eksportowi cytrynianu oraz budowie tłuszczu. Gdy PRMT3 jest zablokowany, poziomy SLC25A1 spadają, eksport cytrynianu maleje, a komórki tłuszczowe przechodzą w kierunku rozkładu cukru zamiast tworzenia nowego tłuszczu. U myszy na diecie wysokotłuszczowej lek blokujący PRMT3 zmniejsza tkankę tłuszczową, poprawia kontrolę glikemii i podnosi wskaźnik wymiany oddechowej (respiratory exchange ratio), co pokazuje, że zwierzęta łatwiej przełączają się na spalanie węglowodanów.
Harmonogramy postu i modyfikacje genetyczne wskazują na tę samą ścieżkę
Następnie badacze zapytali, czy powszechne schematy postu korzystają z tego samego przełącznika. W harmonogramie 16:8 — 16 godzin postu i 8 godzin jedzenia — myszy traciły na wadze i lepiej radziły sobie z glukozą bez ogólnego zmniejszenia ilości spożywanego pokarmu. Ich tłuszcz trzewny wykazywał niższe poziomy PRMT3, SLC25A1 i metylowanych białek, a wykorzystanie paliwa stało się bardziej elastyczne, szczególnie w nocy, kiedy zwykle jedzą. Co zaskakujące, podawanie leku blokującego PRMT3 o określonych porach dnia przyniosło wiele z tych samych korzyści co schemat 16:8. Genetyczne usunięcie SLC25A1 tylko w komórkach tłuszczowych również chroniło myszy przed dietozależną hiperglikemią i stłuszczeniem wątroby, ponownie zwiększając rozkład cukru i zużycie energii w tłuszczu, nawet bez zmniejszenia masy tłuszczowej.
Co to oznacza dla przyszłych terapii
Podsumowując, wyniki sugerują, że głęboki tłuszcz trzewny zawiera czuły na czasowy sygnał przełącznik, kontrolowany przez insulinę, AKT, PRMT3 i SLC25A1, który decyduje, czy nasze ciało pozostanie metabolicznie zwinne, czy utknie w trybie magazynowania. Ograniczone czasowo jedzenie wydaje się przesuwać ten przełącznik w stronę elastyczności poprzez obniżenie PRMT3 i jego efektów pośrednich. Lek hamujący PRMT3 może odtworzyć wiele z tych korzyści u otyłych myszy, co daje nadzieję na przyszły lek, który uczyni korzyści metaboliczne postu bardziej dostępne. Dla czytelników na co dzień przesłanie jest takie: kiedy jemy, nie tylko to, co jemy, może przekształcać sposób, w jaki nasza tkanka tłuszczowa gospodaruje paliwem — co ma istotne konsekwencje dla wagi, poziomu cukru we krwi i długoterminowego zdrowia.
Cytowanie: Huang, Z., Liu, X., Chen, X. et al. PRMT3-mediated post-translational adaptation to fasting regulates metabolic flexibility. Nat Commun 17, 2264 (2026). https://doi.org/10.1038/s41467-026-68883-6
Słowa kluczowe: elastyczność metaboliczna, jedzenie w ograniczonym czasie, tkanka tłuszczowa trzewna, metylacja białek, metabolizm glukozy