Clear Sky Science · pl
Immunoterapia przeciw TLR2 modyfikuje propagację α-synukleiny z neuronu do oligodendrocytu w modelach mysich i ludzkich
Dlaczego te badania są ważne
Zanik wieloukładowy (MSA) to rzadka, lecz szybko postępująca choroba mózgu łącząca objawy podobne do choroby Parkinsona z zaburzeniami równowagi i autonomicznymi, takimi jak spadki ciśnienia krwi. Lekarze potrafią złagodzić objawy, lecz obecnie nie potrafią spowolnić samej choroby. W tym badaniu ujawniono, w jaki sposób źle sfałdowany białko rozprzestrzenia się między komórkami mózgu i uszkadza „izolację przewodów” mózgowych, oraz pokazano, że celowana terapia przeciwciałami może przerwać ten proces w modelach zwierzęcych i komórkowych. Praca wskazuje namacalną, przypominającą lek strategię, która w przyszłości mogłaby zmienić przebieg MSA zamiast jedynie leczyć jej objawy.
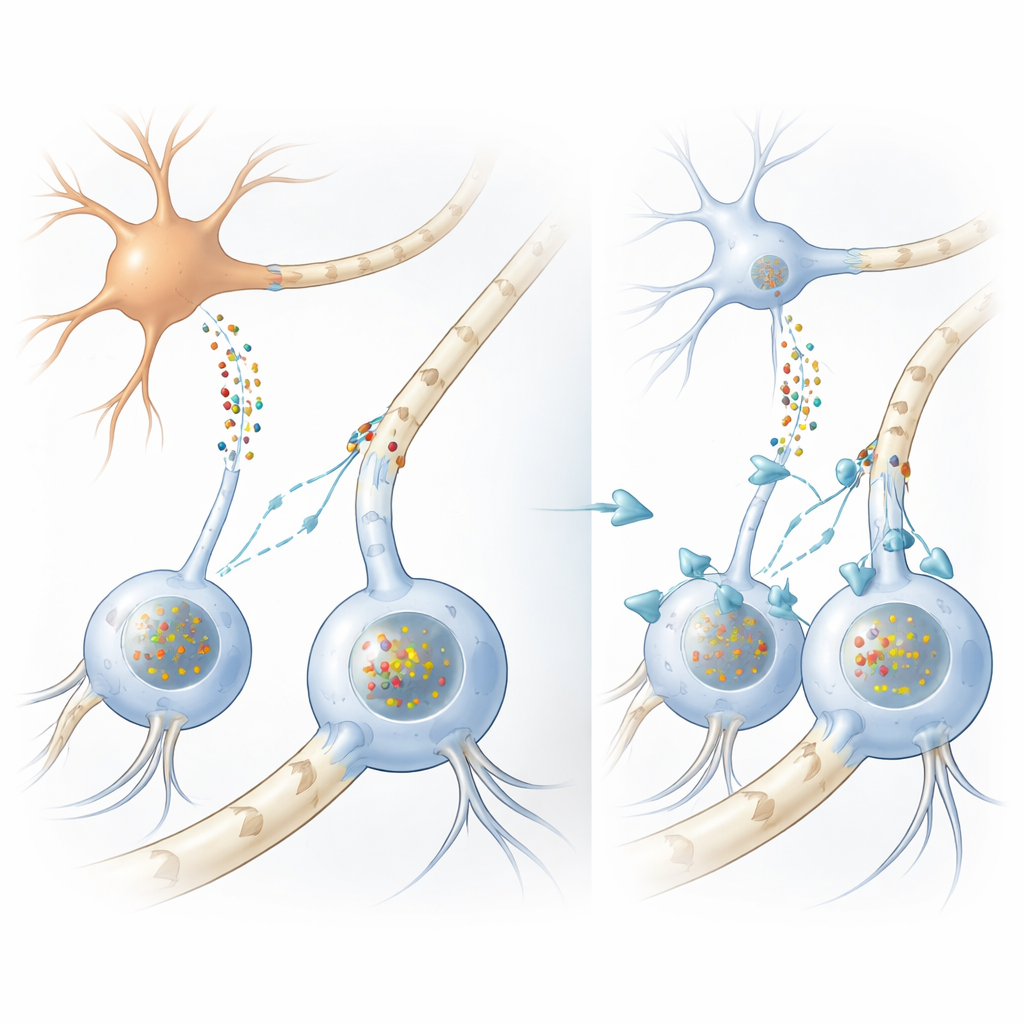
Jak zawodzi okablowanie mózgowe
W wielu zaburzeniach ruchowych, w tym w chorobie Parkinsona, w neuronach gromadzą się skupiska białka zwanego alfa-synukleiną. W MSA jednak najbardziej uderzające złogi powstają wewnątrz komórek wspierających zwanych oligodendrocytami, które normalnie owijają włókna nerwowe tłustymi osłonkami mielinowymi przyspieszającymi sygnały elektryczne. Co dziwne, oligodendrocyty same wytwarzają bardzo niewiele alfa-synukleiny, co od dawna stanowi zagadkę: skąd więc pochodzą ogromne depozyty białka w tych komórkach? Autorzy najpierw potwierdzili, analizując próbki ludzkiego mózgu i szeroko zakrojone analizy RNA, że oligodendrocyty rzeczywiście produkują znacznie mniej alfa-synukleiny niż neurony, co wzmacnia hipotezę, że szkodliwe białko musi pochodzić z zewnątrz.
Białko przekazywane z neuronu do komórki wspierającej
Aby to sprawdzić, zespół zbudował kilka uzupełniających się modeli. W hodowlach wyprowadził z komórek macierzystych neurony przypominające oligodendrocyty i zanurzył je w płynie pozyskanym z komórek neuronopodobnych zmodyfikowanych tak, by wydzielały duże ilości alfa-synukleiny. Komórki wspierające wchłonęły to białko i rozwinęły grudki bardzo podobne do inkluzji glejowych obserwowanych w mózgach osób z MSA, z tymi samymi modyfikacjami chemicznymi i białkami pomocniczymi. Gdy badacze przyjrzeli się myszom linii produkującej ludzką mutantową alfa-synukleinę wyłącznie w neuronach, ponownie znaleźli ludzkie złogi białka w oligodendrocytach w istocie białej, mimo że te komórki nie wykazywały ekspresji ludzkiego genu. Razem te eksperymenty pokazują, że alfa-synukleina może przemieszczać się z neuronów do oligodendrocytów i tam tworzyć inkluzje przypominające chorobowe.
Bramka na powierzchni komórki
Następnie naukowcy zastanawiali się, jak białko wnika do oligodendrocytów. Wcześniejsze prace wskazały, że receptor odpornościowy Toll-podobny 2 (TLR2) na powierzchni komórek działa jako miejsce dokowania dla alfa-synukleiny w neuronach i mikrogleju. Analizując zestawy danych ekspresji genów z mózgów osób z MSA, zespół odkrył, że oligodendrocyty pacjentów wykazywały nietypowo wysokie poziomy TLR2 w porównaniu z kontrolami, a wyższe TLR2 wiązało się z niższą ekspresją genów związanych z mieliną, takich jak białko podstawowe mieliny. Ten związek nie pojawiał się w kilku niezależnych zestawach danych z choroby Parkinsona, co sugeruje, że wrażliwość oligodendrocytów na alfa-synukleinę za pośrednictwem TLR2 jest cechą charakterystyczną MSA, a nie ogólną cechą wszystkich zaburzeń synukleinopatii.
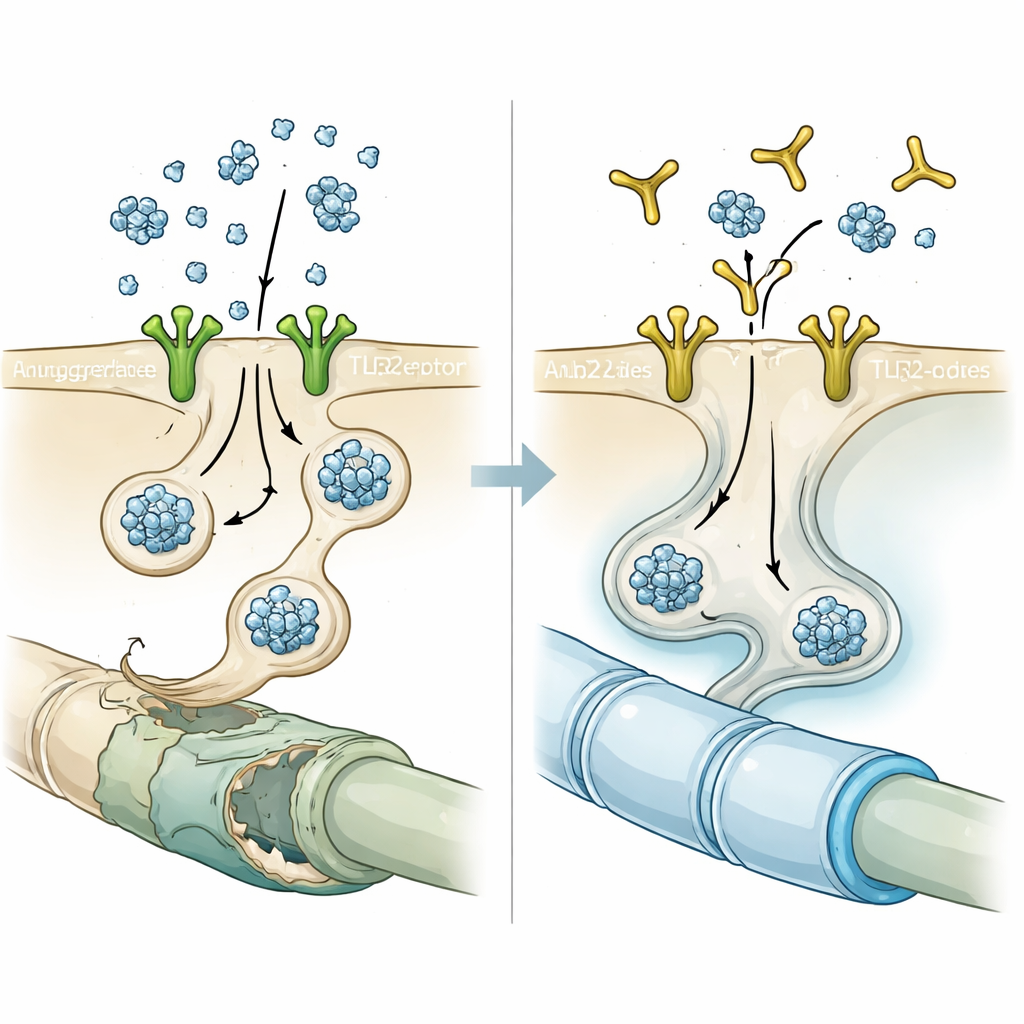
Zablokowanie bramki przeciwciałem
Mając tę wskazówkę, badacze przetestowali NM-101, przeciwciało zaprojektowane tak, by wiązać się z TLR2 i zapobiegać jego aktywacji. W hodowlach komórkowych krótkie wstępne traktowanie oligodendrocytów NM-101 przed dodaniem neuronalnie pochodzącej alfa-synukleiny znacząco zmniejszyło liczbę i intensywność inkluzji. U myszy, które albo nadprodukowaly neuronalną alfa-synukleinę, albo otrzymały wstrzyknięcia wcześniej uformowanych włókien alfa-synukleiny, cotygodniowe infuzje NM-101 obniżyły poziom agregowanego białka w istocie białej, złagodziły odpowiedzi zapalne mikrogleju i astrocytów oraz zmniejszyły aktywację enzymu zapalnego caspase-1 wewnątrz oligodendrocytów. Leczone zwierzęta żyły dłużej i wypadły lepiej w testach motorycznych, co sugeruje, że ochronne efekty przeciwciała miały znaczenie funkcjonalne, a nie były jedynie mikroskopijną ciekawostką.
Odbudowa uszkodzonej izolacji
Ponieważ oligodendrocyty są twórcami mieliny w mózgu, zespół sprawdził, czy transfer alfa-synukleiny uszkadza mielinę i czy blokada TLR2 może pomóc. Sekwencjonowanie RNA pojedynczych komórek ludzkich oligodendrocytów eksponowanych na neuronalnie warunkowaną alfa-synukleinę ujawniło szerokie przesunięcia — odpływ od dojrzałego stanu produkującego mielinę w stronę bardziej niedojrzałego, progenitoropodobnego profilu, z wyciszeniem wielu kluczowych genów mielinowych. Równoległe badania ekspresji genów na laserowo wyizolowanych oligodendrocytach od pacjentów z MSA i z modelu mysiego wykazały wspólny sygnaturowy wzorzec: zmniejszoną ekspresję genów uczestniczących w tworzeniu i utrzymaniu mieliny. W mikroskopie elektronowym istota biała myszy z alfa-synukleiną miała cieńsze, nieuporządkowane pochewki mielinowe. Leczenie NM-101 odwróciło wiele z tych zmian, pogrubiając mielinę, przywracając poziomy białek mielinowych i normalizując ekspresję genów potrzebnych do dojrzewania oligodendrocytów.
Co to wszystko oznacza dla przyszłych terapii
Badanie wspiera spójną narrację: w MSA alfa-synukleina produkowana przez neurony może rozprzestrzeniać się do oligodendrocytów przez TLR2 na ich powierzchni, gdzie się kumuluje, wywołuje zapalenie, zaburza program rozwojowy komórek i niszczy otoczkę mielinową „okablowania” mózgu. Zablokowanie TLR2 za pomocą celowanego przeciwciała pozwoliło badaczom przerwać tę kaskadę zdarzeń w modelach mysich i komórkowych ludzkich, zmniejszając toksyczne inkluzje, łagodząc zapalenie, naprawiając mielinę oraz poprawiając przeżycie i funkcje ruchowe. Choć sam NM-101 wymaga jeszcze rygorystycznych badań u ludzi, praca identyfikuje transfer białka zależny od TLR2 jako centralny mechanizm patologii podobnej do MSA i wskazuje immunoterapię anty-TLR2 jako obiecującą strategię spowolnienia bądź zapobiegania tej wyniszczającej chorobie.
Cytowanie: Bae, EJ., Ham, S., Jeong, Y.W. et al. Anti-TLR2 immunotherapy modulates neuron-to-oligodendrocyte propagation of α-synuclein in mouse and human models. Nat Commun 17, 2175 (2026). https://doi.org/10.1038/s41467-026-68870-x
Słowa kluczowe: zanik wieloukładowy, alfa-synukleina, oligodendrocyty, uszkodzenie mieliny, immunoterapia