Clear Sky Science · pl
Antyrównoległe układanie pili Csu napędza trójwymiarowy montaż biofilmów Acinetobacter baumannii
Jak szpitalne zarazki budują osłonięte miasta
Niektóre z najtrwalszych zarazków szpitalnych przetrwają antybiotyki, ukrywając się w śluzowatych, trójwymiarowych społecznościach zwanych biofilmami. To badanie stawia proste, lecz kluczowe pytanie: jak pojedyncze bakterie splatają się, by stworzyć tak wytrzymałe, warstwowe struktury? Dzięki powiększeniu za pomocą zaawansowanej mikroskopii elektronowej badacze odkryli mikroskopijny „rzep” złożony z włoskowatych filamentów, który pozwala groźnemu patogenowi Acinetobacter baumannii wplatać się w ochronne, trójwymiarowe skupiska. Zrozumienie tej ukrytej rusztowaniowej struktury może otworzyć nowe sposoby rozbijania biofilmów i poprawienia skuteczności istniejących leków.
Maleńkie włoski trzymające bakterie razem
A. baumannii, główna przyczyna trudnych do leczenia zakażeń szpitalnych, pokryta jest cienkimi włoskami powierzchniowymi zwanymi pili Csu. Wcześniejsze prace pokazały, że te pili są niezbędne do formowania wytrzymałych, kopułowatych biofilmów, ale nikt nie wiedział, jak dokładnie splatają komórki w strukturę 3D. Korzystając z różnych metod mikroskopii elektronowej, autorzy najpierw potwierdzili, że w hodowli płynnej pili zwykle wystają pojedynczo z każdej bakterii, niczym kolce koszyka. W gęstych koloniach rosnących na powierzchni obraz zmienia się jednak dramatycznie: wiele pili ciasno się pakuje, tworząc szerokie, płaskie pasma biegnące między sąsiednimi komórkami, tworząc delikatnie wyglądającą, ale rozległą sieć w trzech wymiarach. 
Płaskie drabiny zbudowane z parowanych filamentów
Aby wyjaśnić, jak powstają te pasma, zespół oczyścił pili Csu i obserwował ich zachowanie samodzielnie. W ciągu dni do tygodni pojedyncze filamenty zaczęły łączyć się parami, a następnie scalać w wielofilamentowe „superstaki”, ostatecznie tworząc żelopodobną sieć, która wiernie odtwarzała struktury widziane w prawdziwych biofilmach. Wysokorozdzielcza kriomikroskopia elektronowa ujawniła leżący u podstaw projekt. Każdy pilus nie jest gładką rurką, lecz zygzakowatym prętem. Gdy dwa pręty leżą obok siebie w przeciwnych kierunkach, stykają się w powtarzających się punktach narożnych, tworząc stabilne boczne połączenia. Wiele takich antyrównoległych par może następnie ustawić się w bardzo cienkie, arkuszowate stosy — w istocie mikroskopijną drabinę lub wstęgę, która ma tylko jedną grubość filamentu, ale wiele filamentów szerokości.
Wbudowany plan trójwymiarowego wzrostu
Szczegółowe struktury pokazują, że zdolność do takiego układania jest zakodowana w samej geometrii pili. Wzór zygzaka powtarza się na bardzo krótkim odcinku, tworząc wiele potencjalnych punktów kontaktowych wzdłuż każdego filamentu. W rezultacie, gdy dwa pili spotkają się w odpowiedniej orientacji, może powstać łańcuch połączeń przypominający zamek błyskawiczny, szybko wydłużając arkusz. Co ważne, sposób, w jaki pręty są skierowane, sprawia, że kontakty zwykle tworzą się między pili pochodzącymi z różnych komórek, a nie z tej samej, co naturalnie sprzyja łączeniu komórek. Stosy pozostają elastyczne i rozciągliwe, dzięki czemu rosnący biofilm może absorbować naprężenia fizyczne bez rozpadu. Badacze zauważyli, że podczas podziału komórkowego nowe komórki potomne często mają pili ustawione twarzą w twarz, co sprzyja formowaniu stosów dokładnie tam, gdzie potrzebne jest wiązanie komórek w trójwymiarowe skupisko. 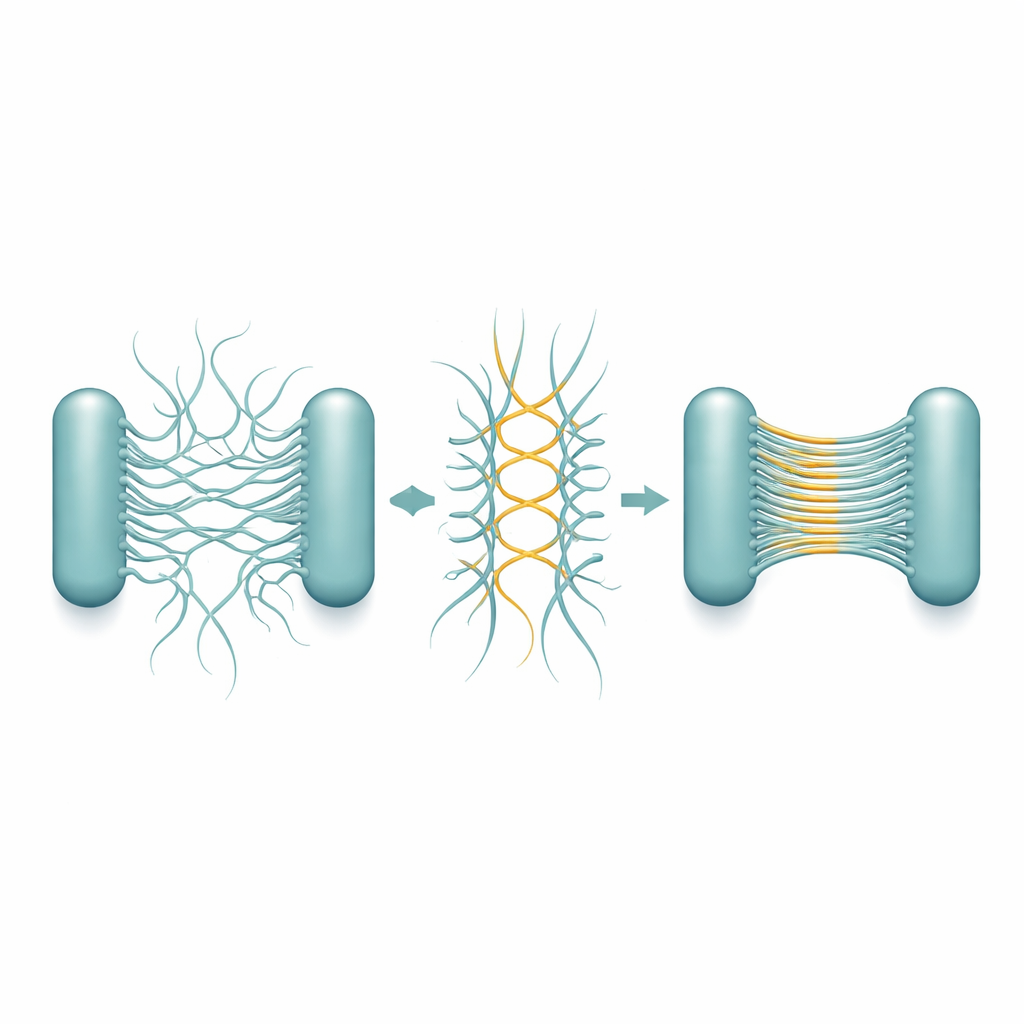
Klej, wypełniacz i wczesne rusztowanie
W badaniu przeanalizowano również, jak inne składniki biofilmu przyczyniają się do jego budowy. Cukrowy polimer zwany PNAG oraz luźne DNA pochodzące z uszkodzonych komórek gromadzą się w dojrzałych biofilmach. Mikroskopia ujawniła, że substancje te wypełniają wąskie szczeliny między bakteriami i owijają się wokół stosów pili, niczym beton wlewany wokół stalowego zbrojenia. Jednak gdy zespół usunął PNAG i DNA, bakterie nadal tworzyły uporządkowane tratwy trzymane razem wyłącznie przez stosy pili Csu. To pokazuje, że pili budują podstawowe rusztowanie, podczas gdy otaczający materiał później je zatapia i stabilizuje.
Nowe słabe punkty w bakteryjnych twierdzach
Mówiąc prościej, praca ta wyjaśnia, jak A. baumannii używa swoich włosków powierzchniowych, by wplatać się w wytrzymałe, wielowarstwowe grudki, które są trudne do przeniknięcia dla leków i komórek układu odpornościowego. Pili służą najpierw jako haczyki do chwytania powierzchni, a potem jako elastyczne pasy, które układają się w płaskie arkusze, wiążąc sąsiednie komórki we wszystkich kierunkach. Polimery cukrowe i DNA wypełniają szczeliny, przekształcając tę sieć pasów w solidną twierdzę. Poprzez wskazanie dokładnego sposobu, w jaki pili łączą się ze sobą, badanie uwydatnia nowy cel: leki lub cząsteczki blokujące kontakty pilus–pilus mogłyby osłabić rusztowania biofilmów od wewnątrz, ułatwiając usuwanie długotrwałych zakażeń bakteryjnych.
Cytowanie: Malmi, H., Pakharukova, N., Paul, B. et al. Antiparallel stacking of Csu pili drives Acinetobacter baumannii 3D biofilm assembly. Nat Commun 17, 2508 (2026). https://doi.org/10.1038/s41467-026-68860-z
Słowa kluczowe: biofilmy, Acinetobacter baumannii, pili, oporność na antybiotyki, krioczopowa mikroskopia elektronowa