Clear Sky Science · pl
Wczesne wykrywanie nieprawidłowego losu komórek i naprawy za pomocą krążących komórek progenitorowych u pacjentów z kostnieniem heterotopowym
Kiedy kość rośnie tam, gdzie nie powinna
Czasami, po poważnym urazie lub operacji stawu, kość zaczyna rosnąć w mięśniach i innych tkankach miękkich tam, gdzie nie powinna. Ten stan, zwany kostnieniem heterotopowym, może zablokować stawy, powodować silny ból i uczynić codzienne czynności niemal niemożliwymi. Lekarze obecnie rozpoznają go dopiero wtedy, gdy niechciana kość już się uformowała, co jest za późno, by temu zapobiec. W badaniu postawiono proste, lecz istotne pytanie: czy rutynowe pobranie krwi mogłoby ostrzec nas na tygodnie przed pojawieniem się tej ukrytej kości?
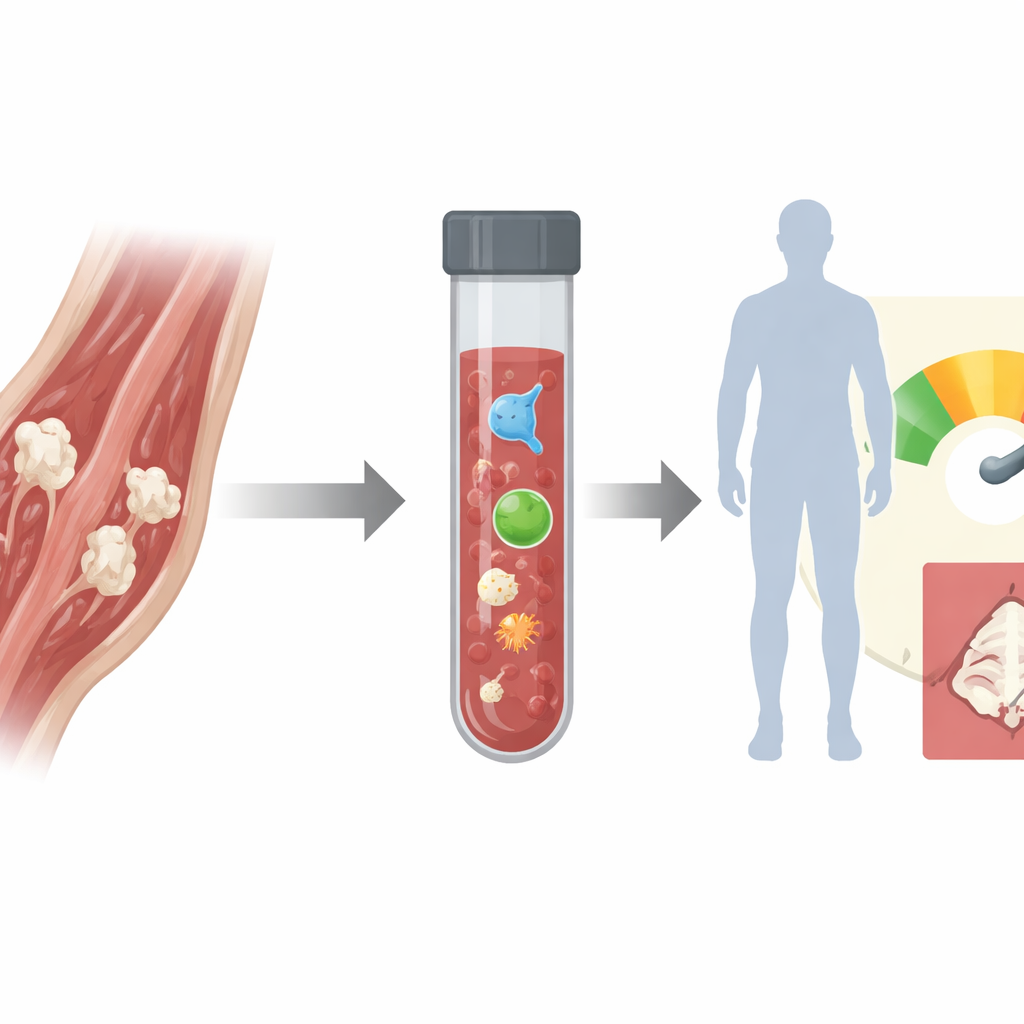
Ukryte zagrożenie po urazie i operacji
Kostnienie heterotopowe występuje zaskakująco często po ciężkich oparzeniach, wybuchowych urazach bojowych, złamaniach, a szczególnie po operacjach wymiany stawu biodrowego. Jednak dostępne dziś narzędzia — zdjęcia rentgenowskie, tomografia komputerowa i scyntygrafia kości — wykrywają je dopiero po sześciu do ośmiu tygodniach, gdy nowa kość jest już dojrzała. Istnieją metody ochronne, takie jak radioterapia czy silne leki przeciwzapalne, ale mają poważne skutki uboczne i często stosuje się je szeroko, ponieważ nie umiemy określić, kto faktycznie ich potrzebuje oraz kiedy je rozpocząć i przerwać. W efekcie wielu pacjentów albo otrzymuje ryzykowne leki niepotrzebnie, albo przegapia wąskie okno, w którym te leki mogłyby zapobiec powstawaniu dodatkowej kości.
Śledzenie rzadkich komórek naprawczych we krwi
Zespół badawczy skupił się na specjalnej grupie komórek naprawczych zwanych mezenchymalnymi komórkami progenitorowymi, które normalnie pomagają odbudowywać kość i tkanki łączne. Po niektórych urazach niewielka liczba tych komórek przedostaje się do krwiobiegu. Korzystając z urządzenia mikrofluidycznego — chipu, który sortuje komórki przepływające przez wąskie kanały — naukowcy wyłowili te rzadkie krążące mezenchymalne komórki progenitorowe z próbek krwi myszy i pacjentów poddawanych operacji wymiany biodra. Odkryli, że zaledwie kilka godzin po urazie, który później doprowadzi do kostnienia heterotopowego, te krążące komórki wykazują charakterystyczny wzór aktywnych genów, odmienny zarówno od normalnych komórek krwi, jak i od próbek pobranych po urazach, które nie skutkują powstawaniem dodatkowej kości.
Przekształcanie wzorców genowych w test wczesnego ostrzegania
Porównując krew pacjentów, u których rozwinęło się kostnienie heterotopowe, z krwią tych, u których do tego nie doszło, oraz dopasowując te wyniki do szczegółowych badań na myszach, zespół zidentyfikował zestaw 32 genów, które razem tworzą molekularny „odcisk” szkodliwego tworzenia kości. Następnie zastosowano algorytmy uczenia maszynowego do wytrenowania modelu predykcyjnego, który analizuje wyłącznie poziomy aktywności tych genów w krążących komórkach progenitorowych. W próbkach ludzkich test oparty na krwi poprawnie zidentyfikował do 90 procent przyszłych przypadków, unikając przy tym fałszywych alarmów u wszystkich pacjentów, którzy pozostali zdrowi. Co zaskakujące, sygnatura genowa pojawiała się już po sześciu godzinach od operacji lub urazu — ponad miesiąc przed tym, jak standardowe obrazowanie może wykryć nową kość.
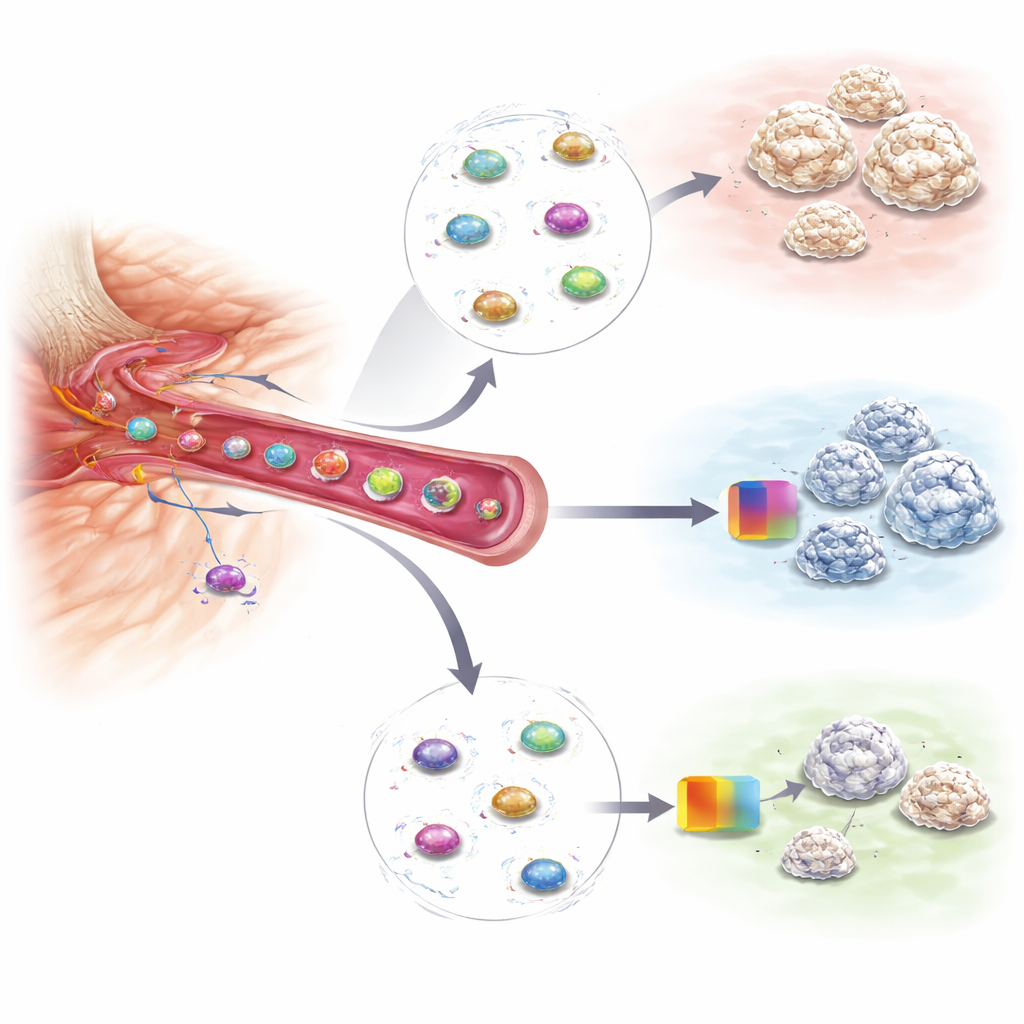
Sprawdzanie, czy leczenie rzeczywiście działa
To samo podejście oparte na badaniu krwi okazało się także przydatne do monitorowania terapii. W modelu myszy badacze leczyli ranne zwierzęta lekiem blokującym enzym zaangażowany w usztywnianie macierzy tkankowej, który wiadomo, że zmniejsza kostnienie heterotopowe. Gdy leczenie było skuteczne, sygnatura genowa w krążących komórkach progenitorowych gwałtownie spadała, a zwierzęta później rozwijały znacznie mniejsze obszary dodatkowej kości. Inne typy urazów, które nie powodują kostnienia heterotopowego, takie jak uszkodzenie mięśni czy uraz głowy, nie wykazywały tego samego wzrostu tych komórek ani ich wzorca genowego, co podkreśla specyficzność testu. Sugeruje to, że wielokrotne pobrania krwi mogłyby zarówno wskazywać pacjentów o wysokim ryzyku, jak i ujawniać, w niemal rzeczywistym czasie, czy profilaktyczne leczenie przynosi efekt.
Co to może znaczyć dla pacjentów
W sumie wyniki wskazują na przyszłość, w której prosty test krwi mógłby kierować wysoce spersonalizowaną opieką po poważnych urazach lub operacjach stawów. Zamiast traktować wszystkich jednakowo, klinicyści mogliby identyfikować osoby, których komórki naprawcze zmierzają w stronę tworzenia kości w niewłaściwym miejscu, rozpoczynać wczesne terapie zapobiegawcze i przerywać je, gdy niebezpieczna sygnatura genowa zaniknie. Poza kostnieniem heterotopowym podobne „płynne biopsje” krążących komórek naprawczych mogą pomóc lekarzom śledzić inne stany, w których gojenie się tkanek przebiega nieprawidłowo, takie jak zapalenie stawów czy włóknienie. Dla pacjentów może to oznaczać mniej powikłań, krótsze kursy ryzykownych leków i większą szansę na zachowanie sprawności i bezbólowego ruchu.
Cytowanie: Nunez, J., Holtz, M., Korlakunta, S. et al. Early detection of aberrant cell fate and repair using circulating progenitor cells in patients with heterotopic ossification. Nat Commun 17, 2231 (2026). https://doi.org/10.1038/s41467-026-68857-8
Słowa kluczowe: kostnienie heterotopowe, płynna biopsja, mezenchymalne komórki progenitorowe, wymiana stawu, wczesna diagnoza