Clear Sky Science · pl
Naśladownictwo wirusowe działa jako supresor guza w zapaleniu jelita
Ukryte DNA, które zwalcza raka
Głęboko w naszej DNA znajdują się rozległe fragmenty niegdyś lekceważone jako „śmieci”. Badanie to pokazuje, że część tego ukrytego materiału może faktycznie pomagać osobom z przewlekłym zapaleniem jelit w ochronie przed rozwojem raka jelita grubego. Działając jak fałszywe zakażenie wirusowe wewnątrz komórek, te elementy DNA uruchamiają wewnętrzny system alarmowy, który powstrzymuje niebezpieczne, od których zaczyna się rak, komórki macierzyste.
Uśpione DNA, które może się obudzić
Prawie połowa naszego genomu składa się z powtarzalnych sekwencji zwanych elementami transpozycyjnymi — odcinków DNA, które potrafią się kopiować i przemieszczać. W zdrowych komórkach te elementy są ściśle zablokowane przez chemiczne znaczniki, takie jak metylacja DNA, dzięki czemu pozostają uśpione. Jednak w niektórych chorobach i po leczeniu niektórymi lekami przeciwnowotworowymi elementy te mogą zostać ponownie włączone. Gdy tak się dzieje, produkują nietypowe dwuniciowe RNA, które dla komórki bardzo przypomina materiał genetyczny pochodzący z wirusa.
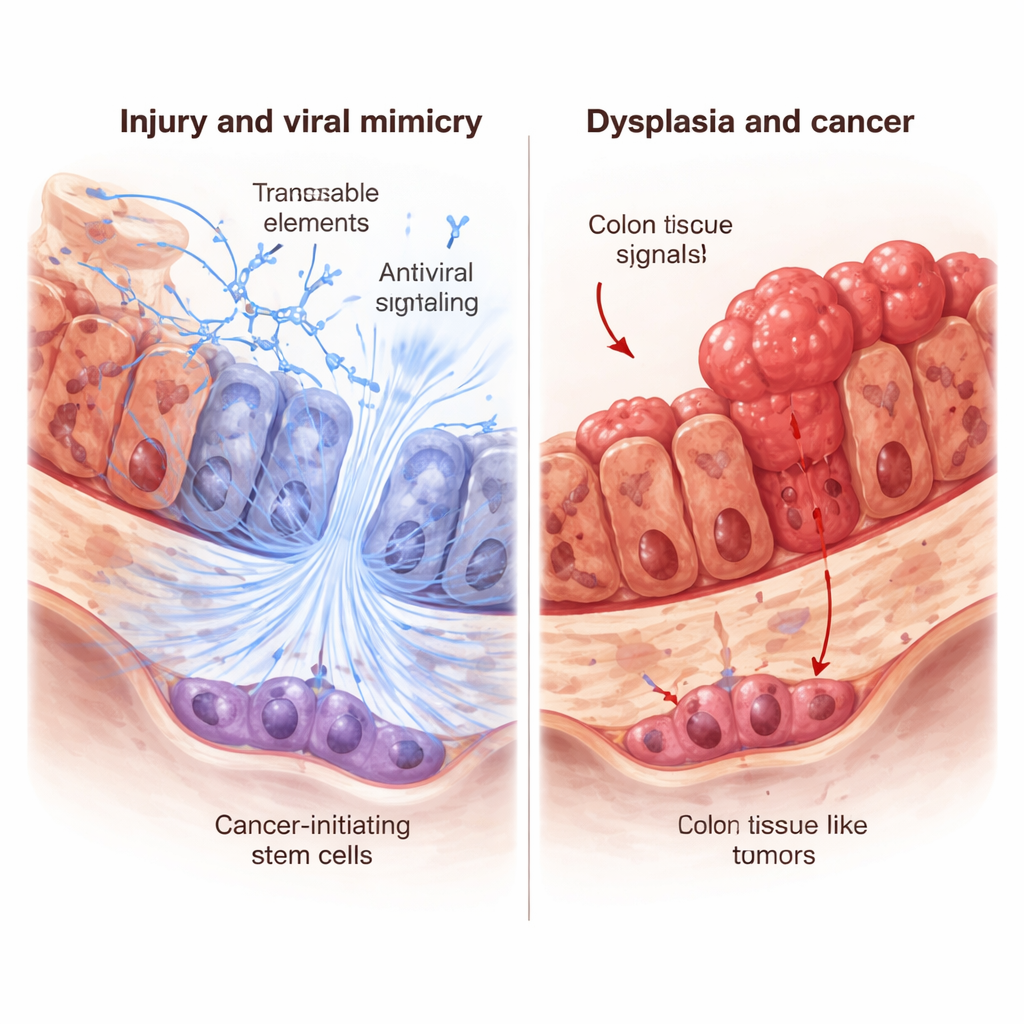
Fałszywy alarm wirusowy w zapalonych jelitach
Badacze przeanalizowali tkankę okrężnicy od osób z nieswoistym zapaleniem jelit (IBD) oraz od myszy z eksperymentalnie wywołanym zapaleniem jelita. Zarówno u ludzi, jak i u myszy aktywne zapalenie wiązało się z większą aktywnością elementów transpozycyjnych i silniejszą aktywacją genów interferonowych, które są częścią antywirusowego systemu alarmowego organizmu — zjawiska znanego jako naśladownictwo wirusowe. Jednak gdy spojrzeli na pacjentów, u których długotrwałe IBD przeszło w zmiany przedrakowe (dysplazję) lub w raka jelita grubego, zaobserwowali odwrotny wzór: zarówno elementy transpozycyjne, jak i geny związane z interferonami były wyciszone. Sugeruje to, że wyłączenie odpowiedzi na naśladownictwo wirusowe może być krokiem na drodze od przewlekłego zapalenia do nowotworu.
Obniżanie metylacji DNA, by blokować guzy
Aby sprawdzić, czy wzmocnienie tego fałszywego alarmu wirusowego rzeczywiście może powstrzymać powstawanie raka, zespół zastosował dwa podejścia zmniejszające metylację DNA w okrężnicy. Jednym z nich był lek 5‑AZA, stosowany już w niektórych nowotworach krwi; drugim była genetyczna delecja DNMT1, kluczowego enzymu utrzymującego metylację DNA, specyficznie w rzadkich komórkach DCLK1‑dodatnich, które mogą działać jako komórki macierzyste inicjujące raka. W modelach mysich, gdzie rak jelita grubego napędzany jest kombinacją uszkodzenia chemicznego i zapalenia, zarówno leczenie 5‑AZA, jak i utrata DNMT1 prowadziły do mniejszej liczby guzów, a w niektórych przypadkach także do ich mniejszych rozmiarów. Zmiany te towarzyszyły rozległa hypometylacja DNA, silna reaktywacja wielu klas elementów transpozycyjnych oraz nasilone sygnalizowanie interferonowe i JAK/STAT, co potwierdzało uruchomienie naśladownictwa wirusowego.
Rozbrojenie alarmu uwalnia komórki inicjujące raka
Białko antywirusowe MAVS znajduje się na mitochondriach i jest niezbędne do przekazywania sygnałów z czujników RNA wirusowego wewnątrz komórek. Autorzy pokazali, że wyłączenie MAVS u myszy znosiło przeciwnowotworowe korzyści zarówno 5‑AZA, jak i utraty DNMT1: guzów było więcej, a przeżywalność pogarszała się. W miniaturowych tkankach okrężnicy hodowanych w naczyniu (organoidach) aktywacja naśladownictwa wirusowego przez hypometylację DNA gwałtownie zmniejszała zdolność komórek DCLK1 z mutacją APC do zachowywania się jak komórki macierzyste i do tworzenia nowych organoidów. Usunięcie MAVS odwracało ten blok, przywracając ich zachowanie podobne do komórek macierzystych i wzrost nawet przy hypometylowanym DNA. Te eksperymenty wykazały, że naśladownictwo wirusowe ogranicza zdolność inicjowania raka przez komórki macierzyste w sposób autonomiczny dla komórki, bez potrzeby udziału komórek układu odpornościowego otaczających guz.
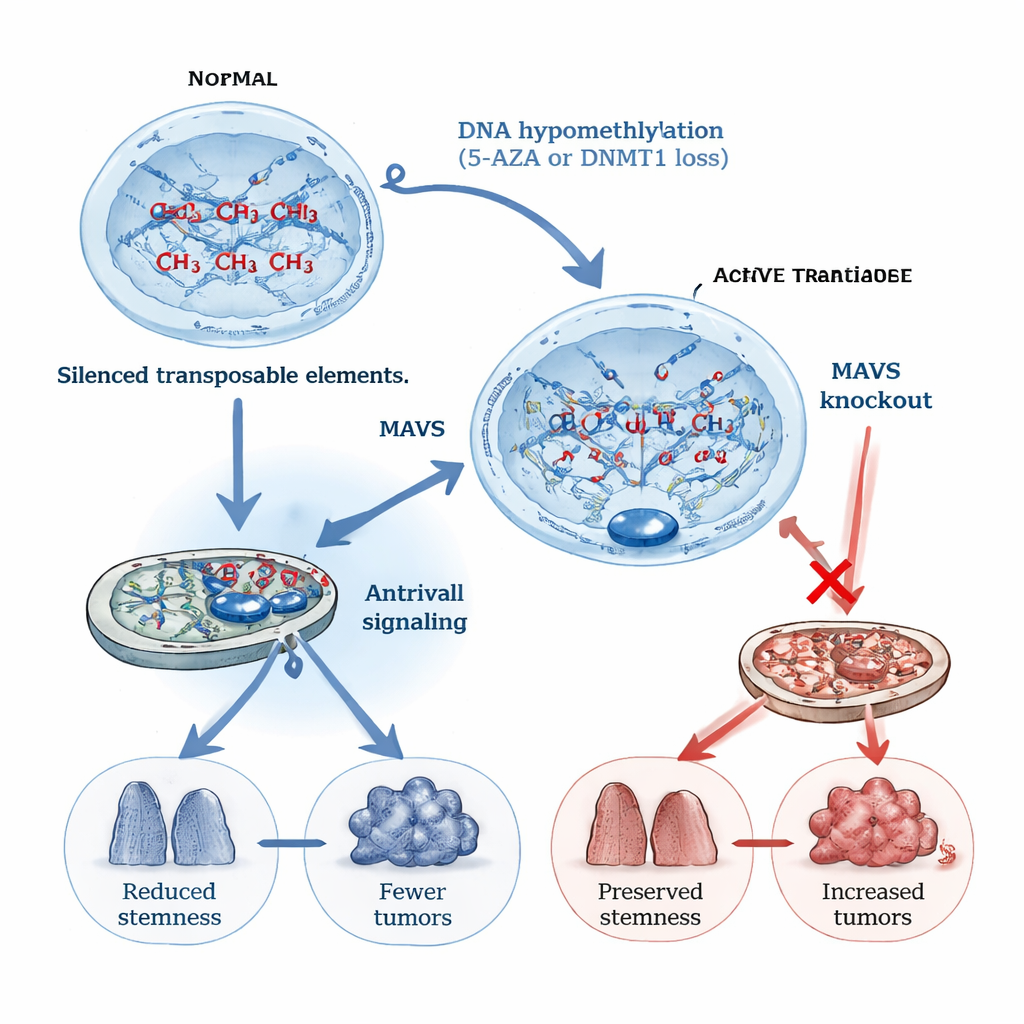
Co to oznacza dla pacjentów
Dla osób żyjących z przewlekłym zapaleniem jelita obawa przed rozwojem raka jelita grubego jest bardzo realna. Praca ta sugeruje, że częścią naturalnej obrony organizmu jest wewnętrzny „alarm wirusowy” tworzony przez ponownie przebudzone elementy transpozycyjne. Gdy ten alarm jest aktywny, ogranicza zdolność uszkodzonych komórek do przekształcenia się w pełnoprawne komórki macierzyste nowotworu; gdy jest wyciszony, nowotwory łatwiej mogą się pojawić. Terapie, które ostrożnie zwiększają naśladownictwo wirusowe — poprzez celowanie w metylację DNA lub jej regulatorów — mogą pewnego dnia pomóc zapobiegać lub leczyć raka jelita grubego, szczególnie u pacjentów wysokiego ryzyka z długotrwałą chorobą zapalną.
Cytowanie: Larsen, F., Jeong, W., Schep, D. et al. Viral mimicry acts as a tumor suppressor in colitis. Nat Commun 17, 1313 (2026). https://doi.org/10.1038/s41467-026-68850-1
Słowa kluczowe: naśladownictwo wirusowe, zapalenie jelita, rak jelita grubego, elementy transpozycyjne, metylacja DNA