Clear Sky Science · pl
Degradacja elektrody ujemnej wywołana dwustopniowym osadzaniem cynku i jej odwracanie w bateriach cynkowych
Dlaczego baterie cynkowe mają znaczenie w życiu codziennym
Bezpieczne i tanie magazynowanie energii elektrycznej jest kluczowe — od podtrzymania działania paneli słonecznych w domu po stabilizację sieci energetycznej. Baterie z metalicznym cynkiem są atrakcyjnymi kandydatami: cynk jest powszechny, nietoksyczny i działa w wodnych elektrolitach, które są znacznie bezpieczniejsze niż łatwopalne płyny w wielu bateriach litowych. Mimo to obiecujące ogniwa nadal tracą pojemność i szybko ulegają zwarciom. Ten artykuł ujawnia ukryty, dwustopniowy proces wzrostu na elektrodzie cynkowej, który powoduje uszkodzenia, oraz przedstawia chemiczną strategię „samoleczenia”, która znacząco wydłuża żywotność baterii.
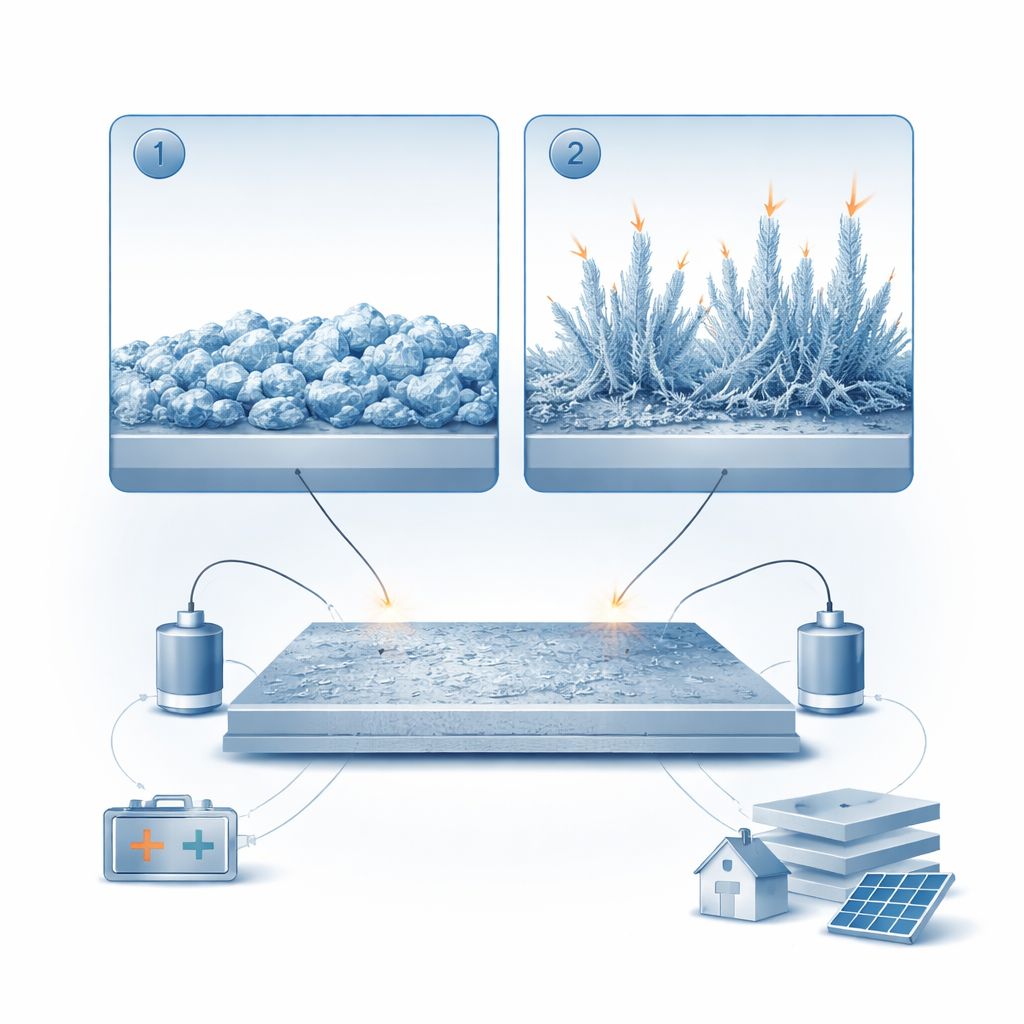
Od gładkiego metalu do „mchu” cynkowego
Elektroda ujemna w tych bateriach wykonana jest z metalu cynkowego, który podczas ładowania i rozładowania wielokrotnie się osadza (dodaje cynk) i rozpuszcza (usuwa cynk). Korzystając z przezroczystej celi wyposażonej w mikroskop, badacze obserwowali, jak cynk narasta na powierzchni metalowej w czasie. Odkryli, że cynk nie rośnie w jeden sposób, lecz przebiega w dwóch odrębnych etapach. Najpierw tworzą się stosunkowo zwarte, grudkowate kryształy, które tworzą błyszczącą, zwartą warstwę. Następnie, w miarę dalszego osadzania, z ostrych krawędzi i wierzchołków wyrastają cienkie, włókniste struktury. Ten drugi, „mossy” — czyli mchu-podobny — etap wypełnia przestrzeń między elektrodami i ostatecznie może je połączyć, grożąc wewnętrznymi zwarciami.
Jak kędzierzawy cynk staje się „martwym” cynkiem
Zespół połączył bezpośrednie obrazowanie, mikroskopię elektronową i symulacje komputerowe, by zrozumieć, dlaczego pojawia się ta warstwa mchu. Ostro zakończone wypustki na grudkowatym cynku koncentrują pole elektryczne — efekt podobny do działania piorunochronów skupiających wyładowania. To skupienie przyciąga więcej jonów cynku na końcówki, napędzając szybki, włóknisty wzrost. Podczas procesu odwrotnego, gdy cynk jest usuwany, filamentu mchu rozpuszczają się najpierw i mogą stracić kontakt elektryczny z podłożem metalicznym. Pozostaje wtedy „martwy” cynk: małe, elektrycznie izolowane kawałki, które nie biorą już udziału w reakcji ogniwa, a mimo to zawierają wartościowy materiał aktywny — co prowadzi do utraty pojemności oraz szorstkich, niestabilnych powierzchni.
Projektowanie sprytniejszego elektrolitu
Wiedząc, że wzrost mchu wynika z lokalnego nagromadzenia jonów przy wystających miejscach, badacze zaprojektowali dodatek do elektrolitu, który przeciwdziała zarówno powstawaniu kędzierzawego cynku, jak i marnotrawstwu związanemu z „martwym” cynkiem. Użyli soli zwanej acetylcholiny jodku, która dostarcza dodatnio naładowanych organicznych kationów i anionów jodkowych w jednej cząsteczce. Zgodnie z czułymi pomiarami masy i spektroskopią w podczerwieni, kationy silnie i selektywnie adsorbują się na powierzchni cynku, tworząc cienką, dodatnio naładowaną warstwę, która wyrównuje strumień jonów cynkowych. To sprzyja gładkiemu, płaskiemu osadzaniu zamiast wzrostu włókien, utrzymując powierzchnię zwartą i bardziej odporną na korozję oraz tworzenie gazowego wodoru.
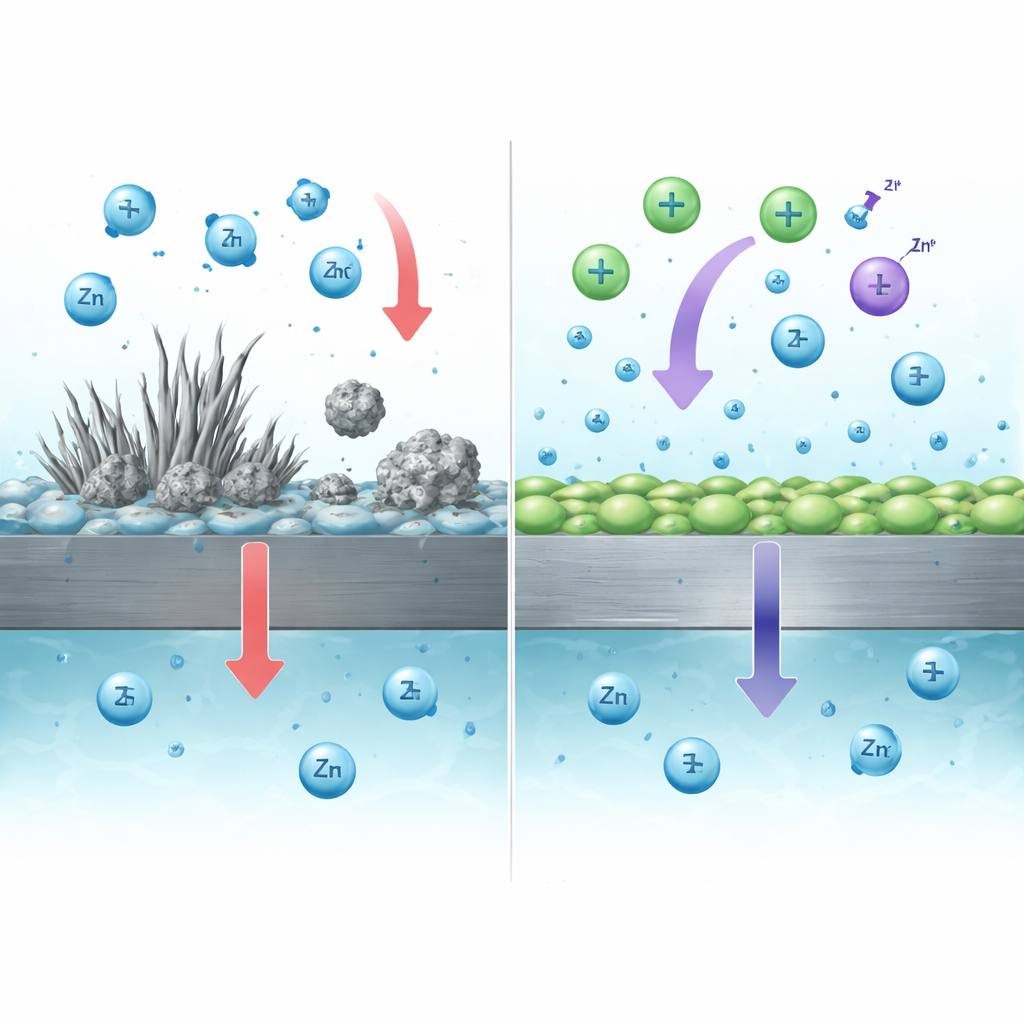
Przywracanie utraconego cynku w celu wydłużenia żywotności baterii
Cząstka jodkowa dodatku pełni inną, ale uzupełniającą rolę. Podczas ładowania jodek częściowo przekształca się w łagodny utleniacz (I3−), który może reagować z martwymi cząstkami cynku oraz z izolującymi produktami ubocznymi zawierającymi cynk, które tworzą się na powierzchni. Te reakcje zamieniają elektrycznie izolowany cynk z powrotem w rozpuszczone jony cynku, które następnie mogą ponownie osadzić się na elektrodzie w kolejnych cyklach. Eksperymenty wykazały, że martwy cynk zanurzony w roztworze zawierającym jod rozpuszczał się prawie do teoretycznego zakresu, a pełne ogniwa używające dodatku z dwoma jonami odzyskiwały więcej ładunku, niż byłoby to możliwe wyłącznie z na świeżo nałożonego cynku — jasny dowód, że wcześniej utracony cynk był „recyklingowany” wewnątrz ogniwa.
Co to oznacza dla prawdziwych baterii
Łącząc kationy wygładzające pole z anionem recyklingującym cynk, nowy elektrolit pozwolił uzyskać elektrody cynkowe o średniej wydajności kulombowej około 99,7% i stabilnej pracy przez ponad 1400 godzin przy wysokim prądzie i pojemności — warunkach istotnych dla magazynowania na skalę sieciową. Symetryczne ogniwa cynkowe i praktyczne woreczkowe ogniwa cynk‑jod utrzymywały niskie straty napięcia i zachowały ponad 96% pojemności po setkach do dziesiątek tysięcy cykli, w zależności od testu. Dla laika kluczowa wiadomość jest taka, że badacze określili dokładnie, w jaki sposób degradują elektrody cynkowe — poprzez dwustopniowy, kędzierzawy wzrost, który tworzy martwy metal — i pokazali chemiczny przepis, który zarówno zapobiega tej szkodliwej strukturze, jak i przywraca utracony materiał. To dwutorowe podejście przybliża bezpieczne, wodne baterie cynkowe do długotrwałego, dużoskalowego zastosowania w domach i sieciach energetycznych.
Cytowanie: Gan, H., Liu, D., Zhang, Y. et al. Negative electrode degradation induced by two-stage zinc plating and its recovery in zinc batteries. Nat Commun 17, 2067 (2026). https://doi.org/10.1038/s41467-026-68844-z
Słowa kluczowe: baterie z metalicznym cynkiem, degradacja elektrody, kędzierzawy cynk, dodatki do elektrolitu, magazynowanie energii sieciowej