Clear Sky Science · pl
Odpowiedzi cGAS-IFN-I przez wyciąganie jądrowego DNA z umierających komórek za pomocą nukleocytozy
Jak nasz układ odpornościowy odczytuje DNA zmarłych komórek
Kiedy nasze komórki obumierają podczas infekcji, nowotworów czy codziennego zużycia, ich pozostałości muszą zostać uprzątnięte bez wywoływania nadmiernego stanu zapalnego. Artykuł ujawnia zaskakujący sposób, w jaki komórki odpornościowe mogą przeciskać się do jąder umierających komórek, wyciągać z nich DNA i wykorzystywać go jako sygnał zagrożenia. Zrozumienie tego ukrytego mechanizmu sprzątania i alarmowania może zmienić nasze podejście do leków przeciwwirusowych, autoimmunologii, terapii przeciwnowotworowej i działań niepożądanych leków.
Ukryty alarm DNA wewnątrz komórek odpornościowych
W naszych komórkach występuje czujnik zwany cGAS, który wykrywa DNA znajdujące się w niewłaściwym miejscu — swobodnie unoszące się w cytoplazmie zamiast bezpiecznie spakowanego w jądrze lub mitochondriach. Kiedy cGAS natrafi na takie DNA, uruchamia silny program alarmowy prowadzący do produkcji interferonów typu I, kluczowych białek przeciwwirusowych i regulujących odpowiedź immunologiczną. Naukowcy wiedzieli, że wirusy mogą dostarczać swoje materiał genetyczny do komórek, wywołując tę ścieżkę, oraz że fragmenty własnego DNA czasami się wydostają i powodują choroby autoimmunologiczne. Pozostała jednak podstawowa zagadka: jak duże ilości naszego DNA, szczególnie pochodzącego z martwych komórek, docierają do cGAS, zamiast zostać po prostu strawione w „żołądkach” komórkowych zwanych lizosomami?
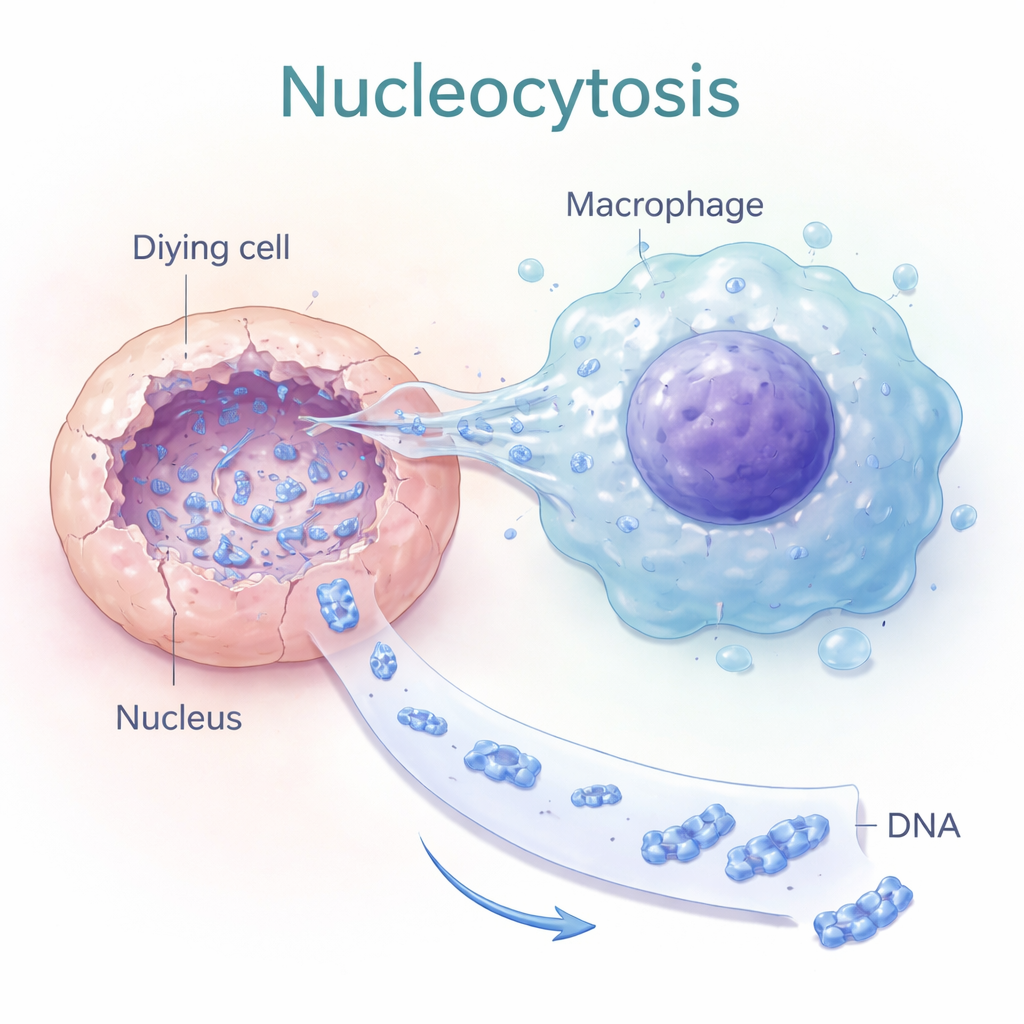
Nukleocytoza: przeciskanie się do jąder martwych komórek
Autorzy opisali proces, który nazwali „nukleocytozą”, w którym niektóre makrofagi — komórki odpornościowe zwykle pochłaniające szczątki — wykonują czynność znacznie bardziej ukierunkowaną. Zamiast połykać całą martwą komórkę, wysuwają cienkie, palcowate wypustki bezpośrednio do jądra umierającej komórki. Badania na żywych komórkach wykazały spadek intensywności sygnału DNA w jądrze umierającej komórki przy jednoczesnym wzroście w przylegającym makrofagu, co wskazuje na aktywne wydobywanie jądrowego DNA. Transfer ten zależał od wewnętrznego szkieletu komórki (aktyny) i od cząsteczek sygnałowych kontrolujących kształt komórki, co sugeruje, że nukleocytoza jest celowym zachowaniem mechanicznym, a nie pasywnym przeciekiem.
Kiedy leki przeciwwirusowe włączają alarm DNA
Podczas pandemii COVID-19 leki takie jak hydroksychlorochina były szeroko testowane jako środki przeciwwirusowe, lecz ich dokładne działanie w organizmie pozostawało niejasne. Naukowcy odkryli, że hydroksychlorochina i kilka pokrewnych „kationowo amfifilowych” leków mogą silnie aktywować szlak cGAS–STING–interferonowy — ale tylko w podzbiorze makrofagów. Leki te zaburzają funkcję lizosomów przez podniesienie ich pH oraz blokowanie enzymu PPT1, który pomaga usuwać tłuszczowe znaczniki z białek. Połączony efekt skłania niektóre komórki do szczególnej formy śmierci, w której białko kalretikulina gromadzi się w jądrze. Makrofagi następnie preferencyjnie wysuwają wypustki w kierunku jąder bogatych w kalretikulinę, wydobywają DNA przez nukleocytozę i wywołują intensywną produkcję interferonów w zaledwie kilku komórkach — wystarczającą, by wygenerować silny lokalny sygnał przeciwwirusowy bez zalewania całego organizmu.
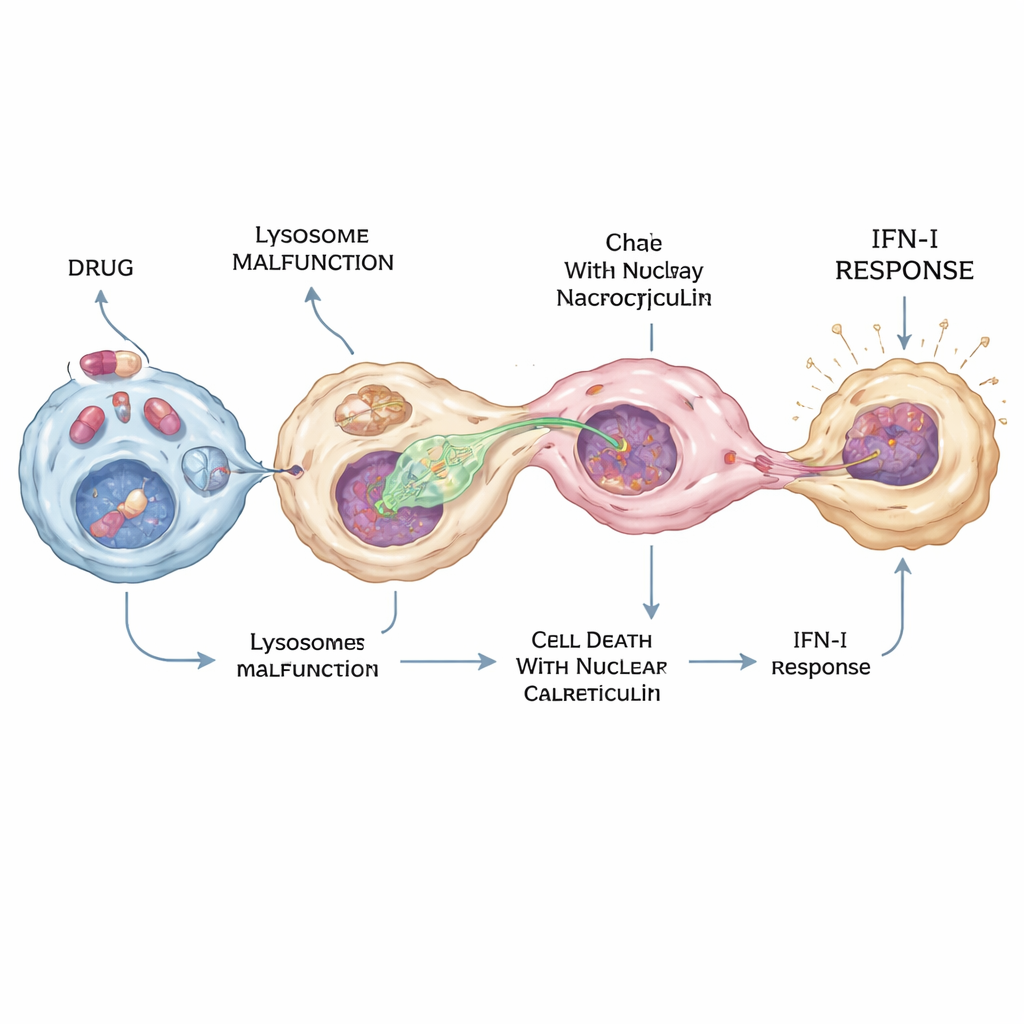
Od lokalnej obrony do chorób i działań niepożądanych
Poprzez badania zarówno hodowli komórkowych, jak i płuc myszy, zespół wykazał, że makrofagi traktowane lekami mogą wywołać odpowiedź interferonową zależną od STING, która pozostaje w dużej mierze lokalna — na przykład w płucu — zamiast stać się ogólnoustrojowa. Pomaga to wyjaśnić, dlaczego leki takie jak hydroksychlorochina mogą wykazywać korzyści przeciwwirusowe lub przeciwnowotworowe w niektórych tkankach, ale też dlaczego przy długotrwałym stosowaniu mogą powodować toksyczność narządową, np. w oczach czy sercu. Ten sam proces nukleocytozy mógłby prawdopodobnie przyczyniać się do chorób autoimmunologicznych lub zapalnych zawsze, gdy martwe komórki i stres lizosomalny pokrywają się czasowo, ponieważ daje bezpośrednią drogę dla własnego DNA do uruchomienia alarmu cGAS.
Dlaczego to ma znaczenie dla przyszłych terapii
Dla osoby nietechnicznej kluczowy przekaz jest taki, że komórki odpornościowe nie tylko biernie zjadają martwe komórki; mogą aktywnie eksploatować ich jądra w poszukiwaniu DNA i używać go jako sygnału wzywającego pomoc. Ta ścieżka nukleocytozy wyjaśnia, jak własne DNA może bezpiecznie aktywować potężne obrony przeciwwirusowe w sposób skoncentrowany i lokalny, jednocześnie uwypuklając, jak leki zaburzające funkcję lizosomów lub PPT1 mogą niezamierzenie przełączyć ten mechanizm. Ucząc się regulować nukleocytozę — podnosząc lub obniżając jej aktywność, poprzez projektowanie mądrzejszych leków przeciwwirusowych i terapii przeciwnowotworowych lub unikając niechcianych sygnałów własnego DNA w chorobach autoimmunologicznych — badacze mają nadzieję wykorzystać ten nowo odkryty mechanizm dla bezpieczniejszych, bardziej precyzyjnych terapii.
Cytowanie: Negishi, H., Wada, Y., Shirasaki, Y. et al. cGAS-IFN-I responses by extracting nuclear DNA from dying cells via nucleocytosis. Nat Commun 17, 1658 (2026). https://doi.org/10.1038/s41467-026-68839-w
Słowa kluczowe: nukleocytoza, cGAS-STING, hydroksychlorochina, interferon typu I, makrofagi