Clear Sky Science · pl
Rozwój niskonapięciowej fotoredoksowej katalizy manganu od fotokatalizy światłem widzialnym o wysokiej energii
Ściszenie światła, zachowanie reakcji
Chemicy często używają jasnego, wysokoenergetycznego światła — na przykład intensywnych lamp niebieskich lub ultrafioletowych — aby napędzać reakcje budujące złożone cząsteczki. Jednak takie „twarde” światło może marnować energię, uszkadzać wrażliwe fragmenty molekuł i jest trudne do zastosowania głęboko w tkankach czy dużych reaktorach. W tym badaniu pokazano, jak proste, niedrogie sole manganu można złożyć bezpośrednio w naczyniu reakcyjnym, aby działały z dużo łagodniejszym światłem czerwonym i bliską podczerwienią, zachowując jednocześnie silne zdolności do tworzenia wiązań cenione w badaniach nad lekami i nauce o materiałach.
Dlaczego łagodniejsze światło ma znaczenie
Wysokoenergetyczne światło przypomina używanie palnika do zapalenia świecy: wykonuje zadanie, ale może też przypalać wszystko w pobliżu. W reakcjach chemicznych prowadzi to do nadreakcji, niszczenia wrażliwych grup i słabej kontroli. Łagodniejsze światło — szczególnie czerwone i bliska podczerwień, które niosą mniej energii — przenika głębiej przez ciecze, a nawet tkanki biologiczne, i jest na ogół bardziej kompatybilne ze skomplikowanymi, delikatnymi cząsteczkami. Problem w tym, że większość istniejących katalizatorów napędzanych światłem jest dostrojona do absorpcji światła o wyższej energii, a ich przeprojektowanie zwykle wymaga długiej, złożonej syntezy. Autorzy postawili sobie za cel obniżenie „budżetu fotonowego” takich reakcji bez konieczności przebudowy katalizatorów od podstaw.
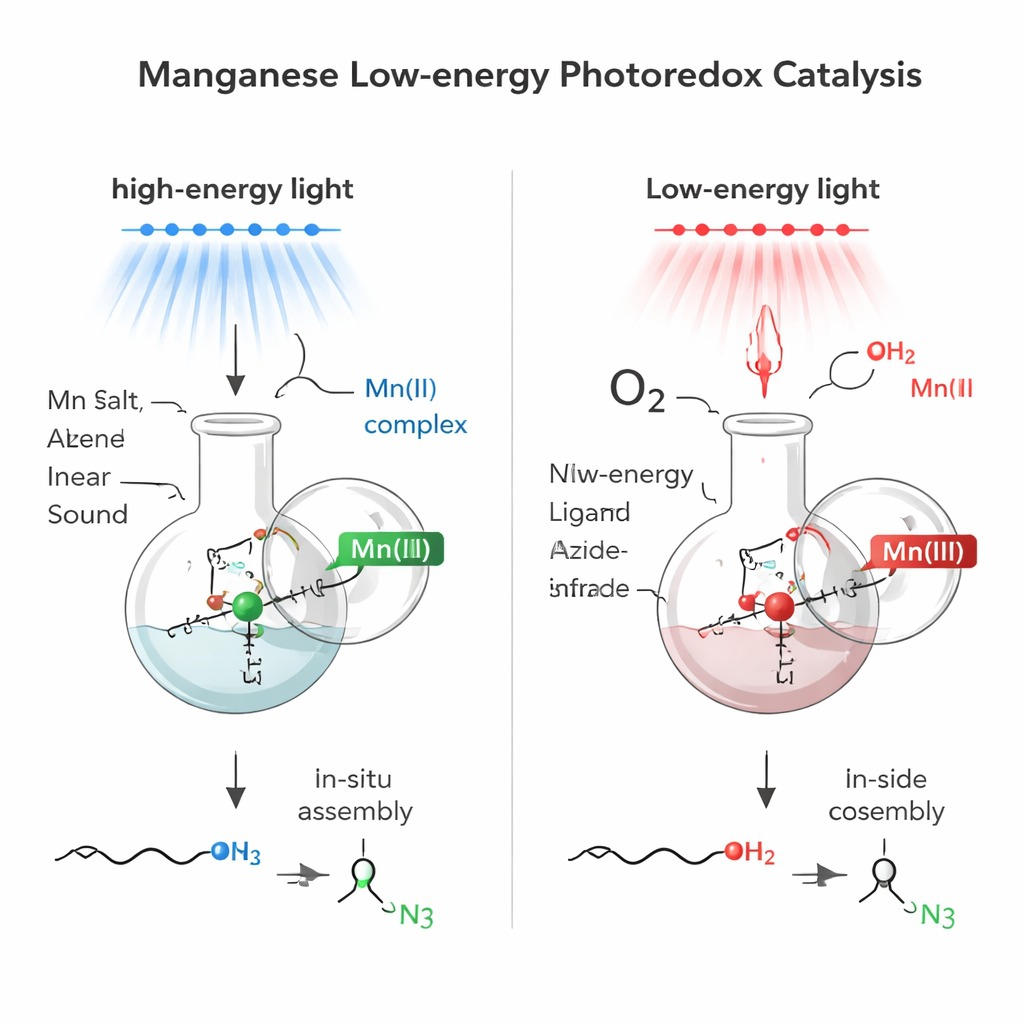
Budowanie katalizatora na miejscu
Zamiast wytwarzać złożone kompleksy metali z wyprzedzeniem, zespół zastosował strategię in situ: po prostu wymieszali dostępne w handlu sole manganu z małą cząsteczką pomocniczą (ligandem) i źródłem azotu bezpośrednio w mieszaninie reakcyjnej. Ta samoskładająca się mieszanina stworzyła system absorbujący światło oparty na manganie. W przypadku soli manganu(II) mieszanina silnie absorbowała światło niebieskie i mogła generować krótkotrwałe „rodniki azotynowe” z powszechnego odczynnika TMSN3. Te reaktywne fragmenty dodawały się następnie do prostych wiązań podwójnych węgiel‑węgiel (alkenów), umieszczając grupę azotową (N3) na mniej podstawionym końcu wiązania — wzór znany jako addycja anty‑Markownikowa. Co godne uwagi, zwykła woda służyła jako źródło wodoru, co uczyniło proces prostym i atomowo efektywnym.
Przejście z niebieskiego do głębokiej czerwieni
Następnie badacze zapytali, czy blisko spokrewniony system manganu mógłby działać przy znacznie niższej energii światła, w obszarze głębokiej czerwieni i bliskiej podczerwieni. Przechodząc od manganu(II) do manganu(III) i dopracowując środowisko reakcyjne, stworzyli nową mieszaninę absorbującą światło aż do około 850 nanometrów — dobrze w obszarze bliskiej podczerwieni. Pod tym łagodnym światłem kompleks manganu(III) nadal generował rodniki azotynowe, ale już w obecności powietrza (jako źródła tlenu) i prostego alkoholu reakcja wprowadzała jednocześnie grupę azotową i alkoholową w poprzek alkenu w jednym kroku. Wynikiem jest b2‑azydowy alkohol, szczególnie użyteczny blok budulcowy, ponieważ zawiera dwa wszechstronne „uchwyty” — N3 i OH — na sąsiednich atomach węgla.
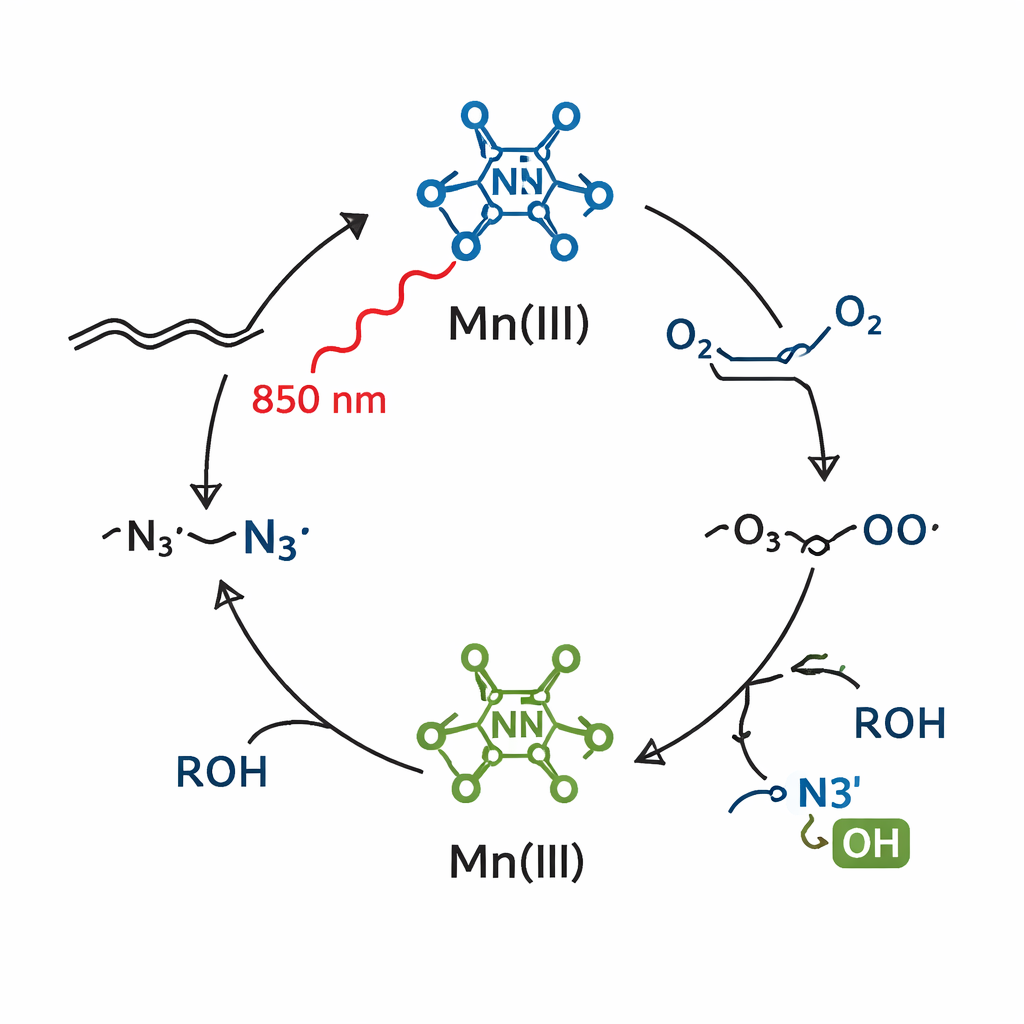
Od prostych alkenów do złożonych cząsteczek przypominających leki
Mając do dyspozycji zarówno systemy na światło niebieskie, jak i niskonapięciowe, zespół przetestował szeroką gamę alkenów. Przekształcili wiele różnych substratów w azotki alkilowe lub b2‑azydowe alkohole w umiarkowanych do wysokich wydajnościach, nawet gdy cząsteczki nosiły grupy zwykle przeszkadzające katalizatorom metali, takie jak niechronione aminy, alkohole, grupy zawierające siarkę czy złożone systemy pierścieniowe. Pokazali także „funkcjonalizację na późnym etapie” przez modyfikację zaawansowanych, lekopodobnych związków, przekształcając istniejące leki w nowe pochodne z dodanymi grupami azydowymi i w niektórych przypadkach alkoholowymi. Te nowe funkcje można później przekształcić w inne bogate w azot struktury lub przyłączyć do celów biologicznych, poszerzając zestaw narzędzi chemii medycznej.
Oszczędna energetycznie chemia z praktyczną obietnicą
Praca pokazuje, że można „ewoluować” reakcję zasilaną światłem niebieskim o wysokiej energii do procesu niskonapięciowego w bliskiej podczerwieni, po prostu zmieniając sposób składania powszechnej soli metalu w roztworze. Systemy manganu tworzone in situ unikają czasochłonnej syntezy katalizatora, wykorzystują obfity i stosunkowo nietoksyczny metal oraz mogą być nawet zasilane naturalnym światłem słonecznym. Dla osób niezajmujących się specjalistycznie chemią kluczowy przekaz jest taki: nie zawsze potrzebujemy silniejszego światła ani drogich metali ziem rzadkich, aby przeprowadzić wymagające reakcje. Projektując katalizatory, które same się tworzą z prostych elementów i reagują na łagodniejsze światło, podejście to wskazuje kierunek ku bardziej energooszczędnym, skalowalnym i biologicznie przyjaznym sposobom wytwarzania złożonych molekuł, od których zależy współczesna medycyna i nauka o materiałach.
Cytowanie: Yang, W., Song, Y., Yu, X. et al. Evolution of manganese low-energy photoredox catalysis from high-energy visible light photocatalysis. Nat Commun 17, 2062 (2026). https://doi.org/10.1038/s41467-026-68837-y
Słowa kluczowe: fotoredoksowa kataliza, kataliza manganu, światło niskiej energii, funkcjonalizacja alkenów, rodniki azotynowe