Clear Sky Science · pl
Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice
Turning Radiation into an Immune Ally
Onkolodzy coraz częściej starają się wykorzystać układ odpornościowy do zwalczania nowotworów, ale wiele nowotworów nadal ignoruje lub opiera się tym lekom. W tym badaniu postawiono aktualne pytanie: czy różne typy celowanego promieniowania można wykorzystać nie tylko do bezpośredniego zmniejszania guzów, lecz także do „wyszkolenia” układu odpornościowego, aby działał skuteczniej — i czy wybór radioaktywnego leku zmienia sposób, w jaki przebiega to „szkolenie”?
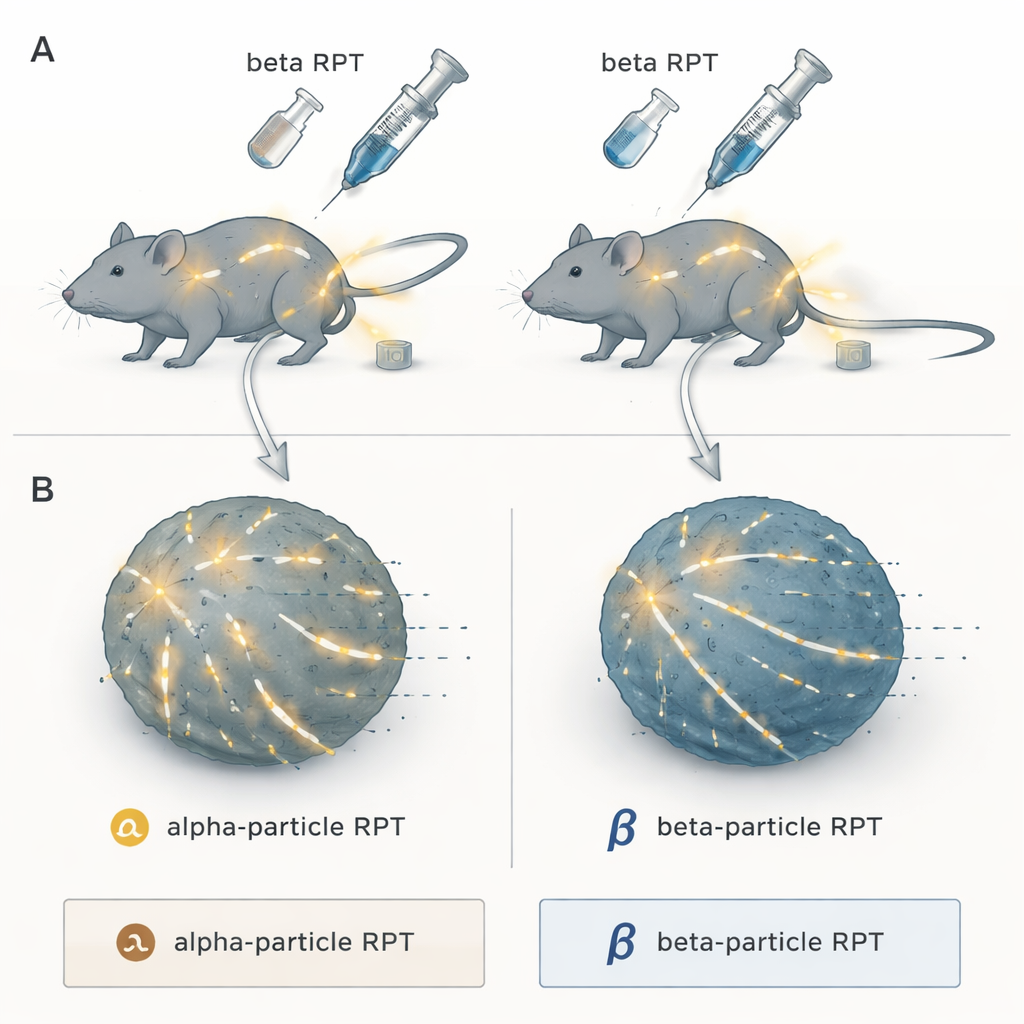
Two Flavors of Precision Radiation
Naukowcy skupili się na terapii radiofarmaceutycznej — podejściu „szukaj i niszcz”, w którym ładunek radioaktywny jest przytwierdzony do cząsteczki naturalnie trafiającej do guzów. Po wstrzyknięciu krąży ona po organizmie i dostarcza promieniowanie do złogów nowotworowych, gdziekolwiek się ukrywają — coś, czego zwykła radioterapia zewnętrzna nie potrafi łatwo zrobić przy chorobie rozsianej. Zespół porównał dwie główne kategorie: emitery cząstek alfa, które uwalniają niezwykle gęste porcje energii na bardzo krótkim dystansie, oraz emitery cząstek beta, które wysyłają promieniowanie o niższej gęstości rozchodzące się dalej w tkance. Wszystkie były związane z tym samym związkiem tropiącym guz, NM600, tak by różnił się jedynie rodzaj promieniowania — nie celowanie.
Pairing Radiation with Immune Checkpoint Blockers
Sama w sobie terapia inhibitorami punktów kontrolnych, takimi jak przeciwciała przeciw PD-L1 i CTLA4, może poluzować hamulce nakładane na komórki odpornościowe, ale działa najlepiej, gdy guz jest już widoczny dla układu odpornościowego. W modelach mysich czerniaka, raka prostaty i raka jelita grubego naukowcy zastosowali starannie dobraną niską dawkę NM600 emitującego albo cząstki alfa, albo beta, z dodatkiem lub bez kombinacji inhibitorów punktów kontrolnych. Różnicowali też moment podania leków immunologicznych — przed, krótko po lub znacznie po terapii radioaktywnej — aby sprawdzić, jak czasowanie wpływa na wyniki, takie jak wzrost guza, przeżycie i długotrwała pamięć immunologiczna.
When Beta Radiation Shines: Boosting an Existing Response
W „immunologicznie gorącym” modelu raka jelita grubego, który już reaguje na immunoterapię, najlepsze efekty osiągnięto przy użyciu NM600 emitującego beta, szczególnie gdy leki immunologiczne rozpoczęto wcześnie lub w terminie pośrednim. Guzy kurczyły się bardziej, myszy żyły dłużej, a wyleczone osobniki często odrzucały ten sam nowotwór, gdy wprowadzono go ponownie po kilku miesiącach. Szczegółowe profilowanie odporności wykazało, że terapia oparta na beta plus blokada punktów kontrolnych nie tyle tworzyła nową odpowiedź, ile wzmacniała istniejącą: istniejące antygenowo‑swoiste komórki T cytotoksyczne się rozszerzały, ulegały większej aktywacji i wytwarzały więcej sygnałów ataku. Krótko mówiąc, emitery beta świetnie nadawały się do propagowania trwającej odpowiedzi immunologicznej.
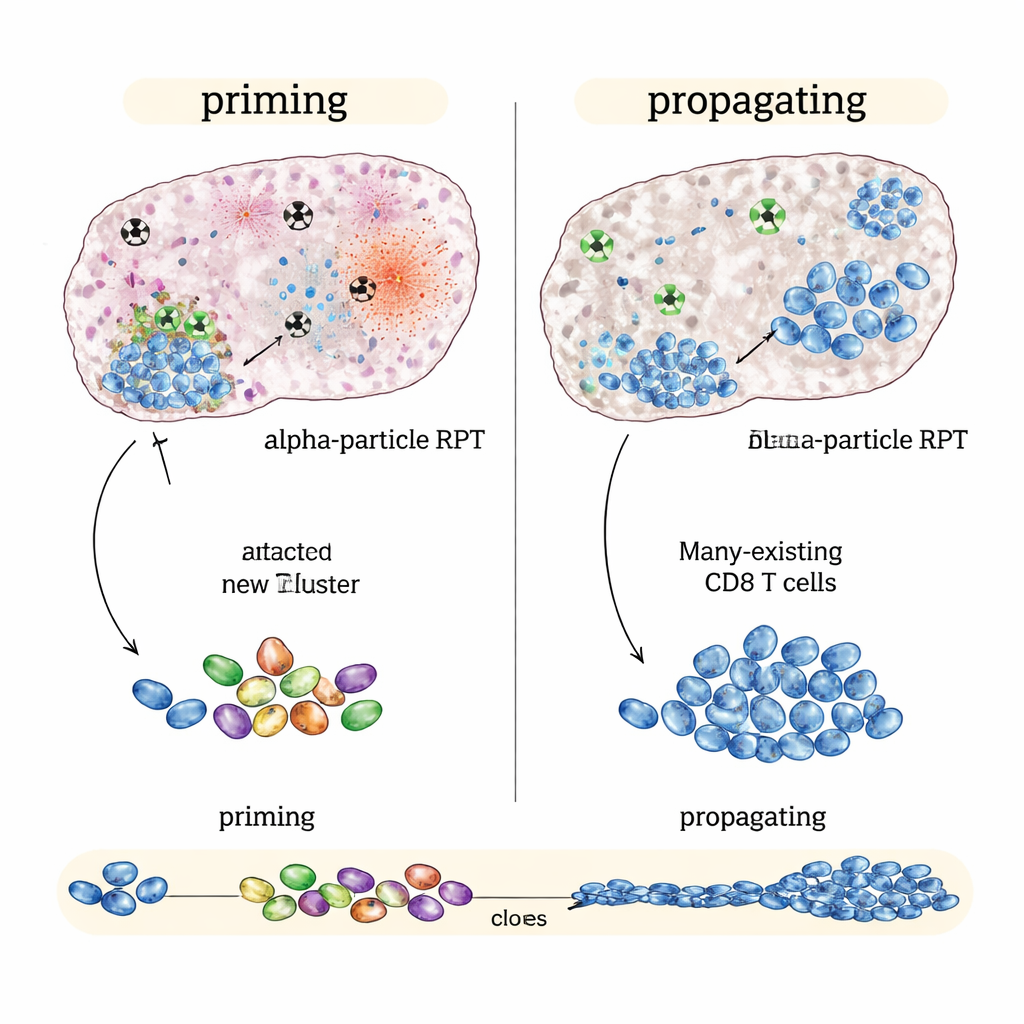
When Alpha Radiation Shines: Sparking New Immune Attack
Przeciwnie, w „immunologicznie zimnych” guzach, takich jak model czerniaka i rak prostaty słabo reagujące na same inhibitory punktów kontrolnych, wersja emitująca alfa działała lepiej niż emitery beta przy tej samej średniej dawce w guzie. Terapia oparta na alfa wraz z lekami immunologicznymi silniej spowalniała wzrost guza i dodatkowo wydłużała przeżycie. Analizy genetyczne na poziomie pojedynczych komórek sugerowały, dlaczego: promieniowanie alfa powodowało intensywne, zlokalizowane uszkodzenia, które zdawały się generować silne sygnały alarmowe w obrębie guza przy jednoczesnym oszczędzaniu pobliskich struktur immunologicznych. Ten wzorzec wiązał się z szerszym, bardziej zróżnicowanym repertuarem odpowiedzi komórek T i oznakami, że powstają nowe komórki T rozpoznające guz, które łączą się z długotrwałymi komórkami pamięci — dowód na „priming” układu odpornościowego, a nie jedynie jego wzmocnienie.
Why the Type and Timing of Radiation Matter
We wszystkich modelach wcześniejsze lub pośrednie podanie inhibitorów punktów kontrolnych — mniej więcej zbieżne z momentem, gdy sygnały zagrożenia wywołane promieniowaniem osiągają szczyt — konsekwentnie przewyższało opóźnione leczenie. Praca sugeruje praktyczną zasadę: w nowotworach już widocznych dla układu odpornościowego niskodawkowe radiofarmaceutyki oparte na beta mogą być idealnymi partnerami dla inhibitorów punktów kontrolnych, ponieważ propagują i wzmacniają istniejącą odporność. W bardziej opornych immunologicznie nowotworach emitery alfa o dużym wpływie mogą być lepsze do inicjowania nowych odpowiedzi komórek T i przekształcania „zimnego” guza w „gorący”. Dla pacjentów oznacza to, że nie wszystkie radioaktywne leki są wymienne; dopasowanie izotopu i harmonogramu do immunologicznej osobowości guza może uczynić terapię łączoną radio‑immunologiczną zarówno skuteczniejszą, jak i trwalszą.
Cytowanie: Kerr, C.P., Jin, W.J., Liu, P. et al. Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice. Nat Commun 17, 2044 (2026). https://doi.org/10.1038/s41467-026-68834-1
Słowa kluczowe: terapia radiofarmaceutyczna, promieniowanie alfa kontra beta, inhibitory punktów kontrolnych układu odpornościowego, immunoterapia nowotworów, mikrośrodowisko guza