Clear Sky Science · pl
Bezpieczeństwo i aktywność biologiczna bispecyficznego receptora T rozpoznającego Gag HIV u mężczyzn żyjących z HIV: pierwsze badanie u ludzi
Dlaczego to nowe badanie nad HIV ma znaczenie
Osoby żyjące z HIV dziś mogą oczekiwać niemal normalnej długości życia dzięki nowoczesnym koktajlom leków. Leki te, zwane terapią antyretrowirusową (ART), nie usuwają jednak wirusa; jedynie go kontrolują. Ukryte skupiska HIV pozostają w organizmie i mogą ponownie wywołać zakażenie, jeśli leczenie zostanie przerwane. To badanie testuje nowy rodzaj precyzyjnej immunoterapii — zbudowanej z laboratoryjnie zaprojektowanego receptora T — która ma za zadanie w bezpieczny sposób wyszkolić układ odpornościowy do namierzania tych kryjówek u osób już dobrze kontrolowanych na ART.
Ukryty wirus, który nie znika
Nawet gdy badania krwi wykazują „niewykrywalny” wirus, HIV utrzymuje się jako materiał genetyczny schowany wewnątrz długowiecznych komórek, głównie typu białych krwinek zwanych komórkami CD4. Te komórki-rezerwuar niosą cichy, lecz nienaruszony wirus, który może się na nowo uaktywnić, zmuszając osoby do przyjmowania codziennych tabletek przez całe życie. Całkowite wyeliminowanie każdej zakażonej komórki jest niezwykle trudne i udało się tylko u nielicznych osób po ryzykownych przeszczepach szpiku kostnego z powodu raka. Wiele zespołów badawczych dąży więc zamiast tego do „funkcjonalnego wyleczenia”: zmniejszenia rezerwuaru na tyle, by własne mechanizmy obronne organizmu potrafiły utrzymać HIV pod kontrolą bez stałej terapii.
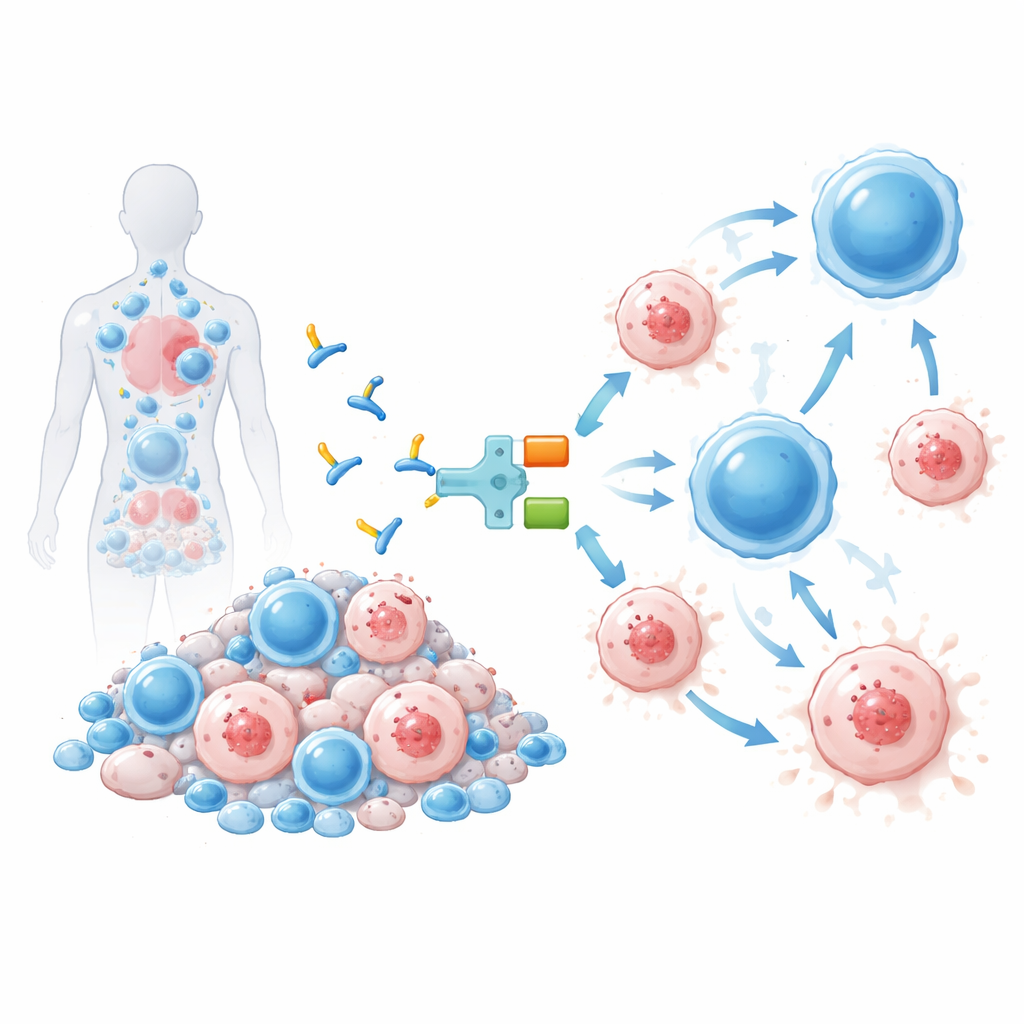
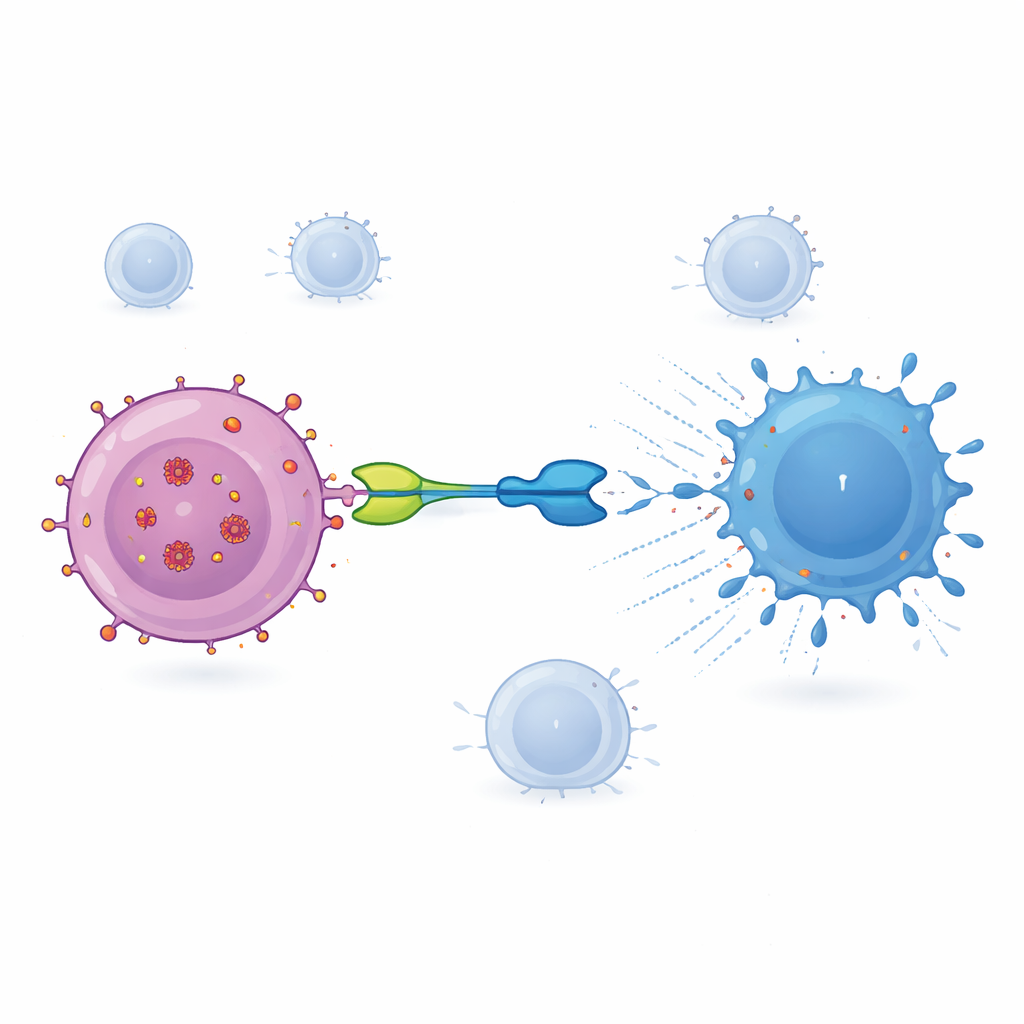
Zaprojketowana cząsteczka przekierowująca komórki T
Terapia badana w tym badaniu, nazwana IMC‑M113V, to niewielkie białko działające jak molekularny łącznik między zakażonymi komórkami a układem odpornościowym. Jeden koniec IMC‑M113V to inżynierowany receptor T komórki rozpoznający mały fragment HIV pochodzący z białka Gag, prezentowany na powierzchni zakażonych komórek w kontekście powszechnego markera immunologicznego (HLA‑A*02:01). Drugi koniec wiąże się z CD3, strukturą obecna na wszystkich komórkach T. Gdy IMC‑M113V jednocześnie połączy obie strony, zbliża zwykłe komórki T do komórki zakażonej HIV i inicjuje ich zabicie. W testach laboratoryjnych ta cząsteczka wykazywała dużą czułość, wykrywając zaledwie kilka kopii fragmentu wirusowego na powierzchni komórki i skutecznie eliminując komórki zakażone kilkoma powszechnymi wariantami HIV, nie powodując jednocześnie istotnej aktywacji wobec panelu zdrowych ludzkich komórek.
Pierwszy test u osób żyjących z HIV
Aby sprawdzić, czy podejście to jest bezpieczne u ludzi, badacze przeprowadzili wczesnofazowe badanie u dwunastu dorosłych mężczyzn żyjących z HIV w Wielkiej Brytanii, Belgii i Hiszpanii. Wszyscy uczestnicy mieli dobrze kontrolowane zakażenie na ART, wysokie liczby CD4 i posiadali wymagany typ HLA. Każda osoba otrzymała jednorazową dawkę dożylną IMC‑M113V na jednym z trzech niskich poziomów dawki, a następnie była uważnie monitorowana przez miesiąc. Głównym celem na tym etapie było bezpieczeństwo: poszukiwanie działań niepożądanych, takich jak gorączka, ciężkie zapalenie czy problemy neurologiczne, które mogą występować przy innych silnych lekach angażujących komórki T stosowanych w leczeniu raka.
Co badacze zaobserwowali w klinice
Wszystkie dawki IMC‑M113V były ogólnie dobrze tolerowane. Połowa uczestników zgłosiła pewne działania niepożądane, głównie łagodne dolegliwości, takie jak zmęczenie lub podrażnienie skóry, i nikt nie rozwinął poważnych problemów, takich jak zespół uwalniania cytokin czy neurotoksyczność. Badania krwi wykazały, że stężenia leku wzrastały i spadały w ciągu około doby, z okresem półtrwania około 15–22 godzin. Przy najwyższej dawce (15 mikrogramów) kilku uczestników wykazało przejściowe wzrosty molekuł zapalnych, zwłaszcza interleukiny‑6, oraz oznaki aktywacji ich komórek T i większej zdolności do produkcji białek zabijających komórki. Te zmiany immunologiczne były najsilniejsze u ochotników, których wirusy miały warianty Gag, do których IMC‑M113V wiąże się szczególnie mocno, co sugeruje, że lek angażował zamierzone cele w organizmie. Jednak po pojedynczej dawce nie zaobserwowano mierzalnego zmniejszenia rozmiaru rezerwuaru HIV we krwi, ocenianego na podstawie RNA wirusa i nienaruszonego DNA wirusowego w komórkach CD4.
Co to oznacza dla przyszłego leczenia HIV
Dla czytelnika niebędącego specjalistą główny przekaz jest taki, że badanie dostarcza ważnego pierwszego dowodu koncepcji: wysoce ukierunkowana immunologiczna „cząsteczka‑most” może być podana bezpiecznie osobom z dobrze kontrolowanym HIV i może pobudzić ich komórki T do rozpoznawania komórek noszących wirusa. Nie wyleczyło to HIV ani nie pozwoliło zaprzestać ART, ale nie było to celem tego pierwszego badania u ludzi. Wyniki wspierają testowanie wyższych i powtarzanych dawek, możliwe łączenie z lekami, które skłaniają więcej zakażonych komórek do ujawnienia się, oraz rozszerzenie podejścia na inne typy układu odpornościowego poza HLA‑A*02:01. Jeśli przyszłe badania potwierdzą, że strategia ta może niezawodnie zmniejszać rezerwuar wirusa bez niebezpiecznych skutków ubocznych, mogłaby stać się kluczową częścią terapii skojarzonych ukierunkowanych na długotrwałą, pozbawioną leków kontrolę HIV.
Cytowanie: Vandekerckhove, L., Fox, J., Mora-Peris, B. et al. Safety and biologic activity of a bispecific T cell receptor targeting HIV Gag in males living with HIV: a first-in-human trial. Nat Commun 17, 2207 (2026). https://doi.org/10.1038/s41467-026-68833-2
Słowa kluczowe: Leczenie HIV, terapia komórkowa T, rezerwuar wirusa, receptor bispecyficzny, badanie kliniczne