Clear Sky Science · pl
Mechanistyczne wglądy w rozwijanie wybranych struktur i-motywu DNA napędzane przez PCBP1 na punkcie kontrolnym G1/S
Fałdy DNA działające jak sygnalizacja świetlna
W naszych komórkach kod genetyczny to coś więcej niż prosta, równoległa drabina DNA. Niektóre jego fragmenty mogą składać się w nietypowe kształty, które działają jak maleńkie przełączniki i pomagają kontrolować momenty kopiowania DNA oraz podziału komórek. W tym badaniu skupiono się na jednym z takich kształtów, zwanym i-motywem, oraz na białku PCBP1, które potrafi rozpoznawać i rozwijać te struktury w chwili, gdy komórka przygotowuje się do replikacji DNA. Zrozumienie tej interakcji rzuca światło na to, jak komórki utrzymują stabilność genomu i co może pójść nie tak w nowotworach.
Dziwne supły DNA w regionach powiązanych z rakiem
Większość osób uczy się, że DNA tworzy słynną podwójną helisę, ale niektóre odcinki bogate w literę C (cytozynę) mogą układać się w czterostrunowy supły znany jako i-motyw. Struktury te mają tendencję do pojawiania się w regionach kontrolnych genów napędzających wzrost komórek, takich jak cMYC i BCL2. Przez lata naukowcy dyskutowali, czy i-motywy rzeczywiście powstają w żywych komórkach, ponieważ łatwiej je wykryć w kwaśnych warunkach probówki niż w niemal obojętnych warunkach wewnątrz organizmu. Dzięki specjalistycznym przeciwciałom rozpoznającym i-motywy, ostatnie prace, łącznie z niniejszym badaniem, potwierdziły, że pojawiają się one w jądrach komórkowych — i często skupiają się w pobliżu kluczowych genów wzrostu i związanych z nowotworami.
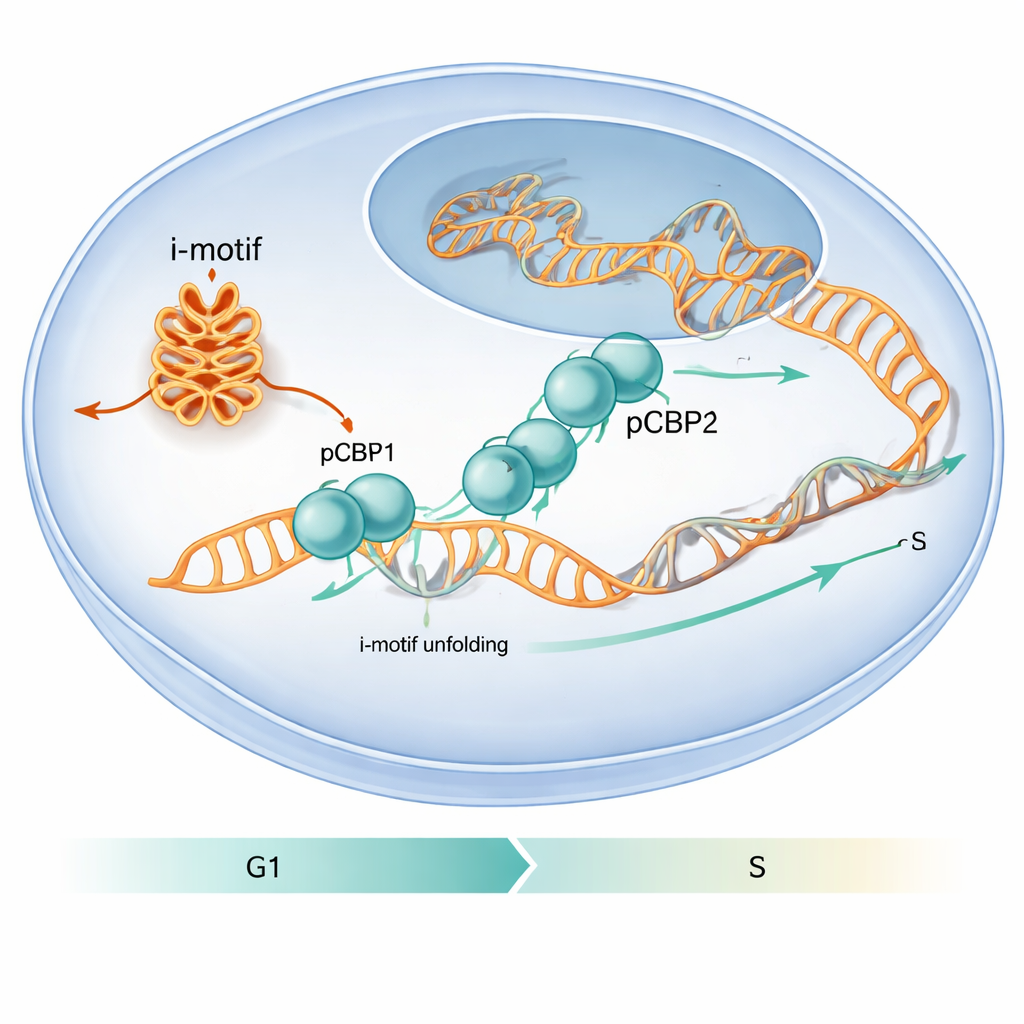
Białko, które wybiera specjalne fałdy DNA
Autorzy postanowili odkryć, jak białka w komórce radzą sobie z tymi nietypowymi fałdami DNA. Skoncentrowali się na PCBP1 — białku znanym z wiązania fragmentów bogatych w C w DNA i RNA oraz z wpływu na cykl komórkowy. Analizując dostępne mapy wiązania w skali genomu i wykonując ukierunkowane eksperymenty, odkryli, że PCBP1 często znajduje się na regionach bogatych w C, które mogą tworzyć i-motywy, szczególnie wokół miejsc startu genów. W eksperymentach komórkowych na ludzkich liniach komórkowych nowotworów, fragmenty promotorów cMYC, BCL2 i powiązanego z insuliną sekwencji ILPR wykazywały zarówno silne sygnały i-motywów, jak i wysokie zajęcie przez PCBP1, co sugeruje, że PCBP1 jest dedykowanym opiekunem tych struktur.
Jak PCBP1 chwyta i rozwija supły
W testach in vitro badacze porównali, jak dobrze PCBP1 wiąże złożone i-motywy w porównaniu z tymi samymi sekwencjami DNA w formie niezłożonej. Regulowali kwasowość, tak aby DNA albo pozostawało złożone, albo się odprężało, przy jednoczesnym zachowaniu stabilności białka. PCBP1 zawsze preferował złożony i-motyw, wiążąc go mniej więcej dwa razy silniej niż tę samą sekwencję w stanie niezłożonym i tylko słabo do niepowiązanych kształtów DNA. Po związaniu PCBP1 mógł aktywnie wspierać rozwijanie, pozwalając nici i-motywu na sparowanie z komplementarnym partnerem. Jednak nie wszystkie i-motywy zachowywały się tak samo: niektóre, jak struktura w promotorze cMYC, rozwijały się szybko, podczas gdy inne, jak te w BCL2, opierały się i rozwijały jedynie powoli. Dodatkowe cechy, takie jak pętle typu hairpin w DNA oraz stopień protonacji cytozyn (obciążenie dodatnim ładunkiem), mogły albo wspierać, albo utrudniać aktywność rozwijającą PCBP1.
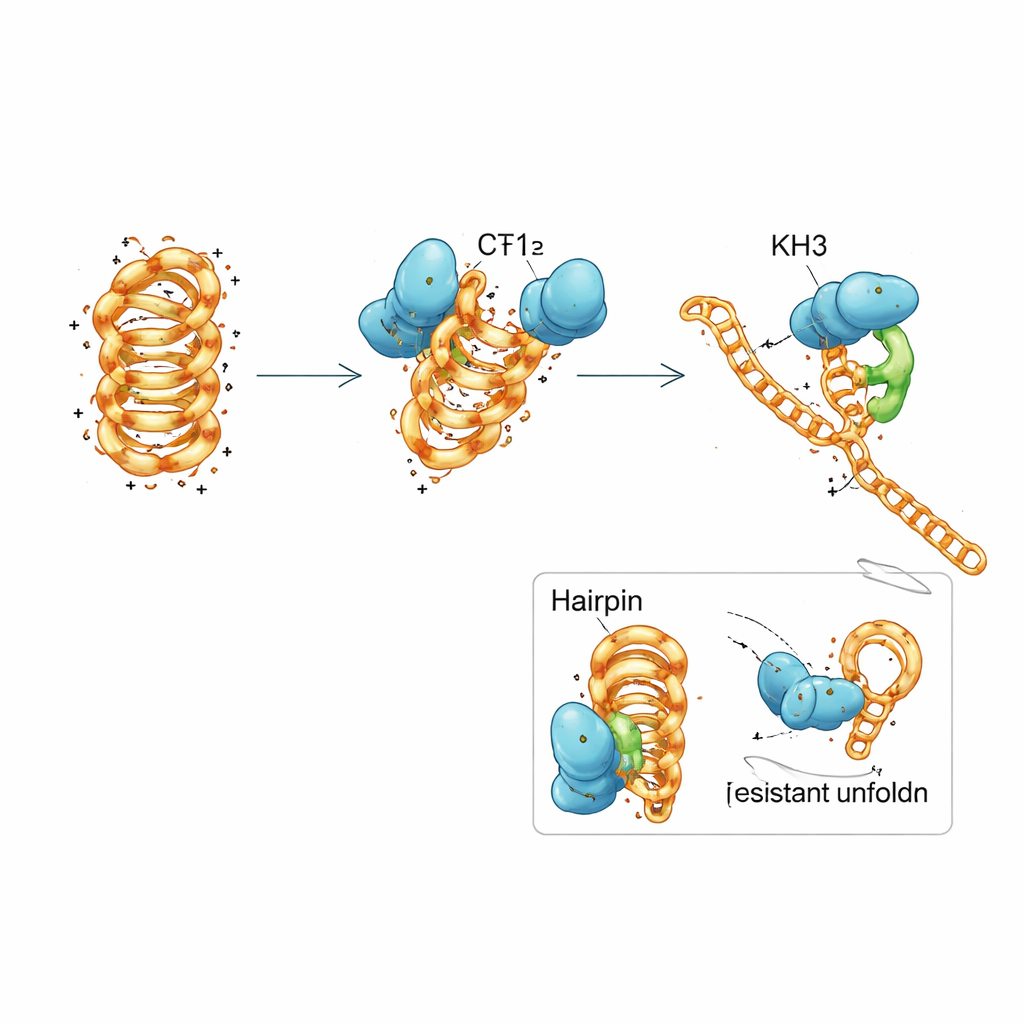
Wysiłek zespołowy w obrębie pojedynczego białka
PCBP1 zbudowany jest z trzech powtarzalnych modułów zwanych domenami KH — typowych motywów chwytających krótkie odcinki kwasów nukleinowych. Zespół rozłożył PCBP1 na części i odkrył, że żadna pojedyncza domena KH nie potrafi w pełni naśladować zachowania całego białka. Dwie pierwsze domeny razem potrafiły przyczepiać się zarówno do złożonego, jak i niezłożonego DNA i przesuwać i-motyw w kierunku mniej stabilnej formy, ale jedynie powoli sprzyjały pełnemu rozwinięciu. Trzecia domena sama niemal wcale nie wiązała. Gdy wszystkie trzy domeny były obecne i mogły współdziałać, białko odzyskiwało silne preferencje dla złożonych i-motywów oraz efektywną zdolność do ich rozwijania. Szczegółowe pomiary biofizyczne i symulacje komputerowe zasugerowały mechanizm krokowy: KH1 i KH2 najpierw dokują do elastycznych pętli i-motywu i częściowo zaburzają wybrane pary zasad, co następnie pozwala KH3 zaangażować się i popchnąć strukturę w stan otwarty, gotowy do replikacji.
Utrzymywanie rytmu cyklu komórkowego
Prace pokazują również, że ten molekularny taniec ma znaczenie dla zachowania komórkowego. Gdy badacze obniżyli poziomy PCBP1 w komórkach ludzkich, w określonych promotorach genów pojawiło się więcej struktur i-motywu, zwiększyły się markery uszkodzeń DNA, a komórki zablokowały się na krytycznym punkcie kontrolnym G1/S — chwilę tuż przed rozpoczęciem replikacji DNA. W normalnych warunkach obecność PCBP1 w regionach tworzących i-motywy osiąga szczyt wokół tego punktu kontrolnego, a następnie spada wraz z początkiem fazy S, gdy i-motywy ulegają rozwiązaniu. To czasowanie sugeruje, że PCBP1 działa jako opiekun: wiąże i rozwija konkretne i-motywy dokładnie w odpowiednim momencie, aby replikacja DNA mogła przebiegać płynnie, a genom został zachowany w integralności. Dla czytelnika nietechnicznego przekaz jest taki, że nietypowe fałdy DNA mogą funkcjonować jak tymczasowe blokady na drodze, a PCBP1 jest jednym ze specjalistycznych narzędzi, których komórka używa do ich usuwania, pomagając zapobiegać błędom, które inaczej mogłyby przyczynić się do rozwoju raka.
Cytowanie: Sengupta, P., Gillet, N., Obi, I. et al. Mechanistic insights into PCBP1-driven unfolding of selected i-motif DNA at G1/S checkpoint. Nat Commun 17, 1149 (2026). https://doi.org/10.1038/s41467-026-68822-5
Słowa kluczowe: DNA i-motyw, białko PCBP1, punkt kontrolny cyklu komórkowego, stabilność genomu, struktura wtórna DNA