Clear Sky Science · pl
Baza danych nanocząsteczek lipidowych wspierająca modelowanie struktura‑funkcja i projektowanie napędzane danymi dla dostarczania kwasów nukleinowych
Dlaczego małe pęcherzyki tłuszczu mają znaczenie dla przyszłych leków
Nanocząsteczki lipidowe to mikroskopijne, oparte na tłuszczach pęcherzyki, które bezpiecznie przenoszą instrukcje genetyczne — na przykład szczepionkowe mRNA — do naszych komórek. Przyczyniły się do skuteczności szczepionek przeciw COVID‑19, jednak badacze wciąż nie rozumieją w pełni, w jaki sposób ich szczegółowy skład chemiczny wpływa na skuteczność. Ten artykuł opisuje nowe zasoby online, Bazę Danych Nanocząsteczek Lipidowych (LNPDB), stworzone, by zgromadzić rozproszone dane w jednym miejscu, umożliwiając naukowcom systematyczne projektowanie lepszych i bezpieczniejszych leków dostarczających materiał genetyczny.
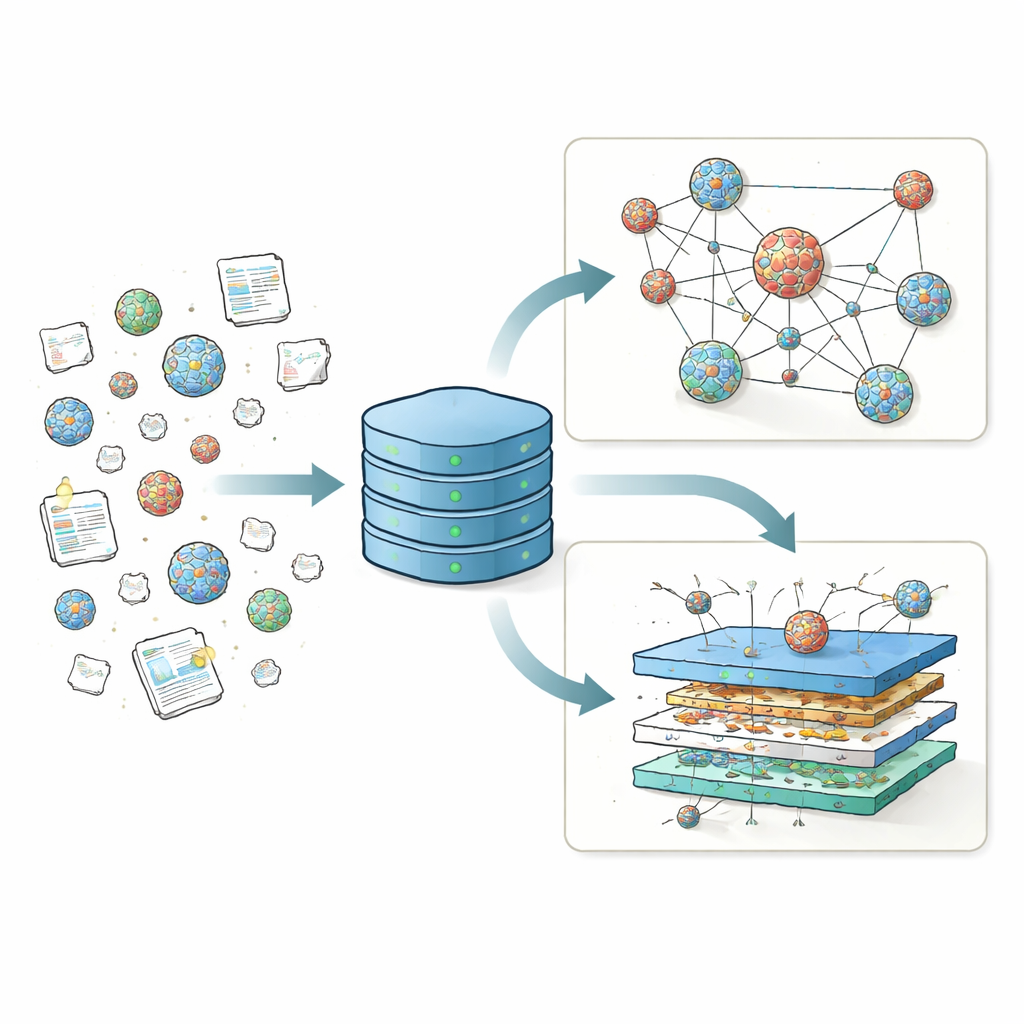
Zgromadzenie rozproszonych wyników w jednym miejscu
Przez lata różne laboratoria testowały tysiące receptur nanocząsteczek lipidowych (LNP), zmieniając główny lipid naładowany, lipidy pomocnicze, cholesterol i lipidy pokrywające, aby sprawdzić, które kombinacje najskuteczniej dostarczają materiał genetyczny. Wyniki te były jednak raportowane w wielu formatach i w dziesiątkach publikacji, co utrudniało porównywanie badań i dostrzeganie ogólnych trendów. W przeciwieństwie do nauki o białkach, która opiera się na centralnym Protein Data Bank napędzającym narzędzia takie jak AlphaFold, dziedzina LNP nie miała zunifikowanego repozytorium danych o strukturze i wydajności. LNPDB wypełnia tę lukę, zbierając szczegółowe informacje o 19 528 formulacjach LNP pochodzących z 42 badań i od jednego dostawcy komercyjnego oraz standaryzując sposób zapisu składników, warunków testów i wyników każdej cząsteczki.
Co zawiera nowa baza danych
Każdy wpis LNP w LNPDB opisany jest wzdłuż trzech głównych osi: skład, eksperyment i symulacja. Pola opisujące skład rejestrują, które lipidy użyto, ile atomów azotu zawiera główny lipid naładowany oraz dokładne proporcje mieszania czterech podstawowych składników: lipidu jonizowalnego, lipidu pomocniczego, cholesterolu i lipidu z polietylenoglikolem (PEG). Pola eksperymentalne obejmują rodzaj dostarczonego ładunku genetycznego — najczęściej mRNA kodujące białko raportujące — miejsce podania (na przykład komórki w hodowli, wątroba, płuca lub mięsień), sposób przygotowania cząstek i miary sukcesu. Wreszcie, pola symulacyjne dostarczają gotowe pliki opisujące fizyczne zachowanie każdego lipidu w wystarczającym szczególe, by uruchomić symulacje komputerowe na poziomie atomowym membran lipidowych. Razem te ustandaryzowane opisy przekształcają zbiór pojedynczych badań w spójny krajobraz, który społeczność może przeszukiwać, filtrować i rozszerzać.
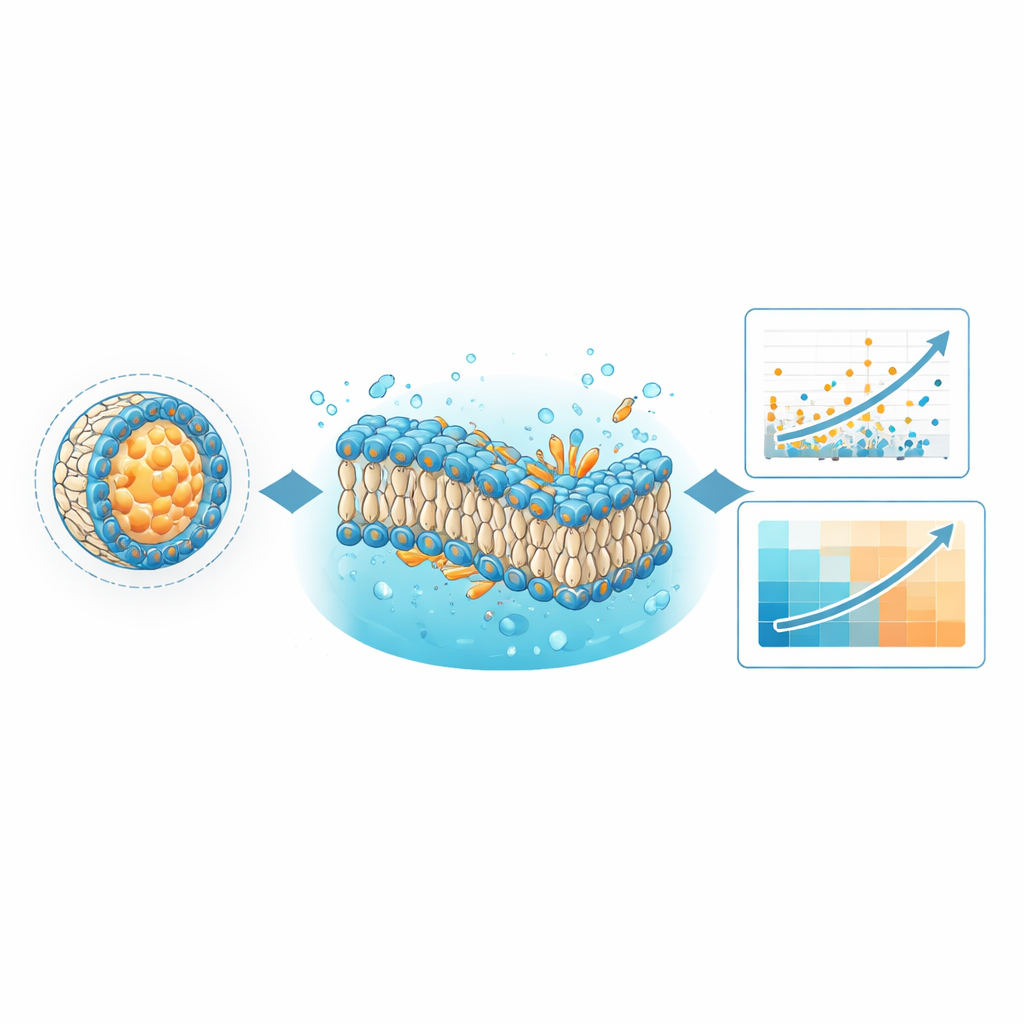
Nauczanie komputerów rozpoznawania lepszych receptur dostarczania
Jednym z natychmiastowych zastosowań LNPDB jest ulepszenie modeli uczenia maszynowego przewidujących, które formulacje najskuteczniej dostarczą materiał genetyczny. Autorzy ponownie wytrenowali swój istniejący model głębokiego uczenia o nazwie LiON, używając rozszerzonego zbioru LNPDB, co więcej niż podwoiło liczbę przykładów, które model wcześniej widział. LiON uczy się wzorców łączących struktury chemiczne lipidów jonizowalnych, skład komponentów pomocniczych i kontekst testowy z wydajnością każdej formulacji. Dzięki bogatszym danym prognozy LiON lepiej zgadzały się z wynikami eksperymentalnymi dla większości zestawów testowych i przewyższały konkurencyjny model AGILE w kilku niezależnych zbiorach. Wskazuje to, że szeroki, różnorodny i stale rosnący zbiór treningowy jest kluczowy dla tworzenia uniwersalnych narzędzi projektowych dla przyszłych leków LNP.
Obserwowanie modelowych membran w poszukiwaniu ukrytych zasad
Baza danych została również zaprojektowana do innego rodzaju obliczeń: symulacji fizyki opartych na dynamice molekularnej. Korzystając z plików symulacyjnych dołączonych do LNPDB, zespół zbudował uproszczone membrany reprezentujące wybrane formulacje LNP i obserwował ich zachowanie przez mikrosekundy symulowanego czasu. Zadali sobie dwa pytania: czy modelowane dwuwarstwy lipidowe pozostają nienaruszone i jaki ogólny kształt przyjmują kluczowe lipidy w membranie? Symulacje wykazały, że formulacje, których membrany pozostawały stabilne, były częściej skuteczne w eksperymentach. Ponadto zmierzono cechę nazwaną „krytycznym parametrem upakowania”, odzwierciedlającą, czy lipid ma kształt bardziej stożkowy czy odwróconego stożka w membranie. W kilku testowanych bibliotekach lipidy o kształtach sprzyjających ujemnej krzywiźnie — przypisywanej ułatwianiu fuzji i zakłócania błon endosomalnych — wykazywały silniejsze dostarczanie, czasem korelując z wydajnością lepiej niż sam model głębokiego uczenia.
Nowa podstawa dla inteligentniejszej nanomedycyny
Dla osoby niebędącej specjalistą główne przesłanie jest takie, że praca ta tworzy wspólną, rosnącą "mapę" tego, jak składniki i struktura małych pęcherzyków tłuszczu wiążą się z ich zdolnością do dostarczania terapii genetycznych. Poprzez zgromadzenie dziesiątek tysięcy wcześniejszych eksperymentów, umożliwienie potężnych modeli predykcyjnych i dostarczenie narzędzi do symulacji zachowania cząstek na poziomie molekularnym, LNPDB kładzie fundamenty pod bardziej racjonalne projektowanie zamiast metod prób i błędów. Z czasem takie podejście oparte na danych może przyspieszyć tworzenie skuteczniejszych szczepionek, terapii edycji genów i innych terapii opartych na kwasach nukleinowych, jednocześnie pomagając badaczom zrozumieć, dlaczego niektóre receptury nanocząsteczek działają — a inne nie.
Cytowanie: Collins, E., Ji, J., Kim, SG. et al. Lipid Nanoparticle Database towards structure-function modeling and data-driven design for nucleic acid delivery. Nat Commun 17, 2464 (2026). https://doi.org/10.1038/s41467-026-68818-1
Słowa kluczowe: nanocząsteczki lipidowe, dostarczanie mRNA, nanomedycyna, uczenie maszynowe, dynamika molekularna