Clear Sky Science · pl
Chemicznie ukierunkowana transkryptomika pojedynczych komórek ujawnia przebudowę szkieletonu z udziałem sulfotransferaz w biosyntezie securininy
Dlaczego chemia krzewu ma znaczenie
Alkaloidy securinega to silnie działające związki występujące w niewielkim krzewie ozdobnym Flueggea suffruticosa, od dawna badane pod kątem potencjalnego zastosowania w leczeniu nowotworów i chorób neurologicznych. Do tej pory nikt jednak nie wiedział dokładnie, jak roślina konstruuje te złożone cząsteczki. W tym badaniu nowoczesne odczytywanie genów pojedynczych komórek połączono ze sprytnymi eksperymentami chemicznymi, aby krok po kroku odsłonić sposób, w jaki roślina składa i przekształca te związki — a przy okazji odkryć zaskakującą nową rolę powszechnego typu enzymu. 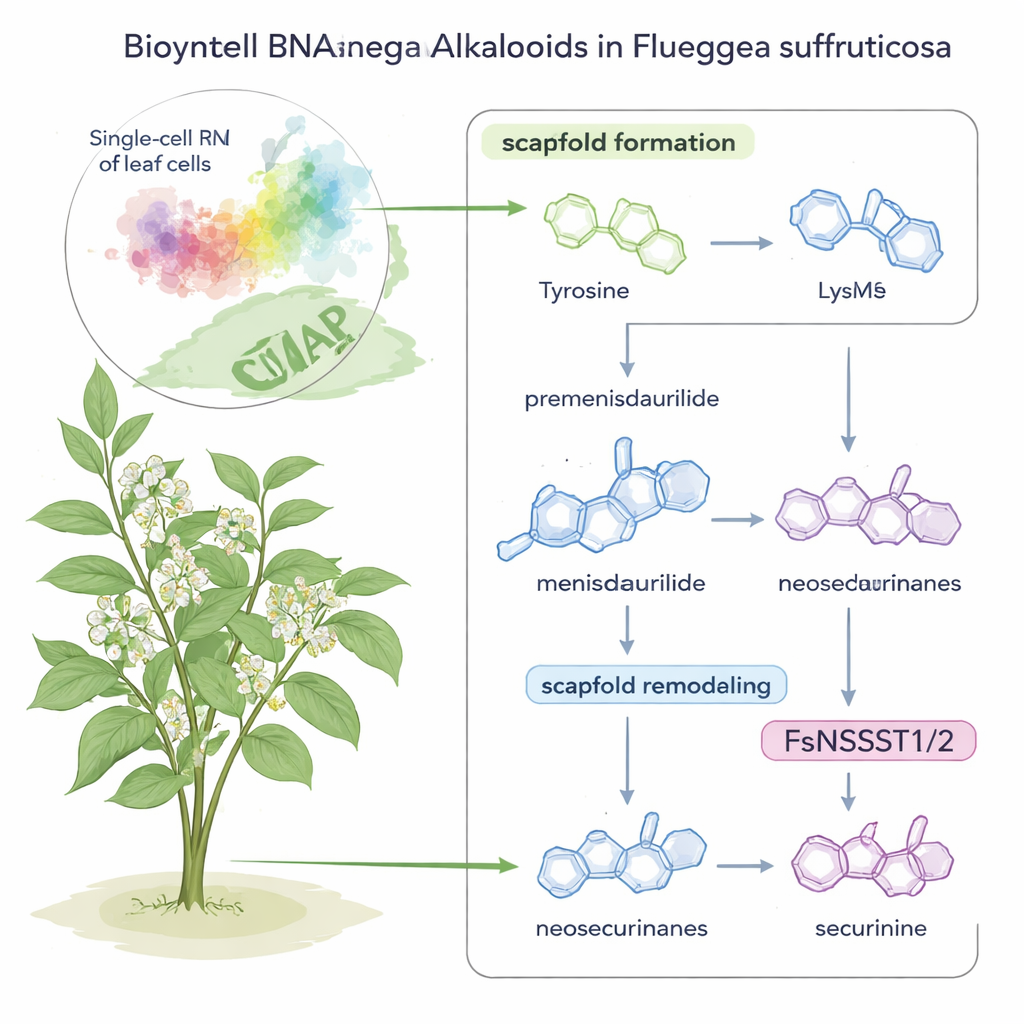
Składniki budulcowe z powszechnych aminokwasów
Historia zaczyna się od dwóch dobrze znanych składników odżywczych: aminokwasów tyrozyny i lizyny. W F. suffruticosa tyrozyna przekształcana jest w nietypową pierścieniową cząsteczkę zwaną premenisdaurylid, która następnie jest zredukowana do menisdaurylidu przez nowo odkryty enzym, który autorzy nazwali FsMS (od „menisdaurylid syntazy”). Równolegle lizyna przekształcana jest w mały, zawierający azot pierścień 1-piperideinę przez inny enzym, FsPS, odkryty w wcześniejszych pracach. Gdy menisdaurylid i 1-piperideina spotykają się w lekko zasadowych, wodnych warunkach, spontanicznie łączą się, tworząc alkaloidy „neosecurinane” — struktury pośrednie na drodze do końcowych związków o działaniu leczniczym.
Obserwowanie reakcji chemicznych w czasie rzeczywistym
Aby udowodnić, że proponowane etapy nie są jedynie teoretyczne, zespół syntetyzował wersje podejrzewanych pośredników znakowane ciężkimi atomami węgla. Podając te znakowane związki wyciągom z roślin, naukowcy mogli śledzić, gdzie dokładnie trafiają atomy. Zaobserwowali przekształcenie znakowanego menisdaurylidu w znakowane neosecurinany, a następnie w znane alkaloidy allosecurinina i securinina, potwierdzając, że te pośredniki rzeczywiście leżą na naturalnej ścieżce. Co istotne, niektóre z kluczowych reakcji powstawania pierścieni zachodziły nawet w przegotowanych wyciągach, pokazując, że część tej drogi może przebiegać bez udziału enzymów, napędzana po prostu chemią samych cząsteczek.
Zbliżenie się do właściwych komórek
Wiedza o tym, które cząsteczki pojawiają się gdzie, to tylko połowa zagadki; identyfikacja genów kontrolujących każdy krok wymaga poznania, które komórki wykonują tę pracę. Badacze zsekwencjonowali RNA z tysięcy pojedynczych komórek pobranych z liści F. suffruticosa, grupując je w odrębne typy komórek na podstawie wzorców aktywności genów. Jedna klasa komórek, związana z żyłkami liścia, wyróżniała się: silnie eksprymowała znane geny szlaku oraz wiele enzymów powiązanych z metabolizmem tyrozyny, lizyny i siarki. Analizując, które geny zmieniały się synchronicznie z enzymami szlaku w obrębie tej grupy, zespół wytypował FsMS oraz dwie sulfotransferazy, FsNSST1 i FsNSST2, jako głównych kandydatów na brakujące ogniwa.
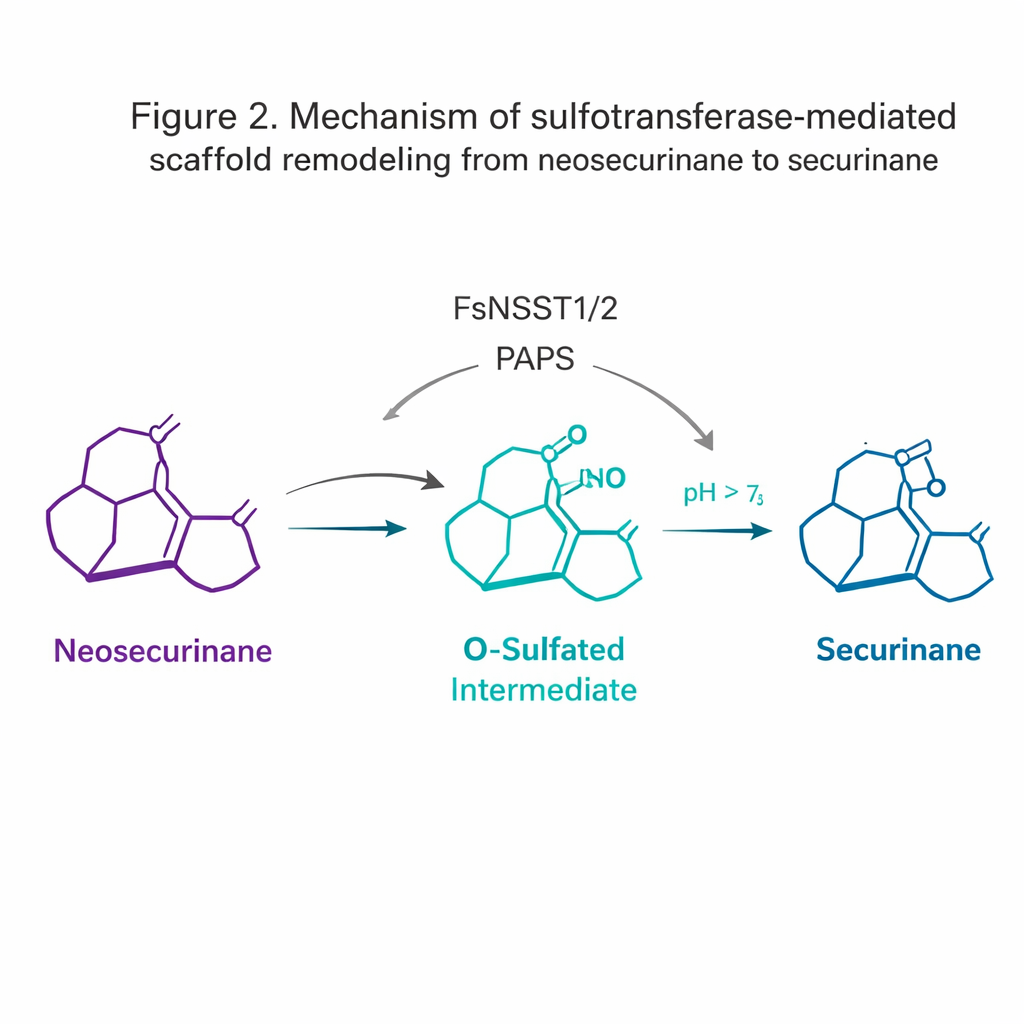
Enzym, który przebudowuje szkielet cząsteczki
Najbardziej zaskakujące odkrycie dotyczyło sulfotransferaz. Zwykle sulfotransferazy przyłączają grupę siarczanową do cząsteczek, poprawiając ich rozpuszczalność lub sygnalizując do rozkładu. Tutaj FsNSST1 i FsNSST2 zamiast tego działają jak wyłączniki: przyłączają siarczan do szkieletonu neosecurinany, tymczasowo przekształcając go w wysokoenergetyczny „O-siarczanowy” pośrednik. Ta aktywowana postać następnie ulega spontanicznemu przesunięciu 1,2-aminowemu — niewielkiej reorganizacji, w której atom azotu migruje — przekształcając [2.2.2] bicykliczny układ „neosecurinany” w [3.2.1] układ „securinany”. Ten subtelny krok przebudowy nadaje charakterystyczne czteropierścieniowe jądro biologicznie aktywnych alkaloidów.
Dlaczego ta ścieżka ma znaczenie
Dla laika kluczowy wniosek jest taki, że roślina wytwarza alkaloidy securinega w dwóch głównych fazach: najpierw buduje wstępny system pierścieni z pospolitych aminokwasów, a następnie chemicznie przebudowuje ten szkielet do bardziej złożonej formy za pomocą „spustu” w postaci siarczanu. Łącząc profilowanie genów komórka po komórce z chemią z użyciem izotopowo znakowanych związków, autorzy szczegółowo odwzorowują tę drogę i wykazują, że sulfotransferazy — enzymy obecne we wszystkich formach życia — mogą robić znacznie więcej niż tylko ozdabiać cząsteczki; potrafią inicjować całkowite przebudowy ich kształtu. Zrozumienie tej ścieżki nie tylko wyjaśnia, jak w naturze powstaje obiecująca klasa związków podobnych do leków, ale także otwiera drogę do inżynierii roślin lub mikroorganizmów w celu produkcji nowych leków inspirowanych securinegą.
Cytowanie: Choung, S., Kang, G., Kim, T. et al. Chemically guided single-cell transcriptomics reveals sulfotransferase-mediated scaffold remodeling in securinine biosynthesis. Nat Commun 17, 1954 (2026). https://doi.org/10.1038/s41467-026-68816-3
Słowa kluczowe: alkaloidy roślinne, biosynteza, transkryptomika pojedynczych komórek, sulfotransferaza, chemia produktów naturalnych