Clear Sky Science · pl
Metyloacja tRNA zależna od ALKB-1 jest niezbędna do efektywnej eliminacji mitochondriów pochodzenia ojcowskiego
Dlaczego mitochondria ojców cicho znikają
Każdy człowiek, robak i większość innych zwierząt dziedziczy swoje „elektrownie komórkowe” — mitochondria — niemal wyłącznie od matki. Mitochondria ojca dostają się do jaja wraz z plemnikiem, ale są szybko usuwane, co jest biologicznym sprzątaniem zapobiegającym przekazywaniu uszkodzonego DNA mitochondrialnego. Badanie przeprowadzone na małych nicieniach ujawnia molekularny „checkpoint stresu”, który pomaga zdecydować, czy mitochondria ojcowskie zostaną skutecznie oczyszczone, dając wskazówki, które w przyszłości mogą mieć znaczenie dla niektórych przypadków niepłodności i chorób mitochondrialnych.
Elektrownie, które dziedziczymy po mamie
Mitochondria wytwarzają energię utrzymującą komórki przy życiu i zawierają własną małą pętlę DNA. W ciągu życia to mitochondrialne DNA może gromadzić szkodliwe mutacje. Gdyby mitochondria obu rodziców były rutynowo przekazywane, te defekty mogłyby się mieszać i kumulować w kolejnych pokoleniach. Aby temu zapobiec, większość zwierząt polega na dziedziczeniu matczynym: zarodek zachowuje mitochondria matki, a niemal wszystkie mitochondria ojca są usuwane wkrótce po zapłodnieniu. Chociaż znane są różne mechanizmy usuwania — takie jak systemy recyklingu komórkowego czy enzymy tnące DNA — naukowcy nie rozumieli jeszcze w pełni, jak subtelne chemiczne znaki na DNA i RNA mogą wpływać na eliminację mitochondriów ojcowskich.
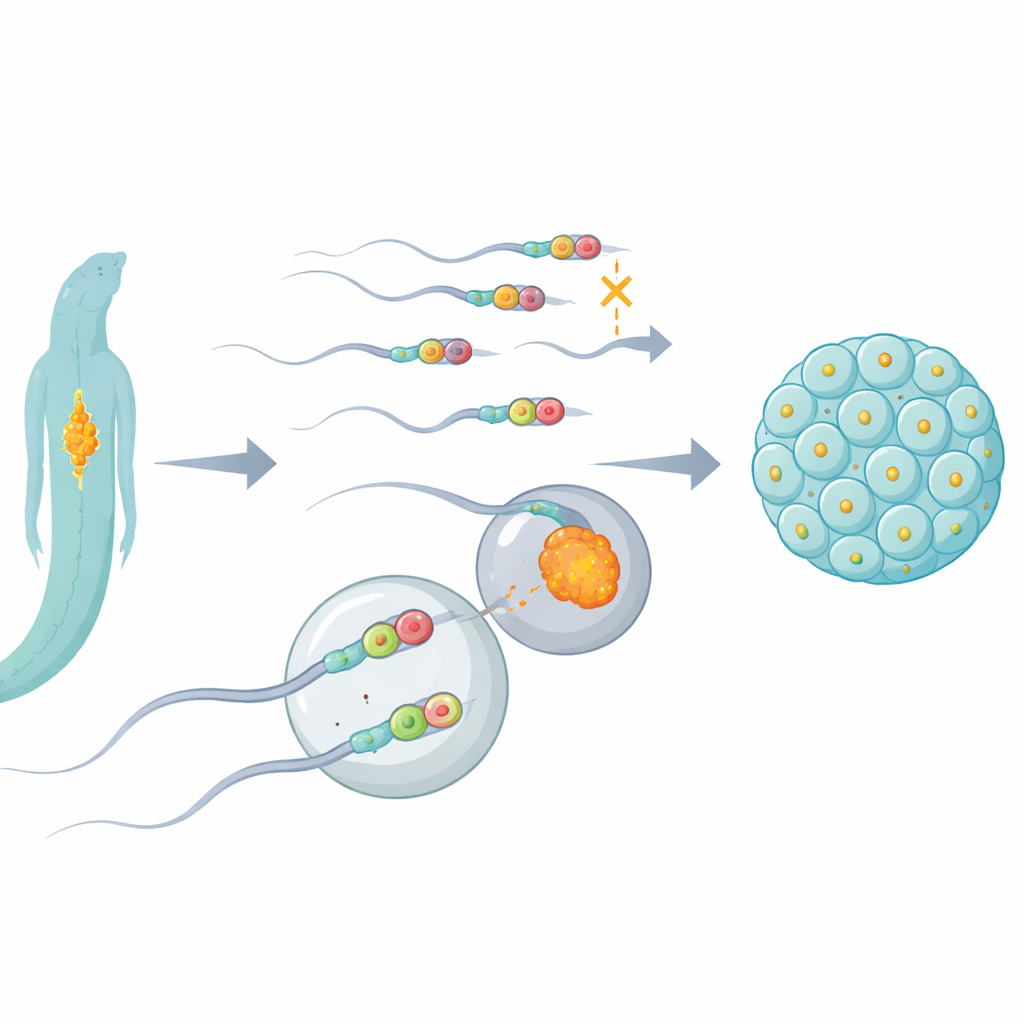
Molekularna gumka z kluczową funkcją rozrodczą
Naukowcy skupili się na białku o nazwie ALKB-1 u nicienia Caenorhabditis elegans, modelowego organizmu genetycznego. ALKB-1 działa jak molekularna gumka, usuwająca grupy metylowe — małe znaczniki chemiczne — z DNA i RNA. Poprzez selektywne wyłączenie ALKB-1 lub zmniejszenie jego poziomu zespół śledził, co dzieje się z mitochondriami plemników i ich DNA po zapłodnieniu. Stwierdzili, że gdy aktywność „gumki” ALKB-1 była utracona, mitochondria ojca i ich DNA utrzymywały się w rozwijających się zarodkach nietypowo długo, zamiast być szybko usunięte. Opóźnienie to występowało głównie, gdy ALKB-1 brakowało w plemnikach i współwystępowało z plemnikami zawierającymi wyjątkowo dużą liczbę mitochondriów i mitochondrialnego DNA.
Jak manipulacja chemią tRNA zaburza mitochondria
Zagłębiając się dalej, naukowcy zapytali, które chemiczne znaczniki są naprawdę istotne dla ALKB-1. Badania DNA sugerowały, że zmiany w metylacji DNA same w sobie nie wyjaśniają problemu z usuwaniem. Zamiast tego uwagę zwrócono na tRNA, małe adaptery pomagające przekształcać przekaz genetyczny w białka. U zdrowych robaków ALKB-1 usuwa specyficzny znacznik — zwany m1A — z podzbioru tRNA. Bez ALKB-1 te znaczniki się kumulowały. Ta subtelna zmiana w chemii tRNA szeroko zmieniała efektywność produkcji wielu białek: synteza białek w cytoplazmie wzrosła, podczas gdy produkcja białek wewnątrz mitochondriów osłabła. W efekcie powstała rozbieżność między białkami przeznaczonymi dla mitochondriów a tym, co organelle mogły obsłużyć, prowadząc do skupisk źle zarządzanych białek i sygnałów stresu mitochondrialnego.
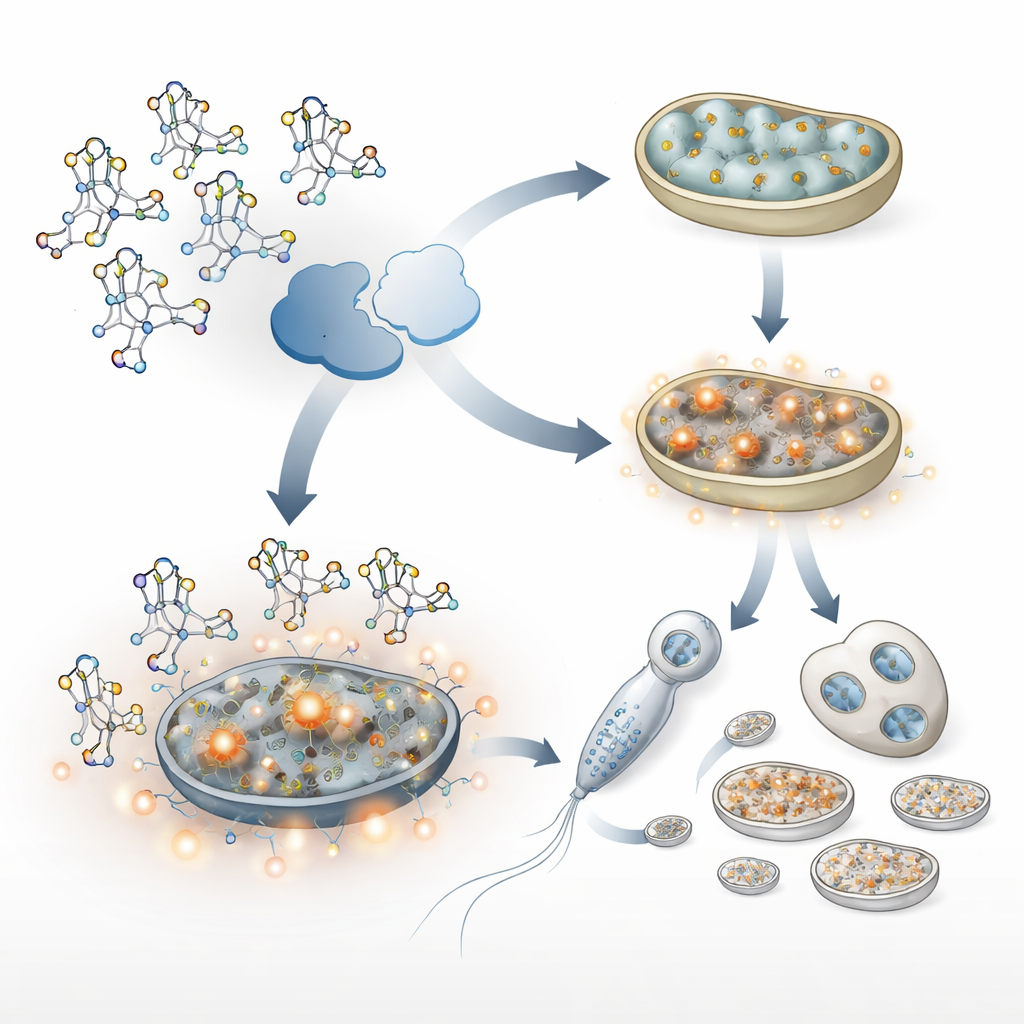
Sygnały stresu, które chronią — i przypadkowo zachowują — mitochondria ojcowskie
Stresowane mitochondria często produkują więcej reaktywnych form tlenu, chemicznie agresywnych produktów ubocznych metabolizmu. U robaków pozbawionych ALKB-1 ilość tych reaktywnych cząsteczek wzrosła znacząco. To z kolei uruchomiło dwa kluczowe programy odpowiedzi na stres: jeden prowadzony przez czynnik podobny do ludzkiego Nrf2 (u robaków nazywany SKN-1) oraz drugi znany jako mitochondrialna odpowiedź na niepoprawnie złożone białka. Razem te szlaki zwiększyły produkcję nowych mitochondriów i kopiowanie mitochondrialnego DNA, szczególnie w plemnikach. Choć ta odpowiedź pomaga komórkom radzić sobie z uszkodzeniem, miała też niezamierzony skutek uboczny: więcej mitochondriów i mitochondrialnego DNA ojca gromadziło się i trudniej było je usunąć po zapłodnieniu. Zablokowanie tych szlaków stresu lub zmniejszenie uszkodzeń oksydacyjnych za pomocą przeciwutleniaczy przywracało bardziej normalne usuwanie mitochondriów ojcowskich.
Gdy sprzątanie zawodzi, cierpią płodność i zarodki
Opóźnione usuwanie mitochondriów ojca nie było tylko mikroskopijną ciekawostką. Samce robaków pozbawione właściwej aktywności ALKB-1 spłodziły mniej potomstwa, a tworzone przez nich zarodki częściej ginęły. Jednocześnie ich plemniki tworzyły się w normalnej liczbie i wyglądały strukturalnie prawidłowo, co sugeruje, że główny problem leżał w kontroli jakości mitochondriów, a nie w samym wytwarzaniu plemników. Badanie proponuje, że znaczniki tRNA kontrolowane przez ALKB-1 działają jako epigenetyczny checkpoint: gdy ten system działa, równowaga białek mitochondrialnych jest utrzymana, stres pozostaje w ryzach, a mitochondria ojcowskie są bezpiecznie eliminowane. Gdy zawodzi, zestresowane i nadmiarowe mitochondria ojca utrzymują się, szkodząc płodności i wczesnemu rozwojowi. Chociaż eksperymenty przeprowadzono na robakach, ujawniają one zasadniczą zasadę — że drobne chemiczne edycje RNA mogą kierować tym, jak dziedziczymy nasze komórkowe elektrownie i ostatecznie wpływać na zdrowie rozrodcze u bardziej złożonych zwierząt, w tym u ludzi.
Cytowanie: Luo, Z., Li, Y., He, C. et al. ALKB-1-dependent tRNA methylation is required for efficient paternal mitochondrial elimination. Nat Commun 17, 2144 (2026). https://doi.org/10.1038/s41467-026-68813-6
Słowa kluczowe: dziedziczenie mitochondrialne, mitochondria ojcowskie, modyfikacja tRNA, stres oksydacyjny, Płodność męska