Clear Sky Science · pl
Atlasy absolutnej ilości małych niekodujących RNA w różnych tkankach ssaków i liniach komórkowych
Dlaczego małe cząsteczki RNA są ważne
W każdej komórce zespoły małych cząsteczek RNA pomagają decydować, które geny są włączane lub wyłączane. Te małe niekodujące RNA działają jak ściemniacze dla naszych programów genetycznych, kształtując rozwój, funkcję narządów i choroby. Mimo zaawansowanych technologii sekwencjonowania, naukowcy mieli trudności z dokładnym zmierzeniem, ile tych cząsteczek jest obecnych w różnych komórkach i tkankach. W tym badaniu przedstawiono dokładniejszą metodę ich zliczania i zbudowano szczegółowy atlas pokazujący rzeczywistą obfitość tych molekuł w wielu tkankach ssaków i typowych liniach komórkowych stosowanych w laboratorium.
Jaśniejszy sposób zliczania małych RNA
Tradycyjne metody sekwencjonowania małych RNA polegają na enzymach, które dołączają adaptery przed odczytem cząsteczek. Enzymy te preferują określone kształty i chemiczne zakończenia, więc niektóre RNA są wychwytywane wydajnie, podczas gdy inne są pomijane lub niedoszacowane. Ten uprzedzony efekt jest szczególnie dotkliwy dla niektórych klas, takich jak piRNA i roślinne małe RNA, które noszą ochronne modyfikacje chemiczne na końcach. Autorzy opracowali nowy protokół nazwy 4NBoost, który przeprojektowuje adaptery i warunki reakcji, by wyrównać te preferencje, oraz dodaje wbudowane kody molekularne umożliwiające odróżnienie prawdziwych cząsteczek od kopii powstałych podczas amplifikacji.
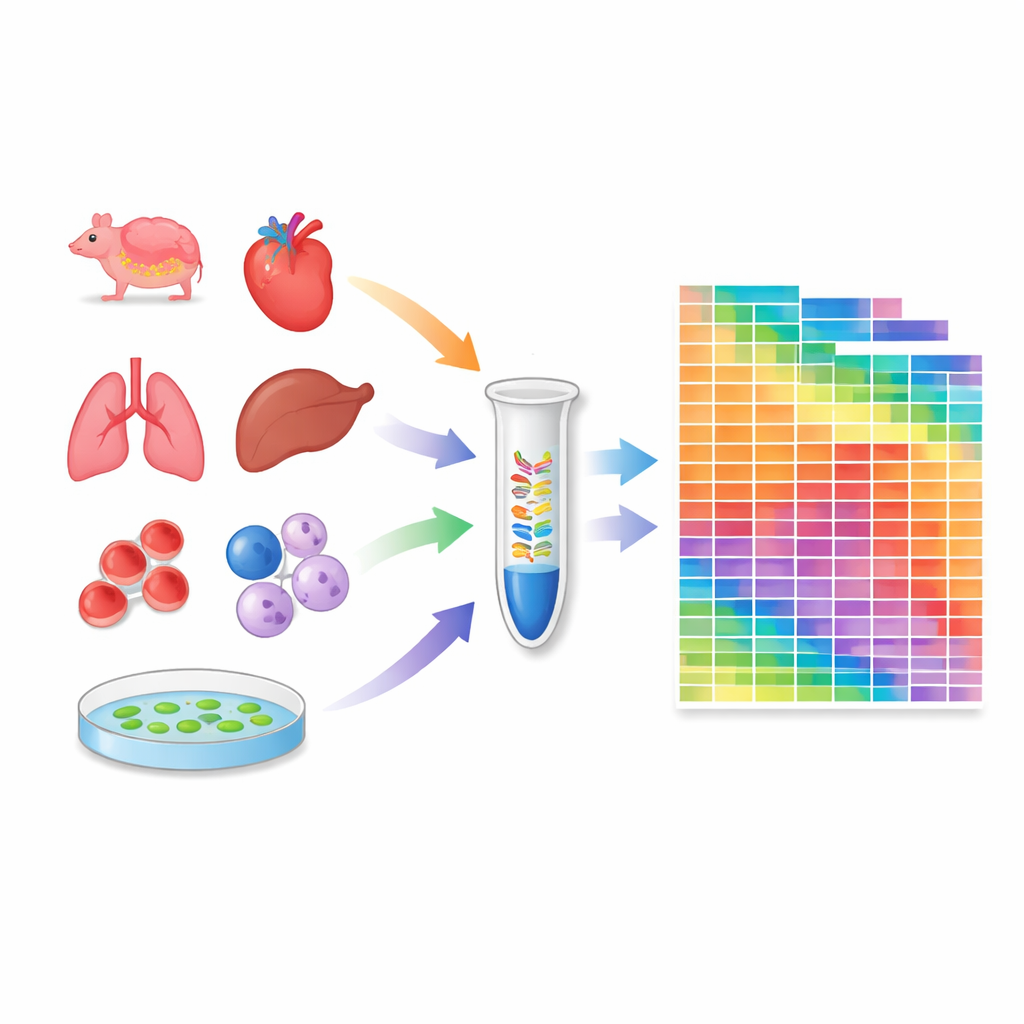
Przekształcenie protokołu w narzędzie pomiarowe
Aby przekształcić 4NBoost z względnego odczytu w narzędzie pomiarowe, zespół dodał starannie zaprojektowane syntetyczne RNA „spike‑in” o znanych stężeniach obejmujących bardzo szeroki zakres. Porównując, ile razy każde spike‑in zostało odczytane przez sekwencer z tym, ile go pierwotnie dodano, zbudowali krzywe wzorcowe, które przekształcają liczbę odczytów na absolutne liczby cząsteczek. Testy z różnymi mieszankami spike‑in i dodatkowymi kontrolnymi RNA pokazały, że 4NBoost może śledzić obfitość dokładnie na kilku rzędach wielkości, w tym RNA z problematycznymi modyfikacjami chemicznymi. Nawet przy zaczynaniu od zaledwie jednego nanograma RNA całkowitego, metoda wiernie oddawała krajobraz małych RNA.
Budowanie atlasu w tkankach i liniach komórkowych
Wyposażeni w skalibrowany protokół, badacze profilowali 259 próbek: 20 tkanek myszy, 18 tkankek pawiana krabożernego (makaka), 24 powszechnie używane linie komórkowe ludzi i myszy oraz kilka tkanek modelowej rośliny Arabidopsis. Dla każdej próbki oszacowali absolutną liczbę cząsteczek dla tysięcy mikroRNA i piRNA. Ujawniono, ile różnych gatunków mikroRNA występuje w każdym kontekście i jak ich całkowite ilości różnią się między tkankami i gatunkami. Niektóre linie komórkowe i narządy mają szczególnie bogate repertoary mikroRNA, podczas gdy inne, takie jak komórki krwi, zdominowane są przez kilka bardzo obfitych gatunków. Atlas ujawnił też znaczne różnice między tkankami myszy i makaka, podkreślając, że regulacja małych RNA może być specyficzna dla gatunku.
Korekta starych danych i rewizja powszechnych założeń
Gdy nowy atlas porównano z popularnymi bazami danych małych RNA zbudowanymi przy użyciu konwencjonalnych metod, pojawiły się uderzające rozbieżności. Kilka ważnych rodzin mikroRNA — takich jak miR‑19 i miR‑29 — okazało się znacznie bardziej obfitych niż dotąd sądzono, podczas gdy inne — jak szeroko badane rodziny let‑7 i miR‑10 — często były przeszacowane. Badanie ponownie przeanalizowało także, która „strona” prekursora (ramię) jest faktycznie wykorzystywana w komórkach, odkrywając przypadki, gdzie obecne adnotacje wskazują błędny dominujący łańcuch. Aby uratować bogactwo istniejących zdeformowanych zestawów danych, autorzy wytrenowali model uczenia maszynowego, który uczy się, jak konwencjonalne pomiary odbiegają od 4NBoost, a następnie matematycznie koryguje je, by lepiej odzwierciedlały rzeczywistą obfitość.
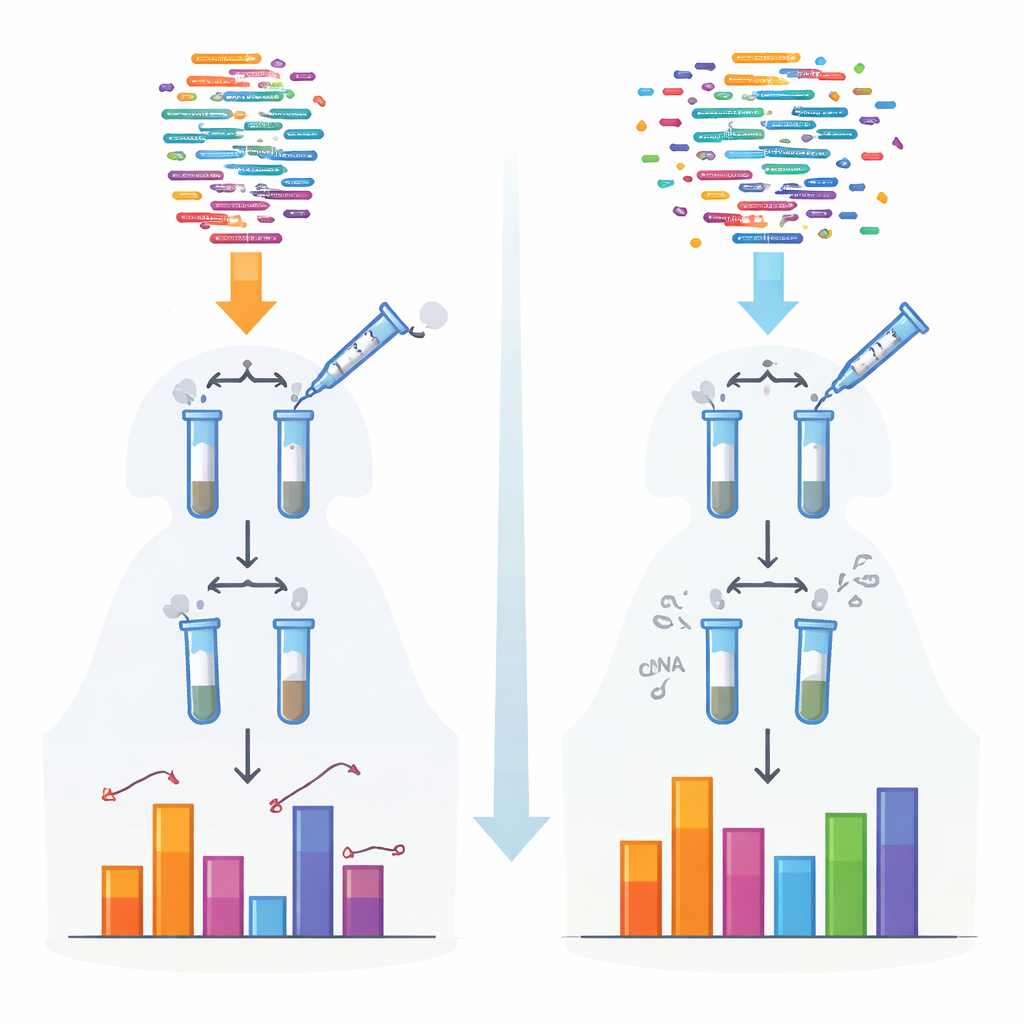
Publiczne źródło do badania małych RNA
Wszystkie pomiary 4NBoost i model korekcji są udostępnione bezpłatnie przez platformę internetową o nazwie SmRNAQuant. Badacze mogą przeglądać lub pobierać absolutne poziomy małych RNA dla konkretnych tkanek, linii komórkowych lub mikroRNA, a także przesyłać własne dane przygotowane przy użyciu popularnego zestawu, aby uzyskać wartości skorygowane pod kątem uprzedzeń. Dla osób niebędących specjalistami kluczowe przesłanie jest takie: zliczanie ma znaczenie — drobne różnice w liczbie kopii małych RNA mogą przesądzać o tym, czy gen jest aktywnie regulowany, czy brak jest jakiegokolwiek efektu. Dostarczając bardziej wiarygodne liczby i sposób naprawy starszych danych, praca ta tworzy mocniejszą ilościową podstawę do zrozumienia, jak małe RNA kształtują normalną biologię i choroby.
Cytowanie: Xiao, W., Zheng, Y., Zhang, H. et al. An absolute quantification atlas of small non-coding RNAs across diverse mammalian tissues and cell lines. Nat Commun 17, 2314 (2026). https://doi.org/10.1038/s41467-026-68812-7
Słowa kluczowe: ilościowe oznaczanie mikroRNA, małe niekodujące RNA, błąd w sekwencjonowaniu RNA, atlas ekspresji w tkankach, korekcja uczeniem maszynowym