Clear Sky Science · pl
Funkcjonalny krajobraz alternatywnego składania w procesie zobowiązywania linii hematopoetycznej
Jak drobne poprawki w genach kształtują naszą krew
Co sekundę w twoim organizmie powstają miliony nowych komórek krwi. Za tym cichym cudem stoi molekularny system edycji, który potrafi wycinać i wklejać fragmenty komunikatów genetycznych w różny sposób, tworząc nieco różniące się wersje tego samego białka. W tym badaniu analizowano, jak ten proces, zwany alternatywnym składaniem, pomaga kierować niedojrzałe komórki macierzyste ku przemianie w erytrocyty, leukocyty lub inne typy komórek krwi — oraz co się dzieje, gdy zabraknie pojedynczego zedytowanego fragmentu.
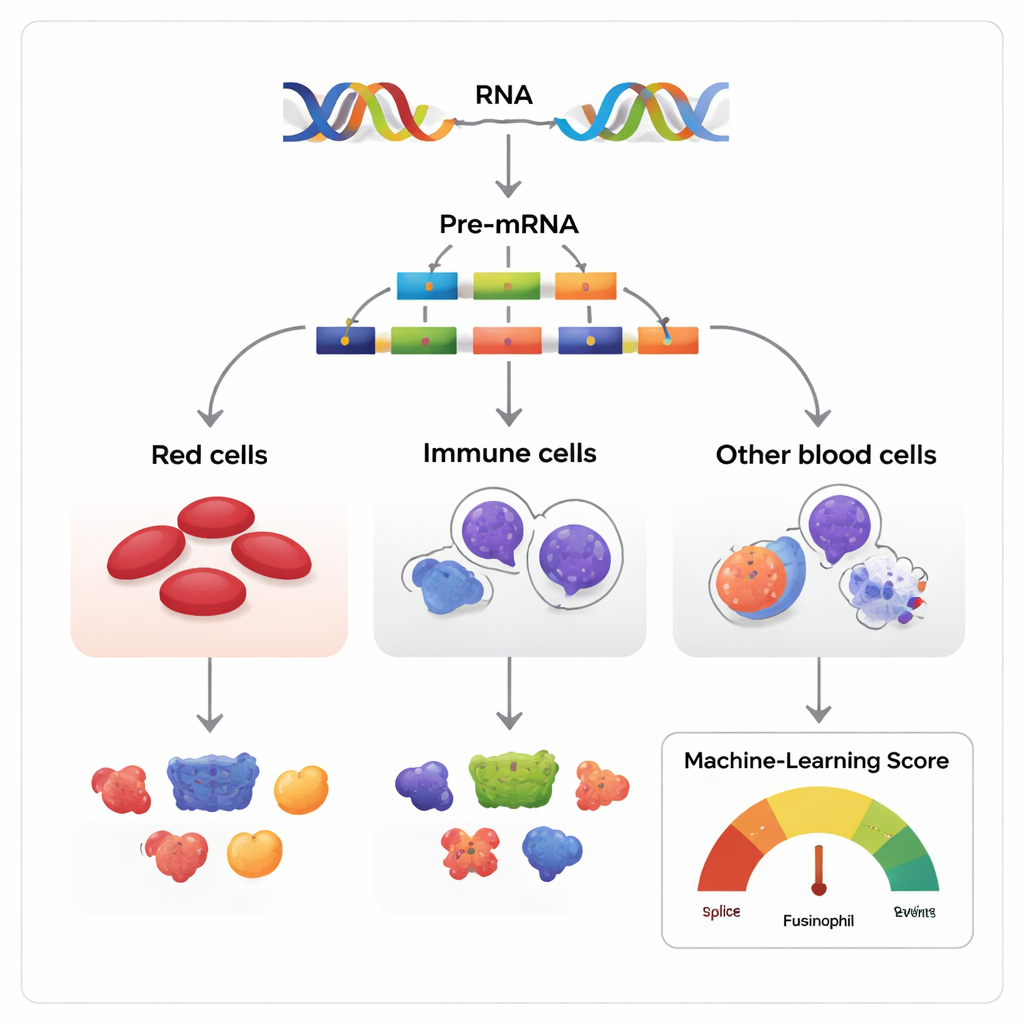
Wiele wersji z tego samego scenariusza genetycznego
Geny często opisuje się jako plany, ale w rzeczywistości przypominają raczej scenariusze, które można przearanżować. Gdy gen jest odczytywany, początkowa kopia RNA zawiera segmenty zwane eksonami, które przed przekształceniem w białko mogą być zachowane lub pominięte. Autorzy badania śledzili ten proces, znany jako pomijanie eksonów, w tkankach formujących krew u ludzi, myszy i kilku innych kręgowców. Zebrali ponad 270 zestawów danych RNA, które razem opisują, jak komórki macierzyste i progenitorowe krwi dojrzewają do trzech głównych linii: erytroidnej (produkującej krwinki czerwone), mieloidnej (walczącej z infekcjami) oraz limfoidalnej (wytwarzającej przeciwciała).
Ranking zmian splicingowych według znaczenia
Ponieważ większość genów z wieloma eksonami może być składana na wiele sposobów, zasadniczym wyzwaniem jest odróżnić warianty nieszkodliwe od tych, które faktycznie wpływają na los komórki. Badacze zbudowali model uczący maszynowo, nazwany Functional AS Score (FAScore), aby rozwiązać ten problem. Dla każdego zdarzenia pomijania eksonu model uwzględnia 19 cech, takich jak siła zmiany użycia w trakcie rozwoju komórkowego, stopień konserwacji otaczającego DNA między gatunkami, czy zmiana dotyczy znanych domen białkowych oraz czy obszar zawiera miejsca modyfikacji chemicznych białka. Algorytm, trenowany w strategii positive–unlabeled z klasyfikacją typu random forest, zwraca wynik od 0 do 1 wskazujący, jak prawdopodobne jest, że dane zdarzenie splicingowe ma funkcjonalny wpływ.
Wykrywanie zachowanych, specyficznych dla linii przełączników
Stosując FAScore do dziesiątek tysięcy zdarzeń pomijania eksonów, zespół sklasyfikował je jako prawdopodobnie funkcjonalne, niefunkcjonalne lub niepewne. Zdarzenia przewidywane jako funkcjonalne częściej występowały w regionach białkowych ważnych dla interakcji, w sekwencjach ewolucyjnie zachowanych oraz w segmentach zawierających chemiczne znaczniki, takie jak fosforylacja czy SUMOylacja. Wiele z tych zdarzeń było aktywnych jedynie w określonych liniach krwi lub w trakcie formowania krwi płodowej, co sugeruje, że działają jako precyzyjne przełączniki w określonych oknach rozwojowych. Badanie wykazało też, że niektóre z najstarszych zdarzeń splicingowych — te współdzielone przez kręgowce od setek milionów lat — są szczególnie skłonne być funkcjonalne, co odzwierciedla skłonność starszych genów do pełnienia podstawowych ról biologicznych.
Dowód eksperymentalny: modulowanie losów komórek krwi
Aby przetestować przewidywania modelu, autorzy wybrali kilka eksonów o wysokich ocenach w genach aktywnych w różnych liniach krwi i usunęli je w komórkach macierzystych i progenitorowych mysiej krwi przy użyciu CRISPR. Wyniki potwierdziły oczekiwania modelu: usunięcie określonych eksonów w genach KLF6 i SSBP3 osłabiło tworzenie kolonii mieloidalnych bez uszczerbku dla produkcji erytrocytów, podczas gdy usunięcie eksonów w EPB41L1 i TBC1D23 zmieniało formowanie kolonii erytroidalnych. W szczególności pominięcie eksonu 15 w TBC1D23 zmniejszyło produkcję prekursorów erytrocytów u myszy i u zebrafish, prowadząc do mniejszej liczby krwinek czerwonych we krwi i niższego poziomu hemoglobiny, przy stosunkowo niewielkim wpływie na leukocyty.
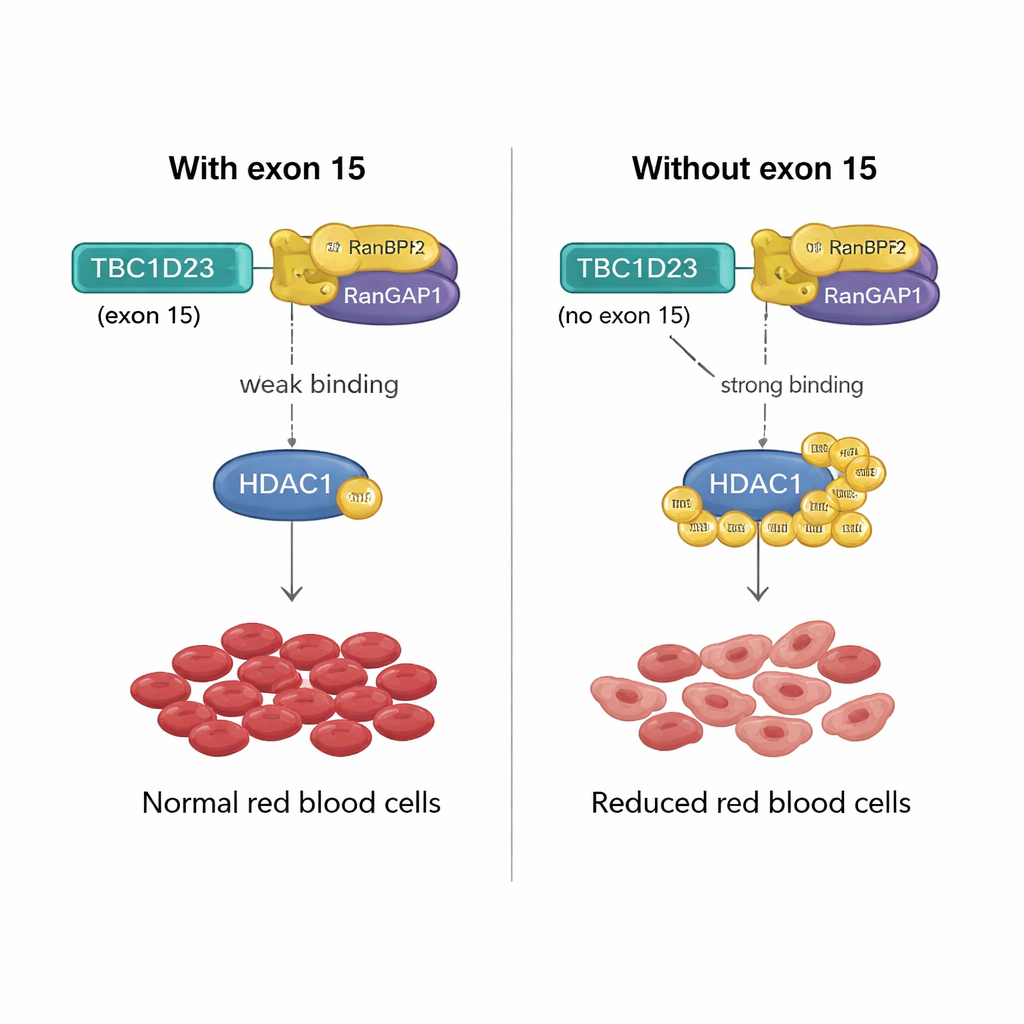
Molekularna dźwignia dla produkcji erytrocytów
Jak fragment kodujący 15 aminokwasów z eksonu 15 TBC1D23 może mieć taki efekt? Zespół odkrył, że włączenie tego eksonu osłabia wiązanie TBC1D23 z parą białek RANBP2/RANGAP1, która współpracuje przy przyłączaniu znaczników SUMO do innych białek. Bez eksonu 15 TBC1D23 silniej wiąże tę parę, zwiększając SUMOylację kluczowego enzymu HDAC1. Intensyfikacja tego znaczkowania zmienia aktywność wielu czynników transkrypcyjnych — głównych regulatorów ekspresji genów — zaburzając programy genowe potrzebne do prawidłowego dojrzewania erytrocytów. Gdy badacze zmodyfikowali wersję HDAC1, której nie można SUMO-ować w dwóch kluczowych miejscach, przywróciło to tworzenie erytrocytów w komórkach pozbawionych eksonu 15 TBC1D23, potwierdzając, że to chemiczne znakowanie jest krytycznym krokiem.
Dlaczego to ma znaczenie dla zdrowia i przyszłych terapii
Dla osoby niebędącej specjalistą główne przesłanie tego badania jest takie, że nie wszystkie zmiany genetyczne są równe: czasami różnica między zdrową krwią a anemią polega na tym, czy drobny fragment genu zostanie zachowany czy pominięty w ostatecznym komunikacie. Łącząc dane RNA na dużą skalę z zaawansowanym systemem oceniania, badanie dostarcza mapy drogowej do wykrywania wariantów splicingowych, które najpewniej wpływają na wybory losów komórek macierzystych. Podejście to pogłębia naszą wiedzę o formowaniu komórek krwi w zdrowiu i chorobie, a także oferuje ogólną strategię identyfikacji istotnych zdarzeń splicingowych w innych narządach, co może ukierunkować przyszłe terapie genowe i spersonalizowane leczenie.
Cytowanie: Hu, X., Wang, J., Chen, L. et al. The functional landscape of alternative splicing in hematopoietic lineage commitment. Nat Commun 17, 2047 (2026). https://doi.org/10.1038/s41467-026-68811-8
Słowa kluczowe: alternatywne składanie, hematopoeza, uczenie maszynowe, erytrocyty, regulacja genów