Clear Sky Science · pl
Podstawa strukturalna regulacji transkrypcji przez regulator podziału komórkowego MraZ w Mycoplasma genitalium
Jak drobna bakteria decyduje, kiedy się dzieli
Każda żywa komórka musi zdecydować, kiedy podzielić się na dwie, a ta decyzja może decydować o różnicy między zdrowym wzrostem a niekontrolowaną infekcją. W tym badaniu przyglądamy się jednej z najprostszych znanych bakterii, Mycoplasma genitalium, by ujawnić w skali atomowej, jak pojedyncze białko, zwane MraZ, przyczepia się do DNA i włącza lub wyłącza kluczowe geny związane z podziałem komórkowym. Zrozumienie tego minimalistycznego systemu kontroli pozwoli naukowcom odkryć ogólne zasady wzrostu bakterii, które w przyszłości mogą zainspirować nowe rodzaje antybiotyków lub syntetyczne „minimalne komórki”.
Uproszczona komórka z ważnymi lekcjami
Mycoplasma genitalium jest znana z bardzo małego genomu: to zaledwie ułamek DNA obecnego w powszechnych bakteriach, takich jak E. coli. Ten niewielki rozmiar czyni ją silnym modelem do ustalenia, które geny i systemy sterujące są rzeczywiście niezbędne do życia. Wiele bakterii przechowuje geny związane z podziałem komórkowym i ścianą komórkową w bloku zwanym klastrem dcw. W mykoplazmach pozbawionych ściany większość tych genów zanikła, ale kilka pozostało, w tym mraZ na samym początku klastra. MraZ działa jak kierownik ruchu, kontrolując aktywność sąsiednich genów, które z kolei wpływają na to, jak i kiedy komórka się dzieli.
Powtarzający się wzorzec DNA jako przełącznik kontrolny
Tuż przed genem mraZ badacze znaleźli wysoko konserwowany odcinek DNA, który działa jak stacja dokująca dla białka MraZ. Region ten zawiera cztery krótkie, powtórzone segmenty, lub „pola”, które mają niemal identyczną sekwencję w wielu gatunkach bakterii. Poprzez ostrożne mutowanie jednego, dwóch lub większej liczby tych pól i następnie mierzenie, jak mocno MraZ nadal może wiązać DNA, zespół wykazał, że białko wiąże się kooperatywnie: każde pole wzmacnia ogólny chwyt. Eksperymenty z reporterem wykorzystujące fluorescencyjny znacznik potwierdziły, że im bardziej te pola były zaburzone, tym mniej skutecznie MraZ potrafił tłumić aktywność genu, co podkreśla ich znaczenie jako precyzyjnie dostrojonego panelu kontrolnego. 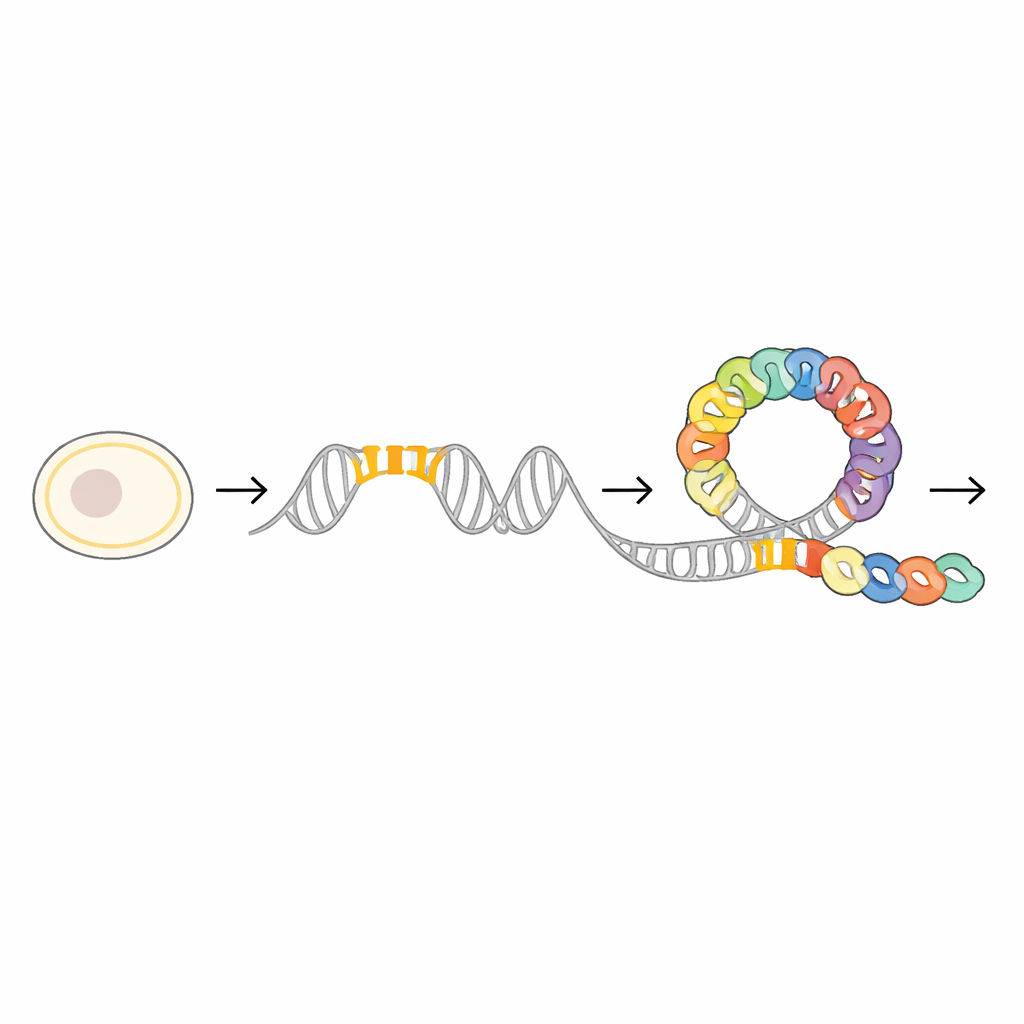
Białko w kształcie pierścienia, które otwiera się, by objąć DNA
Aby zobaczyć, jak ten panel działa na poziomie atomowym, naukowcy użyli kriomikroskopii elektronowej i krystalografii rentgenowskiej, rozwiązując kilka trójwymiarowych struktur MraZ samego i związanego z DNA. Samodzielnie cząsteczki MraZ łączą się w struktury pierścieniowe złożone z ośmiu lub dziewięciu identycznych podjednostek. Te pierścienie mają charakterystyczną „kolebkową” powierzchnię utworzoną przez małą strukturę beta‑arkusza, odmienną od spiralnych helis często widywanych w białkach wiążących DNA. Gdy MraZ napotyka segment DNA z czterema polami, pierścień nie po prostu osiada na helisie; zamiast tego rozciąga się i przegrupowuje, tak że cztery jego podjednostki ustawiają się wzdłuż DNA, każda obejmując jedno pole w bruzdzie głównej.
Kluczowe punkty kontaktu odczytujące kod DNA
Struktury o wysokiej rozdzielczości ujawniły, że każda podjednostka stykająca się z DNA używa trzech naładowanych dodatnio grup bocznych — konkretnych punktów na powierzchni białka — do odczytu sekwencji DNA. Te chemiczne „palce” sięgają do bruzdy podwójnej helisy i tworzą precyzyjne wiązania wodorowe z określonymi parami zasad w konserwowanych polach. Gdy badacze zmienili którykolwiek z tych trzech reszt, MraZ w dużym stopniu tracił zdolność do wiązania DNA i do wyciszania testowego genu‑reportera. Dodatkowe kontakty z kręgosłupem DNA pomagają stabilizować kompleks, ale są mniej specyficzne względem sekwencji. Razem te wyniki pokazują, jak MraZ łączy wysoko wyspecjalizowaną głowicę odczytującą z elastycznym, wielopodjednostkowym korpusem, aby rozpoznać swój docelowy region. 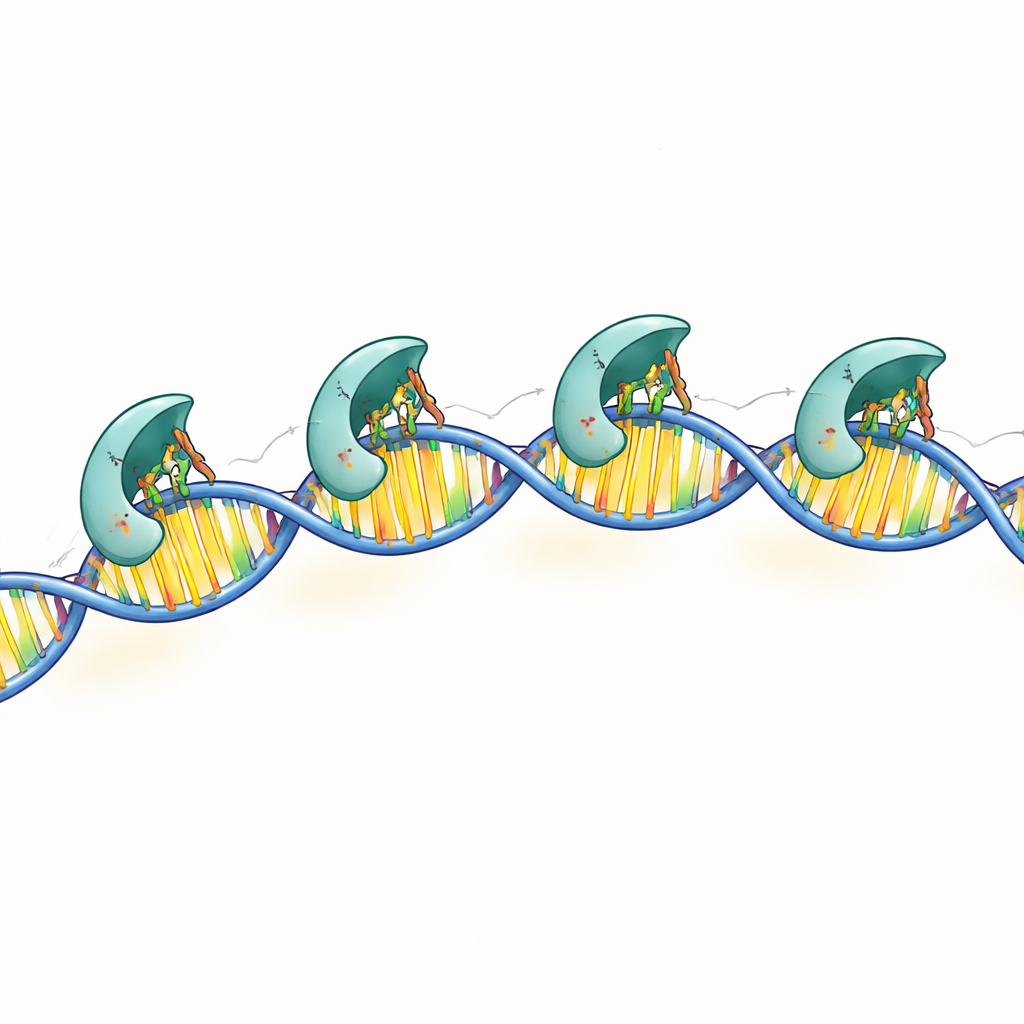
Oligomery dostrajające siłę kontroli
Ponieważ MraZ tworzy pierścienie i inne wielounitowe kształty, zespół zapytał, czy to grupowanie jest wymagane do wiązania DNA, czy jedynie je dostraja. Inżynierując wersję MraZ, która nie mogła się już składać w pierścienie, odkryli, że białko nadal wiązało sekwencję czteropól DNA, ale z mniejszym powinowactwem. Ta monomeryczna forma miała szczególne trudności, gdy zmieniano odstępy między polami, co sugeruje, że pełne oligomery pomaga łączyć i wyrównywać odległe pola, zwiększając lokalne stężenie motywów wiążących wzdłuż DNA. Autorzy proponują model dynamiczny, w którym MraZ przełącza się między zamkniętym pierścieniem a otwartą, związana z DNA formą, używając stanu swojej agregacji jak pokrętła do regulacji, jak mocno zaciska się na promotorze.
Co to oznacza dla bakterii i nie tylko
Mówiąc prościej, praca ta wyjaśnia, jak małe białko w minimalnej bakterii chwyta powtarzający się wzorzec na DNA i używa go jako głównego przełącznika dla genów związanych z podziałem komórkowym. Połączenie kolebkowej głowicy odczytującej i elastycznego pierścieniowego korpusu pozwala MraZ rozpoznawać swój cel z wysoką precyzją, pozostając jednocześnie dostosowalnym do różnych ułożeń DNA. Ponieważ podobne białka i motywy DNA występują w wielu bakteriach, mechanizm odkryty tutaj prawdopodobnie stanowi powszechną strategię koordynacji wzrostu i podziału. Wnioski z tego uproszczonego systemu mogą pomóc badaczom zaprojektować uproszczone obwody genetyczne w komórkach syntetycznych i — w dłuższej perspektywie — przyczynić się do nowych sposobów zakłócania wzrostu bakterii w chorobach.
Cytowanie: Sánchez-Alba, L., Varejão, N., Durand, A. et al. Structural basis for transcriptional regulation by the cell division regulator MraZ in Mycoplasma genitalium. Nat Commun 17, 2132 (2026). https://doi.org/10.1038/s41467-026-68809-2
Słowa kluczowe: podział komórkowy bakterii, interakcja DNA–białko, regulacja transkrypcji, kriomikroskopia elektronowa, Mycoplasma genitalium