Clear Sky Science · pl
Trajektorie komórkowe i transkrypcyjne specyfikacji losu neuronowego u ukwiałów odkrywają dwa tryby neurogenezy dorosłych
Jak proste stworzenie wciąż wytwarza nowe komórki mózgowe
Większość zwierząt, w tym ludzie, produkuje większość neuronów we wczesnym okresie życia, a potem w dużej mierze przestaje to robić. Jednak niektóre pozornie proste organizmy, jak ukwiały, nadal dodają nowe komórki nerwowe przez całe dorosłe życie. To badanie bada, jak ukwiał gwiazdkowy (Nematostella vectensis) ciągle odnawia i przekształca swoją rozproszoną sieć nerwową, ujawniając strategie, które mogą odzwierciedlać dawne rozwiązania dotyczące wzrostu i naprawy mózgów.
Rosnące ciało potrzebuje rosnącej sieci nerwowej
Ukwiały nie mają mózgu; zamiast tego mają pajęczynową sieć nerwową rozciągniętą w obrębie ściany ciała. Ponieważ te zwierzęta rosną lub kurczą się w zależności od dostępności pokarmu, ich sieć nerwowa musi się odpowiednio zwiększać lub zmniejszać. Używając światłoczułego białka fluorescencyjnego jako znacznika czasowego, autorzy oznaczyli istniejące neurony u młodych osobników dorosłych, a następnie obserwowali pojawianie się nowo powstałych komórek w ciągu następnego tygodnia. Stwierdzili obfitość nowych neuronów rozrzuconych wzdłuż osi ciała, nieograniczonych do specjalnej strefy wzrostu. Nowe komórki pojawiały się zarówno na stronie skierowanej ku ustom, jak i na przeciwległym końcu zwierzęcia, co pokazuje, że neurogeneza dorosłych jest przestrzennie rozpowszechniona i ciągła.
Śledzenie pochodzenia nowych komórek nerwowych
Aby odkryć, skąd pochodzą te nowe neurony, badacze połączyli obrazowanie na żywo z sekwencjonowaniem RNA pojedynczych komórek, techniką odczytującą, które geny są aktywne w tysiącach pojedynczych komórek. Skoncentrowali się na komórkach niosących fluorescencyjne „reportery” kontrolowane przez trzy kluczowe geny: FoxL2, SoxC i Elav. FoxL2 oznacza szeroką pulę dzielących się, multipotentnych komórek progenitorowych; SoxC jest włączany krótko, gdy komórki zaczynają się specjalizować; a Elav jest silnie aktywny w neuronach peptydergicznych, które komunikują się głównie za pomocą małych peptydowych sygnałów. Zespół wykazał, że populacja komórek pozytywnych dla FoxL2 i Piwi1 zachowuje się jak komórki macierzyste: samoodnawiają się, jednocześnie nieustannie generując zróżnicowane potomstwo, w tym neurony, komórki parzydełkowe zwane cnidocytami oraz komórki wydzielnicze. SoxC i Elav, przeciwnie, zapalają się dopiero, gdy komórki opuszczają tę pulę progenitorową i zobowiązują się do określonych losów neuronowych.
Dwie różne drogi do neuronów dorosłych
Porównując czas działania reporterów z profilem ekspresji genów każdej komórki, badanie ujawniło dwa odrębne szlaki prowadzące do dojrzałych komórek nerwowych. Neurony peptydergiczne podążają bezpośrednią drogą: powstają z progenitorów, które już wykazują molekularny profil „zobowiązany do peptydergiczności”, a następnie szybko różnicują się w różne podtypy neuronów. Nowi przedstawiciele każdego podtypu pojawiają się proporcjonalnie do tego, jak powszechny jest dany podtyp, co sugeruje, że system utrzymuje zrównoważony skład typów neuronów, zamiast faworyzować konkretne. W tej linii nie stwierdzono wyraźnej serii pośrednich przystanków; zamiast tego ściśle spokrewnione podtypy neuronów wyłaniają się równolegle z podobnie przygotowanych komórek progenitorowych. 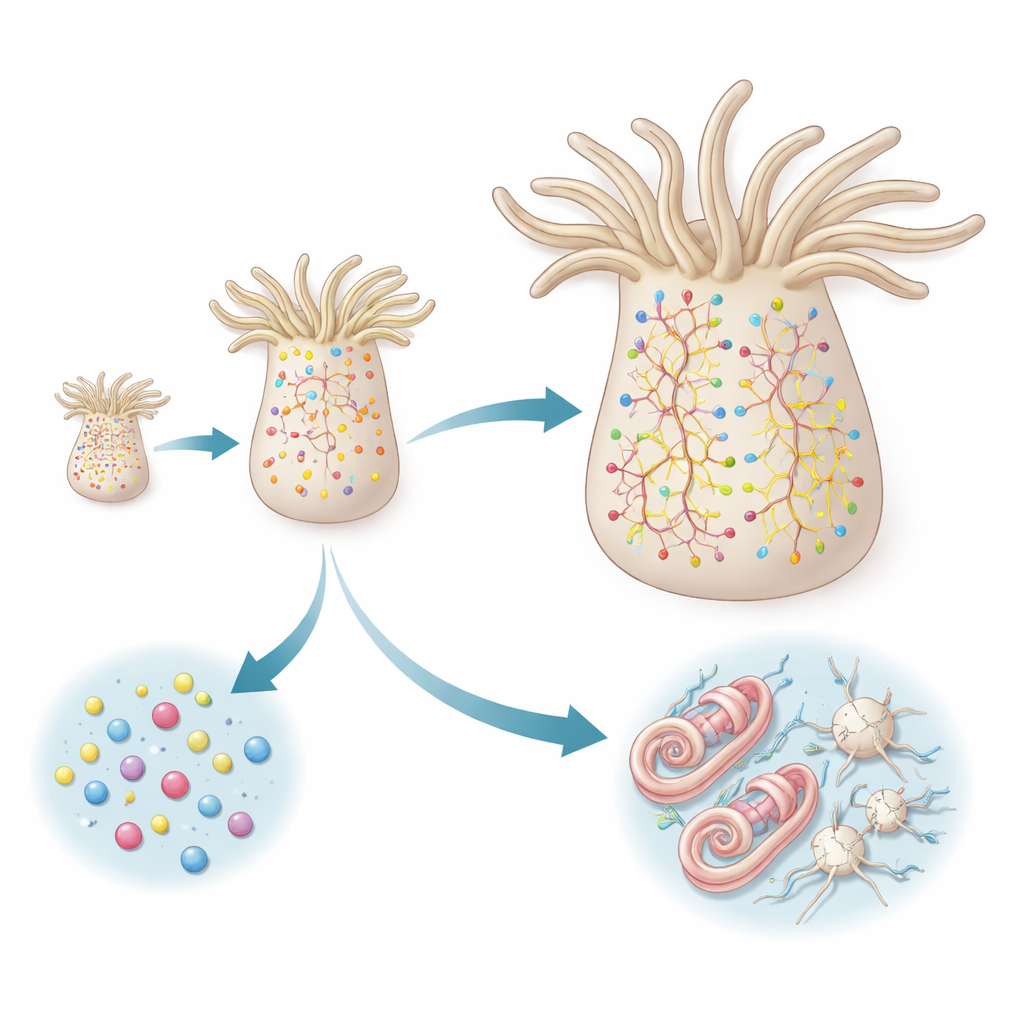
Szczególny przypadek komórek parzydełkowych
Cnidocyty, komórki parzydełkowe unikalne dla parzydełkowców, podążają bardziej stopniową drogą. Najpierw przechodzą przez fazę „budowy kapsuły”, podczas której konstruują swoje charakterystyczne organelle pod ciśnieniem, zdolne do wystrzeliwania mikroskopijnego harpunu. Etap ten polega na specyficznym zestawie genów regulatorowych i białek strukturalnych, które są w dużej mierze nieobecne w innych typach komórek. Dopiero po zakończeniu tego pośredniego programu cnidocyty włączają drugi, bardziej konwencjonalny program neuronalny, dodając kanały jonowe i inne składniki niezbędne do sygnalizacji elektrycznej. Dane genetyczne z mutantów zatrzymujących się na wczesnym etapie wzmacniają ten dwufazowy model: zablokowanie przejścia uniemożliwia pojawienie się późniejszych cech neuronalnych. 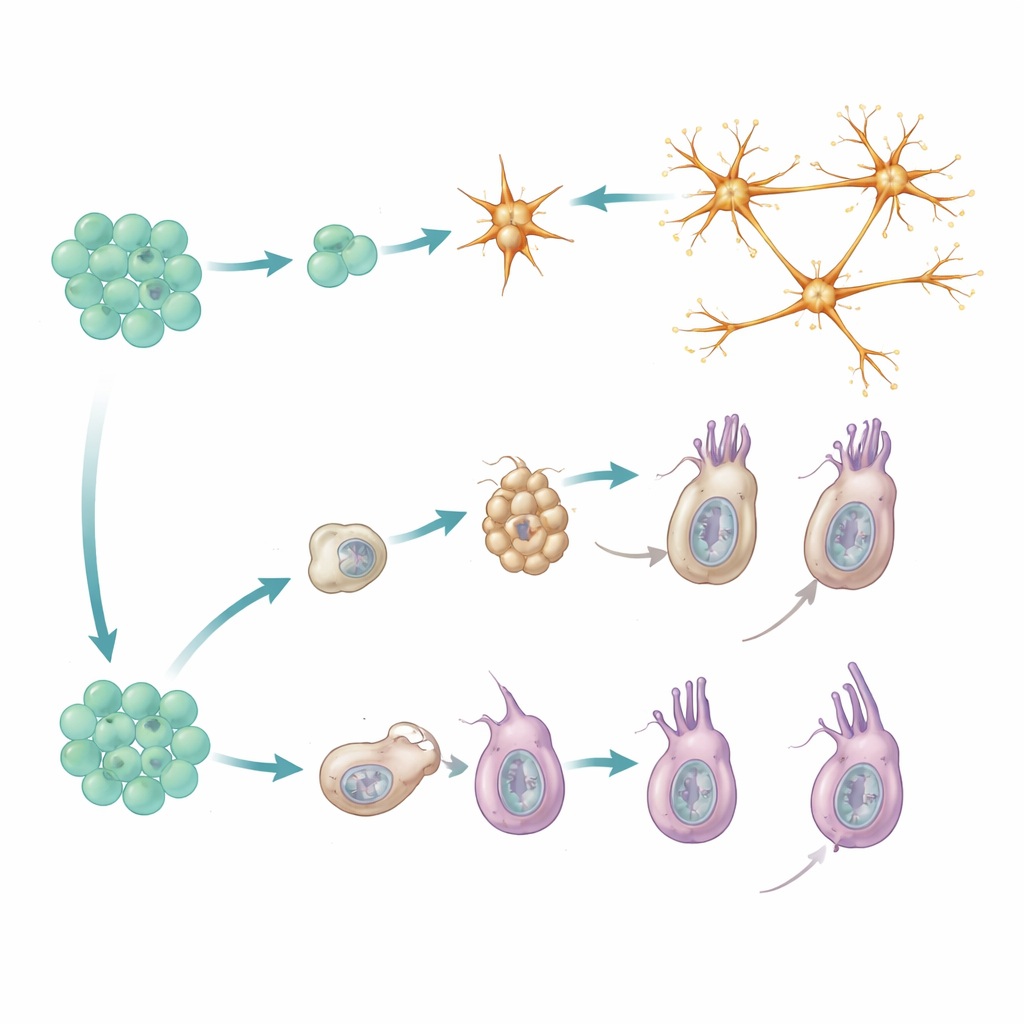
Wspólne zasady i pradawne korzenie
Pomimo różnych dróg, neurony peptydergiczne i cnidocyty polegają na nakładających się rodzinach genów regulatorowych, które utrwalają ich tożsamość. Szerokie cechy neuronalne wiążą się z czynnikami transkrypcyjnymi z rodzin bHLH i bZIP, podczas gdy drobne różnice tożsamości każdego podtypu neuronu określają unikalne kombinacje genów homeodomenowych i palców cynkowych — „kod” przypominający sposób definiowania typów neuronów u bardziej złożonych zwierząt, w tym u nicieni i kręgowców. Autorzy twierdzą, że te modułowe strategie — progenitory o cechach podobnych do komórek macierzystych, przejściowa aktywność SoxC podczas zobowiązywania oraz kody homeodomenowe definiujące podtypy — mogą reprezentować głęboko zachowane zasady neurogenezy. U ukwiałów wspierają one całe życie odnowę i skalowanie sieci nerwowej; u innych zwierząt powiązane mechanizmy mogą leżeć u podstaw zarówno ograniczonej neurogenezy dorosłych, jak i niezwykłych zdolności regeneracyjnych obserwowanych w niektórych liniach rozwojowych.
Cytowanie: Plessier, F., Marlow, H. Cellular and transcriptional trajectories of neural fate specification in sea anemone uncover two modes of adult neurogenesis. Nat Commun 17, 2611 (2026). https://doi.org/10.1038/s41467-026-68802-9
Słowa kluczowe: neurogeneza dorosłych, ukwiał, komórki progenitorowe nerwowe, cnidocyty, transkryptomika pojedynczych komórek