Clear Sky Science · pl
Dostarczanie koacerwatów peptydowych w celu utworzenia trwałych centrów interakcji w komórkach
Budowanie nowych „stanowisk pracy” wewnątrz komórek
Nasze komórki wypełnione są małymi przestrzeniami roboczymi, w których zachodzą istotne procesy — na przykład produkcja energii czy odpowiedzi na stres. Z czasem lub w przebiegu choroby naturalne stanowiska mogą działać gorzej. W tym badaniu autorzy badają sposób na wprowadzenie zupełnie nowych „centrów interakcji” do żywych komórek przy użyciu prostych, laboratoryjnie wytworzonych kropli zbudowanych z krótkich peptydów. Te syntetyczne centra potrafią wychwytywać określone białka, koncentrować je, a nawet pomagać w ich degradacji, co wskazuje na nowe strategie dla przyszłych terapii i inżynierii komórkowej.
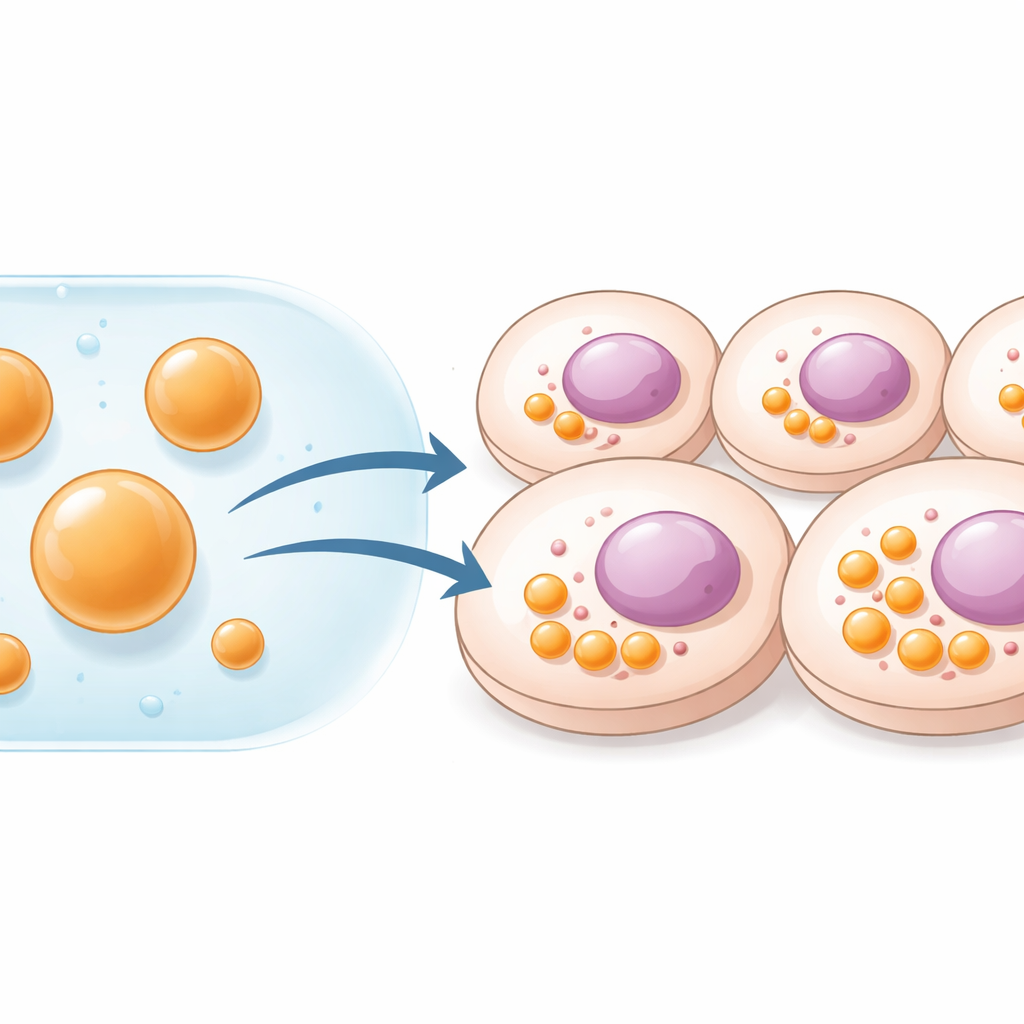
Dlaczego komórki potrzebują niestandardowych przestrzeni roboczych
Komórki zachowują porządek, dzieląc różne zadania na odrębne przegrody. Niektóre są otoczone błonami, jak mitochondria; inne to miększe, kroplopodobne struktury, które powstają, gdy pewne białka i RNA grupują się razem. Te płynne krople, zwane kondensatami, pełnią rolę centrów reakcji, przyspieszając lub wyłączając określone szlaki biochemiczne. Naukowcy wcześniej tworzyli takie przegrody, zmuszając komórki do wytwarzania specjalnych białek-szkieletów wstawianych genetycznie. Choć skuteczne, podejście to wymaga dostarczenia genów i ogranicza ilość materiału, jaką komórka może wyprodukować. Autorzy tego badania postanowili pominąć DNA i zamiast tego zbudować gotowe przegrody poza komórką, a następnie dostarczyć je bezpośrednio jako stabilne, mikrometrowe krople.
Peptydowe krople tworzące trwałe centra
Zespół pracował z krótkimi, nieuporządkowanymi peptydami znanymi jako HBpep oraz redoks-czułą wersją HBpep‑SA. W łagodnie kwaśnych warunkach peptydy te pozostają rozpuszczone, ale po przesunięciu pH w kierunku fizjologicznym — albo po obniżeniu temperatury — ulegają rozdziałowi fazowemu, tworząc miękkie, żelopodobne krople o średnicy około 1–5 mikrometrów. Poprzez regulację stężenia peptydów badacze mogli kontrolować zarówno rozmiar, jak i liczbę kropli. Techniki fluorescencyjne wykazały, że cząsteczki peptydów wewnątrz tych kropli poruszają się wolno, co wskazuje na stan żelowy wystarczająco trwały, by przetrwać rozwodnienie i manipulację. Po dodaniu do hodowli ludzkich komórek nowotworowych, mysich komórek czerniaka i pierwotnych ludzkich komórek odpornościowych, krople były efektywnie wchłaniane i gromadziły się w cytoplazmie. Większe krople szczególnie pozostawały nienaruszone przez co najmniej pięć dni, skutecznie działając jako długotrwałe, syntetyczne organella wewnątrz żywych komórek.
Ładowanie i ukierunkowywanie centrów
Aby te centra były użyteczne, muszą utrzymywać i organizować białka-ładunki. Badacze najpierw poprawili ładowanie, dołączając krótki, pochodny od HBpep tag do białka modelowego GFP. Ten tag sprzyjał silnej partycjonowaniu GFP do kropli i, co ciekawe, jego koncentracji w pobliżu powierzchni, tworząc organizację typu rdzeń‑powłoka. Następnie osadzili wewnątrz kropli nanociała — kompaktowe białkopodobne fragmenty o właściwościach przeciwciał, które ściśle wiążą wybrane cele. Nanocząstka wiążąca GFP pozwoliła centrom selektywnie wychwytywać GFP zarówno w probówkach, jak i wewnątrz komórek. Ponieważ żel peptydowy jest stosunkowo gęsty, początkowo większość uchwyconego GFP gromadziła się na powierzchni kropli. Jednak gdy struktura wewnętrzna została częściowo poluzowana, albo przez zmianę warunków redoks, albo przez pomoc w ucieczce kropli z otaczających je błon endosomalnych, GFP zaczęło także przenikać do wnętrza. W komórkach chemiczne pomocniki sprzyjające ucieczce z endosomów znacząco zwiększały odsetek centrów, które skutecznie rekrutowały swoje cele.
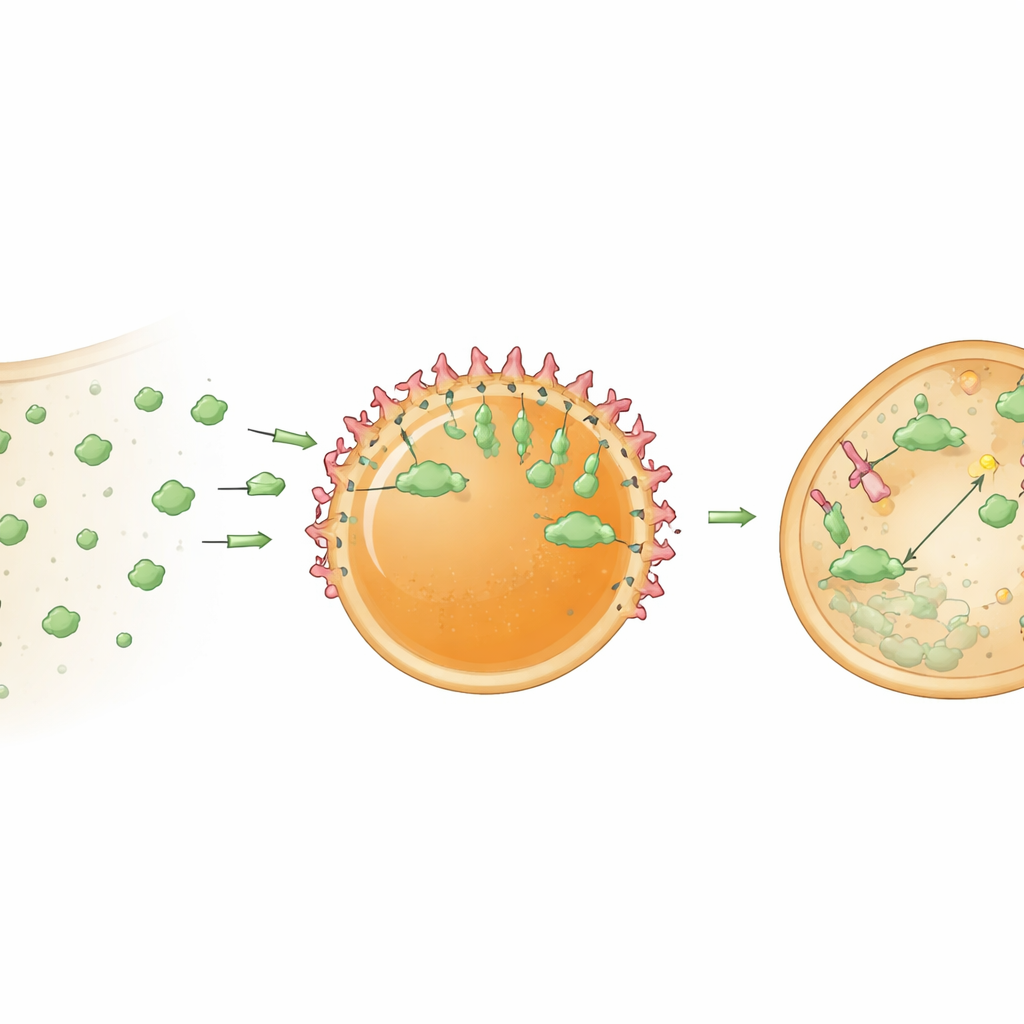
Przekształcanie centrów w „niszczarki” białek
Autorzy następnie ulepszyli te centra, przekształcając je z pasywnych pułapek w aktywne centra przetwarzania. Naładowali krople bioPROTAC‑iem — białkiem fuzyjnym łączącym nanocząstkę wiążącą cel z fragmentem adaptora enzymatycznego, który oznacza białka do zniszczenia przez komórkowe mechanizmy usuwania odpadów. Gdy te „degradosomowe” krople zostały wprowadzone do komórek stabilnie eksprymujących GFP, poziom GFP w cytosolu spadł o około 78 procent w ciągu doby. Kontrolne centra zawierające jedynie nanocząstkę sekwestrowały GFP, lecz nie obniżały istotnie jego całkowitego poziomu, co potwierdza, że silny spadek wynikał z ukierunkowanej degradacji, a nie zwykłego wychwytywania. Wyniki sugerują, że grupowanie bioPROTAC‑ów w skoncentrowanym mikrośrodowisku znacząco zwiększa ich siłę działania w porównaniu z ich swobodnym rozproszeniem w cytoplazmie.
Co to może znaczyć dla przyszłych terapii
Mówiąc prościej, praca ta pokazuje, że naukowcy mogą wytwarzać peptydowe krople w probówce, pakować je z niestandardowymi narzędziami białkowymi, a następnie dostarczać je do żywych komórek, gdzie zachowują się jak nowe, długotrwałe organella. Te syntetyczne centra mogą selektywnie przyciągać naturalne białka i, gdy są wyposażone w maszynerię degradującą, aktywnie usuwać wybrane cele z komórki. Ponieważ platforma ta unika modyfikacji genetycznych komórki i jest modułowa pod względem tego, co może przenosić, otwiera drogę do terapii, które przywracają lub przepisują zachowanie komórkowe — na przykład usuwając szkodliwe białka lub przebudowując wadliwe sygnalizowanie — poprzez proste zainstalowanie nowych, programowalnych „stanowisk pracy” w naszych komórkach.
Cytowanie: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
Słowa kluczowe: sztuczne organella, koacerwaty peptydowe, dostawa do wnętrza komórki, degradacja białek, inżynieria komórkowa