Clear Sky Science · pl
Trans-cięcie CRISPR-Cas9 jest utrudnione przez otoczony pętlę R, wydłużony spacer i nieaktywną domenę HNH
Dlaczego drobne nacięcia DNA mają znaczenie
CRISPR-Cas9 jest znany jako molekularny skalpel tnący DNA w wybranych miejscach, ale to narzędzie ma drugie, mniej doceniane zachowanie: po aktywacji potrafi także nadgryzać inne fragmenty materiału genetycznego w pobliżu. Zrozumienie, kiedy to „kolateralne” cięcie włącza się lub wyłącza, jest kluczowe dla tworzenia bezpieczniejszych terapii edycji genów i czułych testów diagnostycznych. W tym badaniu rozłożono na czynniki pierwsze cechy fizyczne kompleksu Cas9–DNA–RNA, które decydują, czy Cas9 wykona tylko zamierzony nacięcie, czy też zacznie rozcinać przypadkowe jednoniciowe fragmenty DNA.
Jak zaczynają się nożyce CRISPR
Aby działać, Cas9 wiąże krótki fragment RNA przewodnika, który kieruje je do dopasowanej sekwencji DNA w genomie. Gdy Cas9 znajdzie cel, RNA przewodnika paruje się z jedną nićmi DNA, rozdzielając dwie nici i tworząc hybrydowy obszar DNA–RNA zwany pętlą R. W swojej klasycznej roli Cas9 następnie przecina obie nici DNA w tym miejscu. Jednak niedawne prace wykazały, że po takiej aktywacji domena tnąca RuvC może także rozcinać niezwiązane jednoniciowe DNA, np. odcinki pol(T), gdzie indziej w roztworze. Autorzy postawili pytanie: które dokładne cechy geometryczne i strukturalne docelowego DNA i RNA przewodnika sprawiają, że aktywność kolateralna jest silna, słaba lub nieobecna?
Krótki kontra długi cel: dawanie Cas9 miejsca do poruszania się
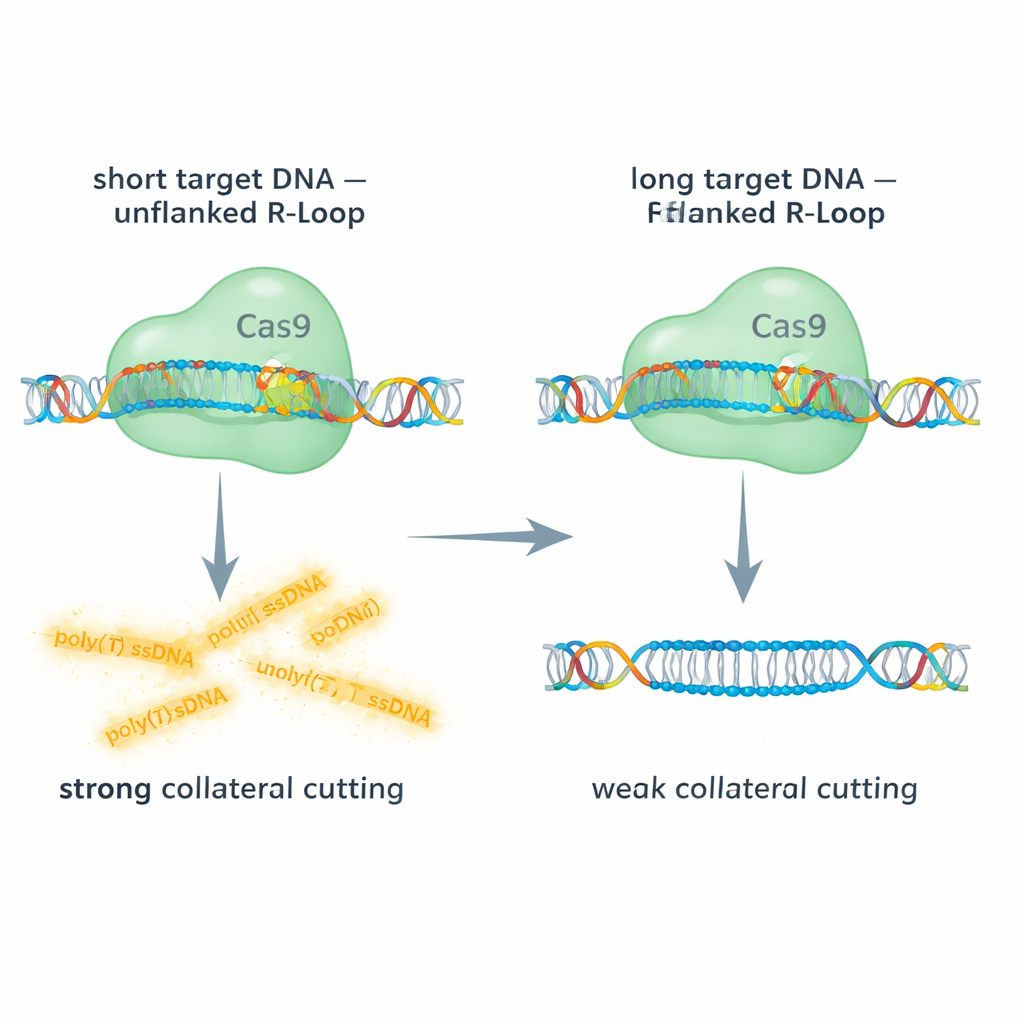
Zespół porównał działanie Cas9 na krótkich i długich dwuniciowych celach DNA, używając fluorescencyjnych odczytów do śledzenia zarówno cięcia na miejscu, jak i kolateralnego cięcia sondy jednoniciowego DNA. Przy krótkich celach DNA pętla R przy 5′ końcu RNA przewodnika jest „nieotoczona” — nie ma dodatkowego dwuniciowego DNA kontynuującego poza obszarem hybrydowym. W tych warunkach Cas9 wykazywał silną aktywność kolateralną wobec jednoniciowego DNA. W przeciwieństwie do tego, gdy użyto dłuższych fragmentów DNA, które pozostawiały dodatkowe dwuniciowe DNA otaczające pętlę R, kolateralne cięcie spadało dramatycznie, czasem o około 90%, mimo że główne cięcie na miejscu nadal zachodziło. Celowanie w długie jednoniciowe DNA, co usuwa pętlę R całkowicie, w dużej mierze przywracało aktywność kolateralną. Te porównania pokazują, że dwuniciowa „czapka” przylegająca do pętli R usztywnia kompleks i fizycznie utrudnia dostęp lub elastyczność potrzebną domenie RuvC do rozcinania innych nici.
Dostrajanie długością przewodnika i niedopasowaniami
Naukowcy zbadali następnie, jak sam RNA przewodnika reguluje to zachowanie. Wprowadzili drobne niedopasowania między przewodnikiem a docelowym DNA i śledzili, jak dobrze Cas9 nadal tnie. Główne cięcie na miejscu tolerowało wiele niedopasowań pojedynczych zasad, ale cięcie kolateralne było bardziej kruche i silnie zależało od dokładnego położenia niedopasowania, co podkreśla jego wrażliwość. Następnie systematycznie wydłużali spacer RNA przewodnika poza zwyczajowe 20 nukleotydów. Mimo że Cas9 nadal mógł wiązać i ciąć DNA docelowe, aktywność kolateralna spadała niemal liniowo wraz ze wzrostem długości spaceru: dodanie zaledwie dwóch dodatkowych zasad zmniejszało aktywność kolateralną mniej więcej o połowę, a cztery dodatkowe zasady redukowały ją jeszcze bardziej. W praktycznych testach z materiałem genetycznym SARS-CoV-2 tylko amplicony DNA zaprojektowane tak, by tworzyć nieotoczoną pętlę R z przewodnikiem o standardowej długości, dawały silny sygnał kolateralny, co podkreśla, jak projekt primerów i przewodnika może zadecydować o skuteczności testów opartych na CRISPR.
Istotna pomocnicza domena w tle
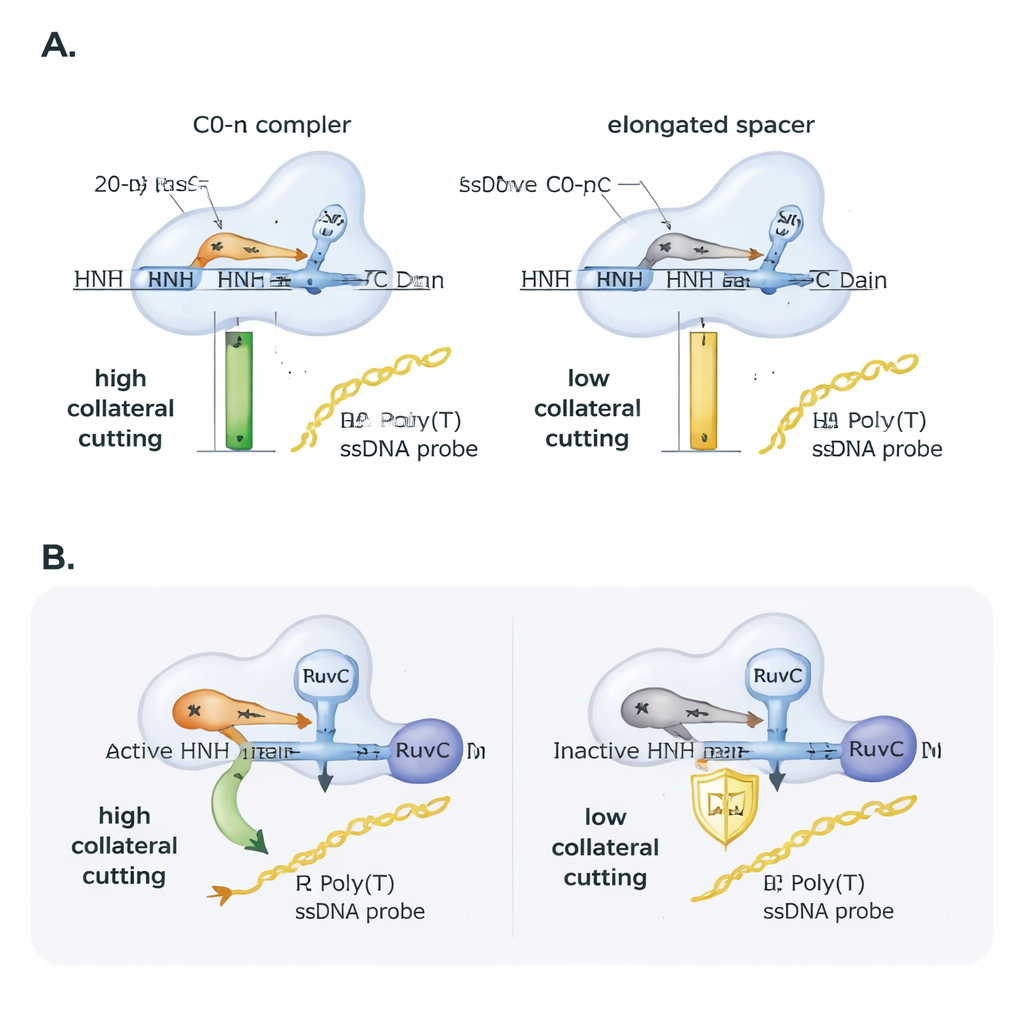
Cas9 ma dwie domeny tnące, RuvC i HNH. Wcześniejsze prace wiązały kolateralne cięcie bezpośrednio z RuvC, ale to badanie pokazuje, że HNH też ma znaczenie. Gdy autorzy użyli wariantu Cas9 z nieaktywną domeną HNH, aktywność kolateralna gwałtownie spadła, mimo że wiązanie celu i zachowanie związane z nacinaniem pozostały. Co ciekawe, jeśli dostarczono Cas9 cel DNA, który był już nacięty na jednej nici, wersja z nieaktywnym HNH odzyskiwała aktywność kolateralną podobną do normalnego enzymu. Sugeruje to, że rola HNH jest częściowo mechaniczna: poprzez przecięcie lub poluzowanie celowanej nici pomaga białku osiągnąć kształt, który odsłania RuvC na pobliskie jednoniciowe DNA. Analizy strukturalne istniejących modeli 3D wspierały ten pogląd, pokazując że nieotoczone pętle R i przewodniki o standardowej długości pozwalają 5′ końcowi RNA „przylegać” do Cas9 i korzystnie ustawiać regiony katalityczne, podczas gdy otoczone pętle R i wydłużone przewodniki upakowują białko bardziej ciasno i prawdopodobnie osłaniają miejsce RuvC przed przypadkowymi nićmi.
Co to oznacza dla przyszłych narzędzi
Dla osób niebędących specjalistami główny przekaz jest taki, że zachowanie Cas9 nie jest zero-jedynkowe: drobne detale geometryczne — jak daleko rozciąga się DNA, jak długi jest przewodnik i czy pomocnicza domena ukończy swoje cięcie — decydują, czy enzym trzyma się głównego zadania, czy też rozdrabnia pobliskie jednoniciowe nici. Krótkie cele pozostawiające pętlę R nieotoczoną, standardowe 20-nt przewodniki i aktywna domena HNH wspólnie sprzyjają silnemu cięciu kolateralnemu; długie otaczające DNA, wydłużone przewodniki lub nieaktywna domena HNH je tłumią. Te spostrzeżenia dają badaczom bardziej precyzyjne narzędzie do regulacji Cas9, pomagając w projektowaniu bezpieczniejszych systemów edycji genów, które unikają niepożądanych szkód ubocznych, lub potężniejszych testów diagnostycznych, które celowo wykorzystują aktywność kolateralną do wykrywania śladowych ilości materiału wirusowego lub genetycznego.
Cytowanie: Montagud-Martínez, R., Ruiz, R., Baldanta, S. et al. CRISPR-Cas9 trans-cleavage is hindered by a flanked R-loop, an elongated spacer, and an inactive HNH domain. Nat Commun 17, 1998 (2026). https://doi.org/10.1038/s41467-026-68789-3
Słowa kluczowe: CRISPR-Cas9, kolateralne cięcie, pętla R, spacer RNA przewodnika, diagnostyka kwasów nukleinowych