Clear Sky Science · pl
NatA angażuje się w kompleksy wieloskładnikowe przy wyjściu tunelu polipeptydowego rybosomu
Jak komórki dopracowują nowe białka w chwili ich powstawania
Każdej sekundy Twoje komórki wytwarzają tysiące nowych białek na maleńkich maszynach zwanych rybosomami. Gdy łańcuch białkowy się wydostaje, musi zostać przycięty, oznakowany i poprawnie złożony, inaczej może działać nieprawidłowo i przyczyniać się do chorób. W tym badaniu przyjrzano się jednemu z kluczowych systemów znakowania, modyfikacji zwanej acetylacją N-końca, i pokazano, jak centralny kompleks enzymatyczny NatA współdziała z kilkoma partnerami właśnie tam, gdzie nowe białka wychodzą z rybosomu. Zrozumienie tej choreografii pomaga wyjaśnić, jak komórki utrzymują sprawne funkcjonowanie swoich fabryk białek.
Mały chemiczny znacznik, który ma znaczenie
Większość białek zaczyna życie od tego samego pierwszego elementu budulcowego, aminokwasu metioniny. Często ta początkowa metionina jest usuwana i zastępowana małym chemicznym znacznikiem zwanym grupą acetylową. Ten znacznik, dodawany na sam czubek białka (jego N-terminus), może wpływać na długość życia białka, jego lokalizację w komórce i funkcję. Dwa główne typy enzymów stacjonują przy wyjściu tunelu rybosomu, aby zarządzać tym pierwszym przeróbką: aminopeptydazy metioninowe (MAP), które usuwają początkową metioninę, oraz N-terminalne acetylotransferazy (NAT), które dodają grupę acetylową. Spośród NAT-ów NatA jest kluczowym graczem w komórkach ludzkich, potencjalnie modyfikującym niemal 40% wszystkich białek. Ponieważ wiele białek jest wytwarzanych jednocześnie, komórka musi zorganizować te enzymy tak, aby przycinanie i znakowanie zachodziły szybko i we właściwej kolejności.
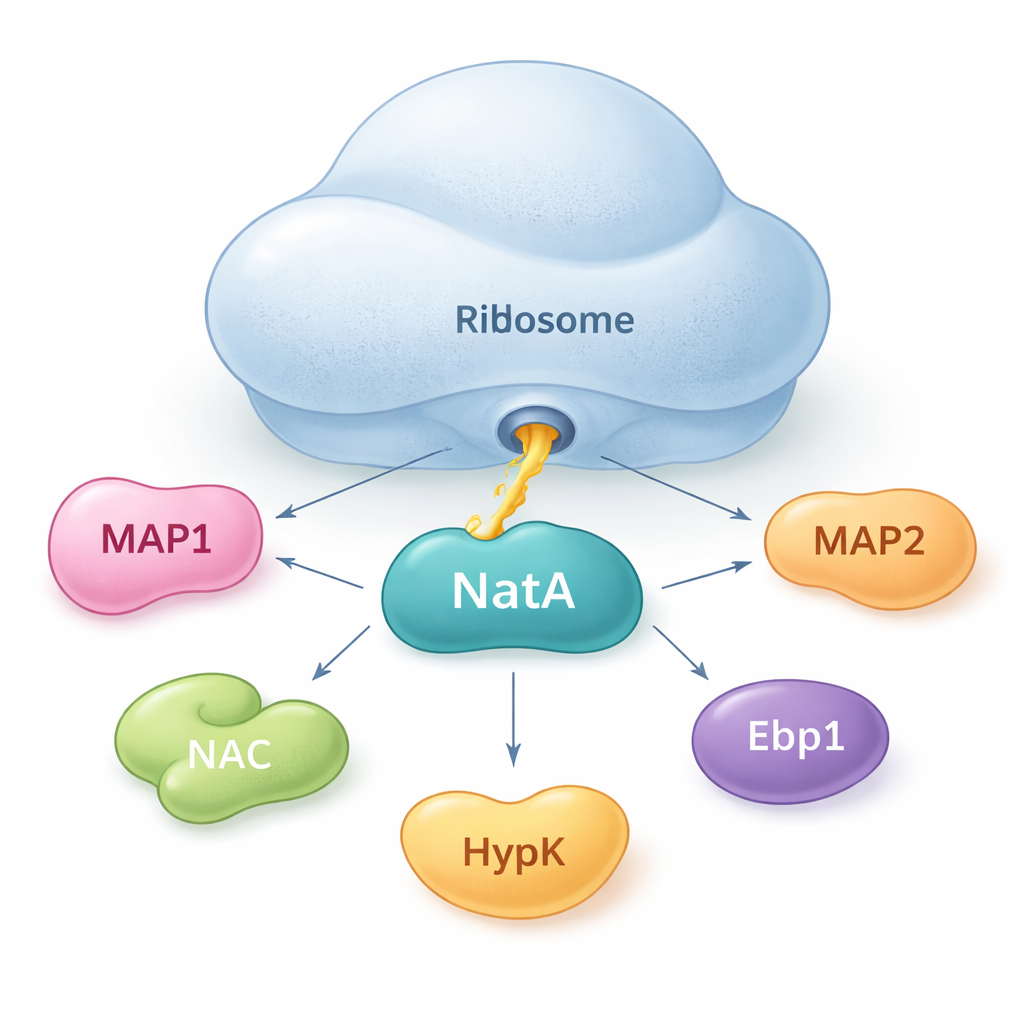
NatA jako punkt spotkań dla pomocników białkowych
Autorzy pokazują, że NatA nie działa w pojedynkę. Zamiast tego zachowuje się jak węzeł, który gromadzi wiele białek pomocniczych, zarówno związanych z rybosomem, jak i wolnych w roztworze. Dzięki czułym pomiarom wiązania w roztworze wykazali, że NatA może tworzyć zwarte kompleksy z MAP1, kompleksem związanym z nowo powstającymi polipeptydami (NAC), białkiem regulatorowym HypK oraz innym enzymem, Naa50, nawet bez obecności rybosomu. NAC może pośredniczyć między NatA a MAP1, pozwalając na połączenie kroków przycinania i acetylacji w jednym zespole. Jednak HypK, które zazwyczaj tłumi aktywność NatA, może blokować wiązanie NAC. Sugeruje to, że komórki mogą przełączać NatA między stanem bardziej aktywnym, powiązanym z NAC, a powściągliwym stanem związanym z HypK, w zależności od potrzeb.
Drugie miejsce dokowania tuż przy wyjściu tunelu
Wykorzystując krioelektronową mikroskopię, technikę obrazowania dużych cząsteczek w niemal atomowych detalach, badacze odkryli, że NatA może wiązać się z rybosomem w dwóch odmiennych pozycjach. Jedno miejsce, wcześniej znane, leży nieco z dala od wyjścia tunelu. Nowo odkryte miejsce „proksymalne” umieszcza centrum katalityczne NatA bardzo blisko miejsca, z którego wydostaje się rosnący łańcuch białkowy, skracając dystans, jaki łańcuch musi przebyć, aby zostać zmodyfikowany. Co intrygujące, obie pozycje mogą być zajęte jednocześnie, co oznacza, że dwa kompleksy NatA mogą siedzieć na tym samym rybosomie. Bardziej oddalona kopia działa jako rusztowanie i kotwica, podczas gdy kopia proksymalna jest optymalnie ustawiona do znakowania nowych białek. Dwa cząsteczki NatA stykają się także ze sobą, co wskazuje, że NatA może koordynować własne duplikaty w wieloenzymowe zespoły.
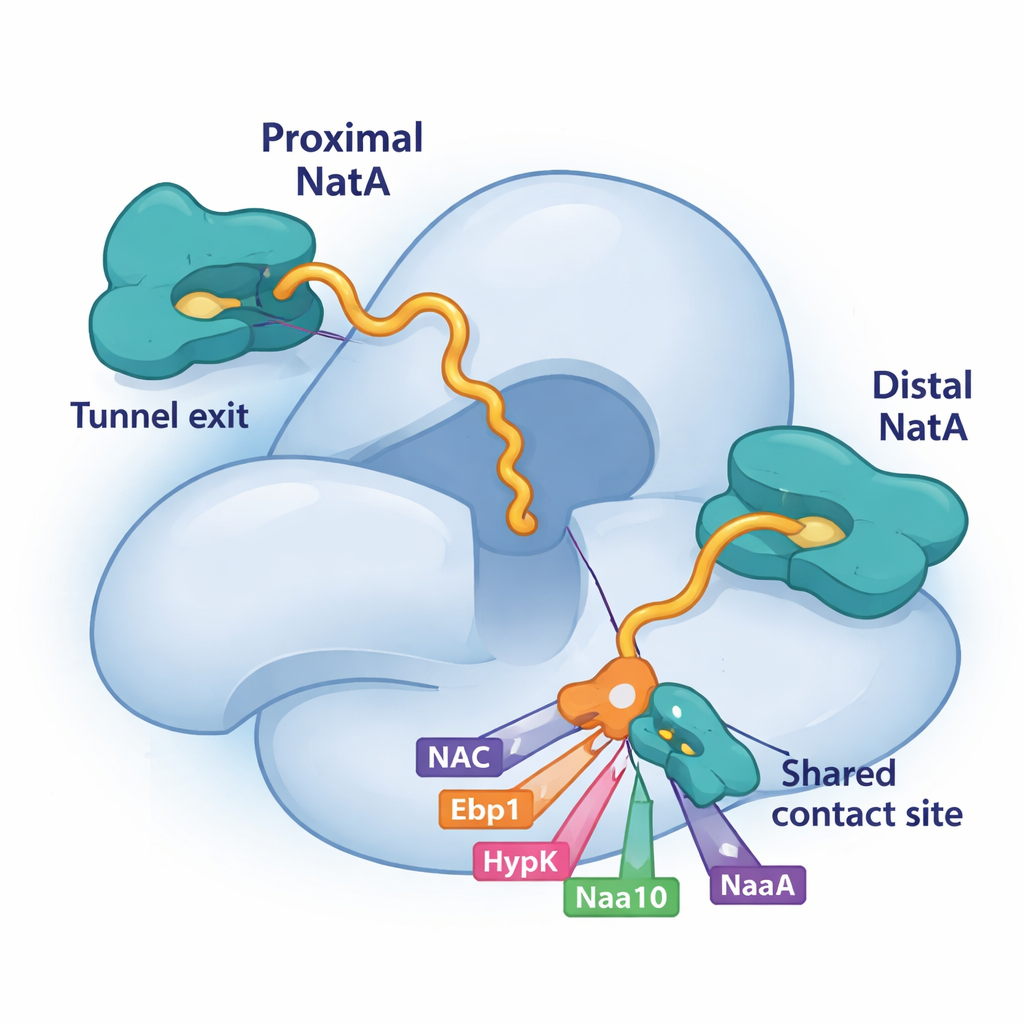
Rywalizacja o wspólne miejsce lądowania na NatA
Kluczowym elementem tej układanki jest mała szczelina na dużej podjednostce NatA, Naa15. Badanie pokazuje, że cztery różne czynniki związane z rybosomem — NAC, HypK, Ebp1, a nawet fragment ogonowy własnej podjednostki katalitycznej NatA, Naa10 — wykorzystują krótkie helisy, aby zaczepić się dokładnie na tej samej płaszczyźnie Naa15. Ponieważ wszystkie polegają na tym wspólnym miejscu lądowania, muszą ze sobą konkurować o dostęp. Gdy HypK zajmuje to miejsce, nie tylko wycisza aktywność NatA, ale także uniemożliwia parowanie NatA z NAC lub tworzenie dimerów NatA–NatA. Gdy natomiast wiążą się tam NAC, pseudoenzym Ebp1 lub proksymalny Naa10, mogą one przebudować pozycję NatA lub jego połączenia przy rybosomie. Ta konkurencyjna interakcja daje komórce elastyczny sposób wyboru, którzy partnerzy zgromadzą się wokół NatA w danym momencie.
Pseudoenzym jako kontroler ruchu
Białko Ebp1 jest szczególnie intrygujące. Przypomina jedno z enzymów usuwających metioninę, ale brak mu aktywności katalitycznej; jest „pseudoenzymem”. Wcześniejsze prace wykazały, że Ebp1 może siedzieć na rybosomie w pobliżu wyjścia tunelu i zaciskać długi odcinek RNA. W tym badaniu autorzy stwierdzają, że gdy NatA przyłącza się do rybosomu, Ebp1 zmienia pozycję, puszcza RNA i zamiast tego używa własnej helisy, aby zająć to samo miejsce wiązania na Naa15, które wykorzystują NAC i HypK. Ta reorganizacja sugeruje, że Ebp1 może działać jako zastępca lub organizator: może kształtować lokalne środowisko RNA, a następnie przekazywać kontrolę aktywnym enzymom, takim jak MAPy i NatA, nie wykonując przy tym bezpośrednio reakcji chemicznej.
Dlaczego ta molekularna kontrola tłumu ma znaczenie
Dla osoby niezajmującej się tematem detale helis i miejsc wiązania mogą brzmieć abstrakcyjnie, ale przekaz jest prosty: komórki prowadzą wysoce zaaranżowany, wieloetapowy system kontroli jakości dokładnie tam, gdzie powstają białka. NatA znajduje się w centrum tego systemu, zdolna do rekrutowania lub uwalniania różnych partnerów w zależności od tego, które czynniki uzyskają dostęp do kluczowej płaszczyzny dokującej i które miejsce na rybosomie NatA zajmuje. Ta elastyczna sieć pomaga zapewnić, że przycinanie i acetylacja zachodzą we właściwym czasie i w odpowiedniej kolejności dla tysięcy różnych białek. Ponieważ błędy w przetwarzaniu N-końca są powiązane z zaburzeniami rozwojowymi, neurodegeneracją i rakiem, opisanie, jak NatA i jego partnerzy się składają, daje badaczom wyraźniejszą mapę tego, jak kontrolowana jest wczesna obróbka białek — i jak można by ją ukierunkować, gdyby zaszła awaria.
Cytowanie: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
Słowa kluczowe: kontrola jakości białek, acetylacja N-końca, wyjście tunelu rybosomalnego, kompleks NatA, modyfikacja kotranslacyjna