Clear Sky Science · pl
Roślinna futuzylo-transferaza FUT11 odkształca akceptor cukrowy, katalizując reakcję przez przejściowy mechanizm z pośrednikiem oksokarbokationowym
Jak rośliny dopracowują cukrowe modyfikacje swoich białek
Białka w naszych komórkach, podobnie jak w komórkach roślinnych, często są ozdobione złożonymi łańcuchami cukrów, które pełnią rolę kodów kreskowych — kierują tym, jak białka się fałdują, jak długo utrzymują stabilność i z jakimi partnerami mogą wchodzić w interakcje. W tym badaniu skupiono się na roślinnym enzymie o nazwie FUT11, który dokłada małą cząsteczkę cukru, fukozę, do tych łańcuchów. Odkrywając dokładnie, jak FUT11 działa na poziomie atomowym, autorzy ujawniają zaskakujący trik: enzym chwilowo wygina swój akceptor cukrowy, wypychając go ze stanu równowagi, aby umożliwić trudny krok chemiczny. Zrozumienie tego procesu ma znaczenie nie tylko dla biologii podstawowej, lecz także dla projektowania bezpieczniejszych leków produkowanych w roślinach, które nie wywołują niepożądanych reakcji immunologicznych u ludzi.
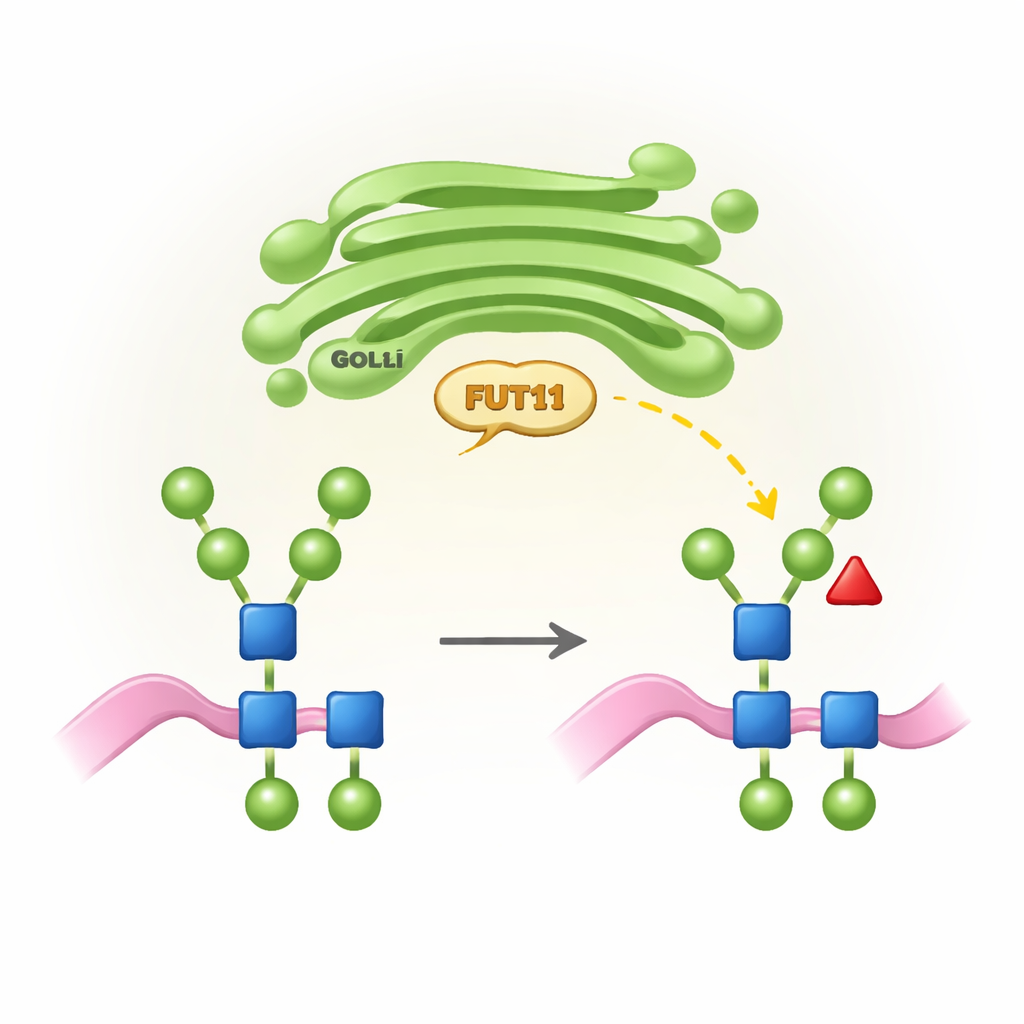
Roślinne znaczniki cukrowe i dlaczego są ważne
Wszystkie organizmy wyższe wykorzystują proces zwany N-glikozylacją do przyłączania łańcuchów cukrowych (N-glikanów) w określonych miejscach na białkach. U zwierząt łańcuchy te są przekształcane w aparacie Golgiego w złożone struktury, które często kończą się kwasem sjalowym i niosą rdzeniową fukozę w określonej pozycji. Rośliny jednak stosują inną „zasadę projektowania”: ich N-glikany zwykle nie zawierają kwasu sjalowego, ale niosą rdzeniową fukozę w innej pozycji (określanej jako β1,3) oraz dodatkową cząsteczkę ksylozy. Te roślinne cechy są niezbędne dla prawidłowego wzrostu i płodności, lecz mogą być rozpoznawane jako obce przez układ immunologiczny człowieka. FUT11 jest jednym z kluczowych enzymów w roślinach instalujących tę rdzeniową fukozę, a jego aktywność kształtuje zarówno rozwój roślin, jak i sposób, w jaki białka produkowane w roślinach będą postrzegane w organizmach ludzkich.
Mapowanie miejsc, w których FUT11 może działać na rozgałęzionych cukrach
Aby zrozumieć, co rozpoznaje FUT11, badacze przetestowali enzym na mikroarrayu zawierającym 144 różnych struktur N-glikanów. Stwierdzili, że FUT11 jest dość selektywny względem jednej gałęzi „drzewa cukrowego” — tak zwanej gałęzi β1,3 — która musi nieść określony fragment budulcowy (końcowy N-acetyloglukozamin, GlcNAc), aby reakcja zaszła. Jednocześnie FUT11 jest tolerancyjny wobec innych dekoracji: działa nadal, gdy centralna mannoza niesie roślinnej pochodzenia ksylozę, a nawet gdy inna fukoza została już przyłączona w pozycji typowej dla ssaków. Przeciwna gałąź (β1,6) jest w większości wystawiona na rozpuszczalnik i tworzy jedynie słabe kontakty z enzymem, co wyjaśnia, dlaczego FUT11 może akceptować szeroką gamę modyfikacji w tym miejscu. Te preferencje wiązania pomagają wyjaśnić, dlaczego rośliny wytwarzają charakterystyczny zestaw struktur N-glikanów i pokazują, jak FUT11 można wykorzystać lub omijać przy inżynierii komórek roślinnych do zastosowań biotechnologicznych.
Unikatowa struktura do chwytania i ustawiania cukrów
Dzięki krystalografii rentgenowskiej zespół rozwiązał trójwymiarową strukturę FUT11 w kompleksie z dawcą cukru (GDP-fukozą) oraz akceptorem N-glikanu. Enzym ma dwuzatokową architekturę typu „GT-B”: jedna zatoka mieści GDP-fukozę, podczas gdy nietypowo rozbudowana zatoka akceptora, z roślinną, N-terminalną poddomeną, oplata N-glikan. Ta dodatkowa poddomena, połączona z resztą enzymu mostkami dwusiarczkowymi, zakotwicza środkową część glikanu i pomaga ustawić reaktywną jednostkę GlcNAc w kierunku darczyńcy. Mutacje kluczowych aminokwasów potwierdziły ich role: zmiana pojedynczego glutaminianu (Glu158) likwidowała aktywność, podczas gdy modyfikacja dwóch pobliskich reszt osłabiła futuzylowanie w zmodyfikowanych komórkach ludzkich. Wyniki te łączą obraz strukturalny z funkcją w komórce, pokazując dokładnie, które części białka są niezbędne do wiązania i katalizy.
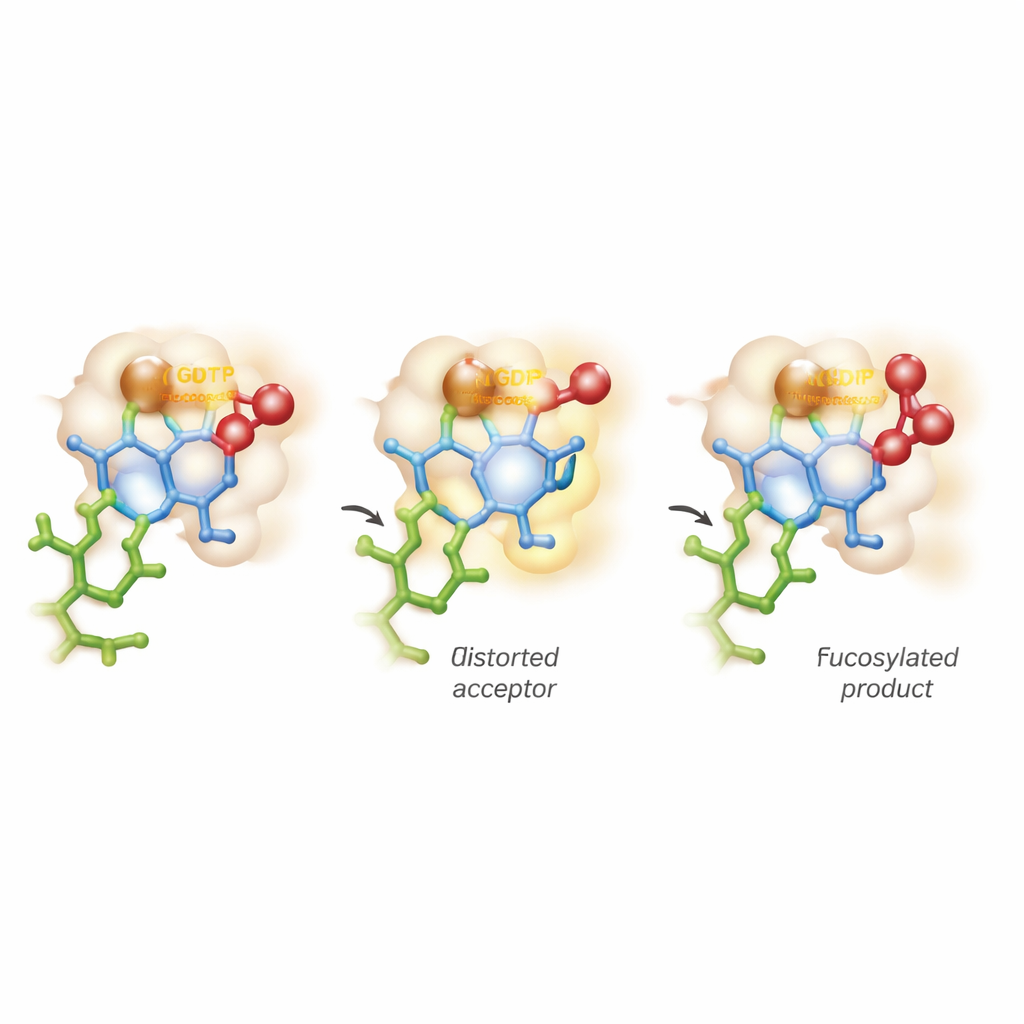
Wyginanie cukru i balansowanie między dwiema ścieżkami reakcji
Najbardziej uderzające spostrzeżenie pochodzi z zaawansowanych symulacji komputerowych łączących mechanikę kwantową z dynamiką molekularną. Tradycyjne poglądy zakładają, że akceptor cukrowy zachowuje stabilny, krzesełkowy kształt, podczas gdy enzym jedynie aktywuje dawcę. Tutaj FUT11 zachowuje się bardziej agresywnie: oddziaływania napędzane przez Glu158 tymczasowo odkształcają wewnętrzny pierścień GlcNAc do mniej wygodnej, spuckowanej formy. W tym naprężonym ustawieniu krytyczna grupa hydroksylowa jest idealnie wyrównana do ataku na darczyńcę fukozy. Obliczenia wykazują, że w miarę jak wiązanie z GDP pęka, na cukrze pojawia się krótkotrwały, dodatnio naładowany stan przypominający oksokarbokation, zanim nowe wiązanie do akceptora zostanie w pełni uformowane. Oznacza to, że reakcja nie mieści się dokładnie w podręcznikowych kategoriach SN1 lub SN2, lecz przebiega wzdłuż kontinuum, w sposób asynchroniczny, niemal schodkowy.
Ukryta elastyczność i echo ewolucji
Porównując FUT11 z pokrewnym enzymem ludzkim, FUT9, autorzy odkryli, że enzym roślinny może również, choć słabo, modyfikować inny typ motywu cukrowego (LacNAc), tworząc strukturę znaną jako Lewis X. Ta aktywność uboczna prawdopodobnie nie ma znaczenia biologicznego w roślinach, gdzie Lewis X nie występuje zwykle, lecz podkreśla, jak podobne rusztowania białkowe mogą być przekształcane w toku ewolucji do działania w różnych kontekstach cukrowych. Badanie sugeruje, że FUT11 i jego krewni dzielą modułowy schemat rozpoznawania N-glikanów, z subtelnymi modyfikacjami przesuwającymi specyficzność między roślinnymi rdzeniami a zwierzęcymi antenami.
Dlaczego ten trik wyginania ma znaczenie dla nauki i medycyny
Podsumowując, praca pokazuje, że FUT11 robi więcej niż tylko zbliża dwóch cukrowych partnerów: aktywnie wygina akceptor, ustawiając go w reaktywnej pozycji, i kieruje chemię przez ulotny, naładowany pośrednik. Dla czytelnika niebędącego specjalistą oznacza to, że cukier na białku nie jest sztywnym miejscem dokującym, lecz elastycznym uczestnikiem, którego enzym modeluje wedle potrzeby. Ten nowy obraz „katalizy konformacyjnej” pomaga wyjaśnić, jak enzymy osiągają zarówno szybkość, jak i selektywność, oraz daje plan do przeprojektowania ścieżek glikozylacji. W praktyce, dokładna wiedza o tym, jak FUT11 rozpoznaje i modyfikuje roślinne N-glikany, może kierować inżynierią roślin uprawnych i systemów produkcji opartych na roślinach, aby zminimalizować immunogenne wzorce cukrowe w terapiach dla ludzi lub tworzyć projektowane glikoproteiny o dobranych właściwościach biologicznych.
Cytowanie: Taleb, V., Sanz-Martínez, I., Serna, S. et al. Plant fucosyltransferase FUT11 distorts the sugar acceptor to catalyze via a transient oxocarbenium intermediate mechanism. Nat Commun 17, 1960 (2026). https://doi.org/10.1038/s41467-026-68786-6
Słowa kluczowe: glikozylacja roślin, futuzylo-transferaza FUT11, N-glikany, mechanizm enzymatyczny, glycoengineering