Clear Sky Science · pl
Profilowanie proteomiczne łatek naprawczych po uszkodzeniach wywołanych UV ujawnia opiekunów histonów o kluczowej roli w naprawie chromatyny
Jak nasze komórki leczą szkody od światła słonecznego
Za każdym razem, gdy nasza skóra jest wystawiona na silne światło słoneczne, w DNA komórek powstają niewidoczne uszkodzenia. Jeśli pozostaną nie naprawione, te drobne blizny mogą się kumulować i przyczyniać do starzenia się oraz powstawania nowotworów. DNA nie funkcjonuje jednak samodzielnie; jest starannie owinięte wokół białek zwanych histonami, tworząc strukturę zwaną chromatyną, która pomaga definiować tożsamość każdej komórki. W badaniu postawiono pozornie proste, lecz istotne pytanie: gdy komórki naprawiają uszkodzenia wywołane UV w swoim DNA, w jaki sposób odbudowują tę złożoną architekturę chromatyny, aby zachować tożsamość komórkową zamiast ją zaburzyć?
Odkrywanie ukrytej strefy naprawczej
Aby odpowiedzieć na to pytanie, badacze musieli przyjrzeć się konkretnie miejscom w genomie, gdzie naprawa aktywnie zachodzi, zamiast analizować cały jądrowy materiał jednocześnie. Opracowali podejście nazwane IPOND-R, które chemicznie znakowało krótkie odcinki świeżo syntetyzowanego DNA powstającego podczas naprawy, a nie w trakcie zwykłego replikowania genomu. Wyłapując te oznakowane „łatki naprawcze” DNA wraz ze wszystkimi białkami do nich przyłączonymi, a następnie identyfikując te białka za pomocą wysokorozdzielczej spektrometrii mas, stworzyli katalog obecnych tam białek z rozdzielczością czasową — kto się pojawia i kiedy w odpowiedzi na uszkodzenia UV w komórkach ludzkich. Zapewniło to nieobciążone spojrzenie na wyspecjalizowane białkowe sąsiedztwo tworzące się bezpośrednio w miejscach naprawy.
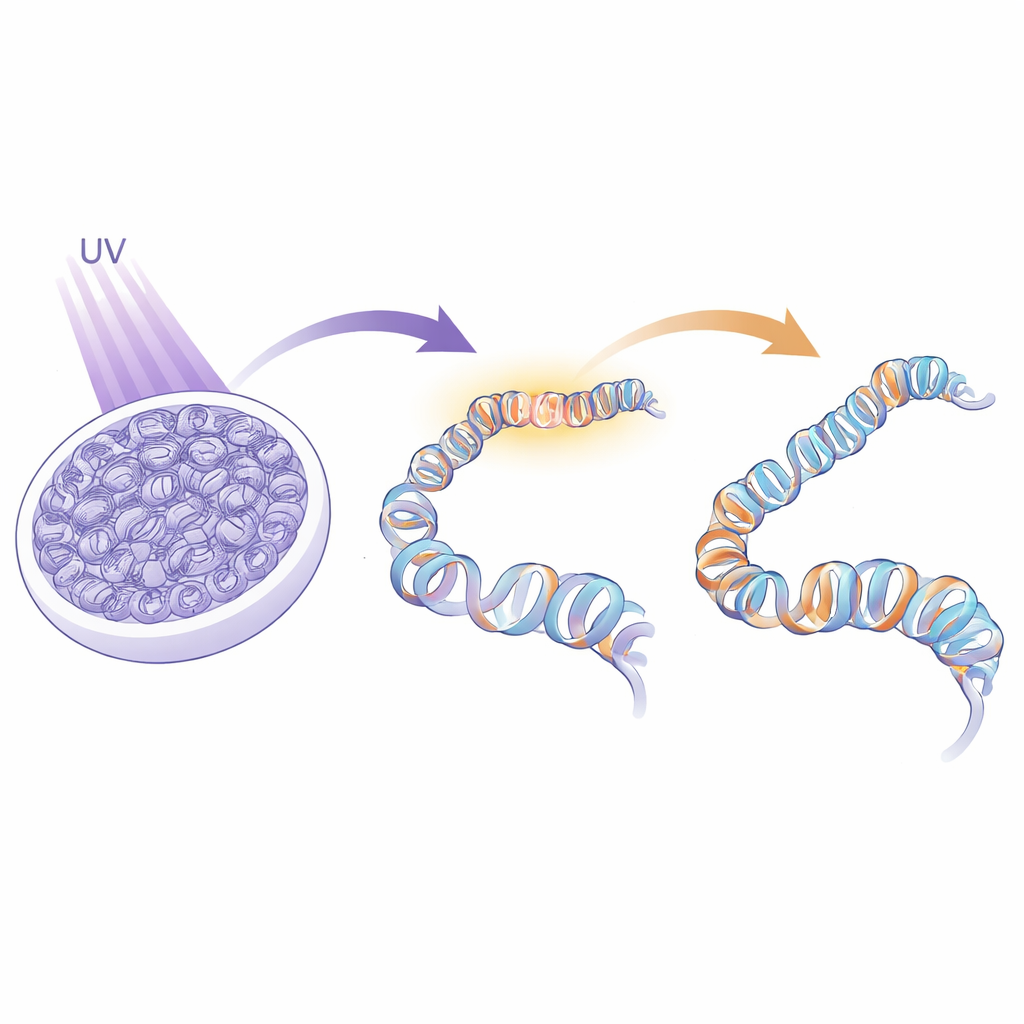
Gęsty tłum na rusztowaniu naprawczym
Metoda IPOND-R ujawniła setki białek wzbogaconych na DNA poddawanym naprawie wkrótce po ekspozycji na UV. Zgodnie z oczekiwaniami obecne były dobrze znane czynniki naprawy DNA, które rozpoznają i wycinają zmiany wywołane UV. Jednak zestaw danych poszedł dalej, obejmując białka zaangażowane w regulację genów, architekturę jądra i, co kluczowe, organizację chromatyny. Wielu z tych gości było opiekunami histonów — wyspecjalizowanymi białkami towarzyszącymi histonom podczas ich zdejmowania i odkładania na DNA. Porównanie wczesnych i późnych punktów czasowych wykazało, że większość tych opiekunów pojawia się jedynie przejściowo, co sugeruje starannie zaaranżowaną sekwencję dezintegracji i ponownej montażu chromatyny ściśle powiązaną z procesem naprawy DNA.
Nowi dostawcy i recyklerzy histonów
Wśród białek wzbogaconych na łatkach naprawczych wyróżniły się dwa opiekuny histonów: DNAJC9 i MCM2. Czynniki te były wcześniej znane głównie z ról przy widełkach replikacyjnych DNA, gdzie genom jest kopiowany, ale nie powiązano ich wcześniej z naprawą uszkodzeń wywołanych UV. W niniejszym badaniu zespół wykazał, że DNAJC9 jest centralnym dostawcą świeżych jednostek histonowych (konkretnie par H3–H4) podczas naprawy. Korzystając z fluorescencyjnych znaczników rozróżniających nowe histony od starych, wykazano, że obniżenie poziomu DNAJC9 mocno osłabia napływ nowo wytworzonych wariantów histonów do miejsc uszkodzonych przez UV, przy jednoczesnym zachowaniu podstawowych etapów naprawy DNA. DNAJC9 działa przed znanymi chaperonami deponującymi histony, takimi jak CAF-1 i HIRA, dostarczając im nowe histony, bez zmiany ich obecności w miejscach uszkodzeń.
Równoważenie starych i nowych składników
Naprawa chromatyny to nie tylko wstawianie nowych elementów. Oryginalne histony niosą także modyfikacje chemiczne przechowujące informacje epigenetyczne — sygnały, które mówią komórce, które geny mają być aktywne, a które wyciszone. Badanie pokazuje, że DNAJC9 pomaga również przywrócić rodzicielskie histony po tymczasowym odsunięciu ich od rejonów uszkodzonych. Gdy DNAJC9 został wyczerpany, stare histony nie wracały w pełni, a ogólna gęstość histonów w miejscach naprawy spadła. Badacze odkryli następnie, że DNAJC9 współpracuje z MCM2, aby skoordynować tę delikatną równowagę: oba białka są wymagane do efektywnego recyklingu starych histonów oraz prawidłowego lokowania nowych, nawet w komórkach, które nie replikują aktywnie DNA. Wskazuje to na funkcję niezależną od replikacji dla MCM2 i ustanawia funkcjonalne partnerstwo między obydwoma opiekunami w miejscach naprawy.
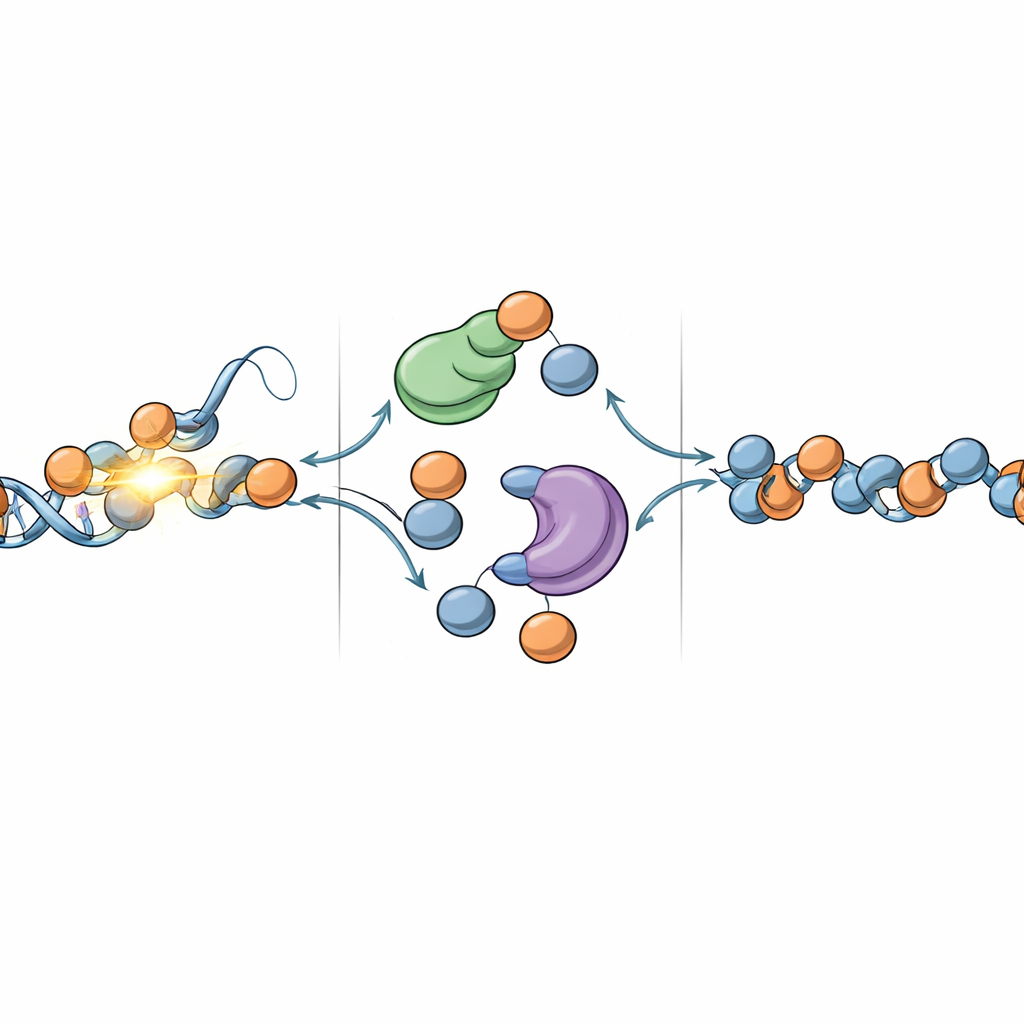
Dlaczego ma to znaczenie dla tożsamości komórek i chorób
Praca przedstawia obraz naprawy chromatyny jako operacji o dwóch stronach: uszkodzone DNA jest naprawiane, podczas gdy otaczający krajobraz histonowy jest odbudowywany z mieszanki elementów ponownie użytych i świeżo dostarczonych. DNAJC9 i MCM2 zajmują w tym procesie kluczowe miejsce, koordynując przepływ starych i nowych histonów, tak aby po uszkodzeniu UV komórki mogły przywrócić nie tylko kod genetyczny, ale także wzorce epigenetyczne definiujące ich tożsamość. Ponieważ podobne wyzwania pojawiają się przy wielu typach uszkodzeń DNA, ta koncepcja tworzy podstawę do zrozumienia, jak komórki utrzymują stabilny epigenom pod wpływem stresu — kwestii istotnej dla starzenia, raka i innych chorób związanych z zaburzeniami regulacji chromatyny.
Cytowanie: Plessier, A., Chansard, A., Petit, E. et al. Proteomic profiling of UV damage repair patches uncovers histone chaperones with central functions in chromatin repair. Nat Commun 17, 2127 (2026). https://doi.org/10.1038/s41467-026-68781-x
Słowa kluczowe: naprawa uszkodzeń DNA, chromatyna, opiekunowie histonów, promieniowanie UV, stabilność epigenomu