Clear Sky Science · pl
Podstawy strukturalne i patologiczne implikacje dimerowego rdzeniowego kompleksu ERAD OS9-SEL1L-HRD1
Komórkowa ekipa sprzątająca pod mikroskopem
W każdej z naszych komórek działa tłoczna fabryka przekształcająca instrukcje genetyczne w działające białka. Jak w każdej fabryce, zdarzają się błędy. Gdy białka fałdują się nieprawidłowo, mogą zatykać system i przyczyniać się do chorób. W badaniu tym przyjrzano się jednemu z głównych mechanizmów kontroli jakości komórki — kompleksowi SEL1L‑HRD1 — aby ujawnić jego szczegółową strukturę 3D i pokazać, jak drobne zmiany genetyczne mogą uszkodzić tę maszynerię i potencjalnie prowadzić do chorób u ludzi.
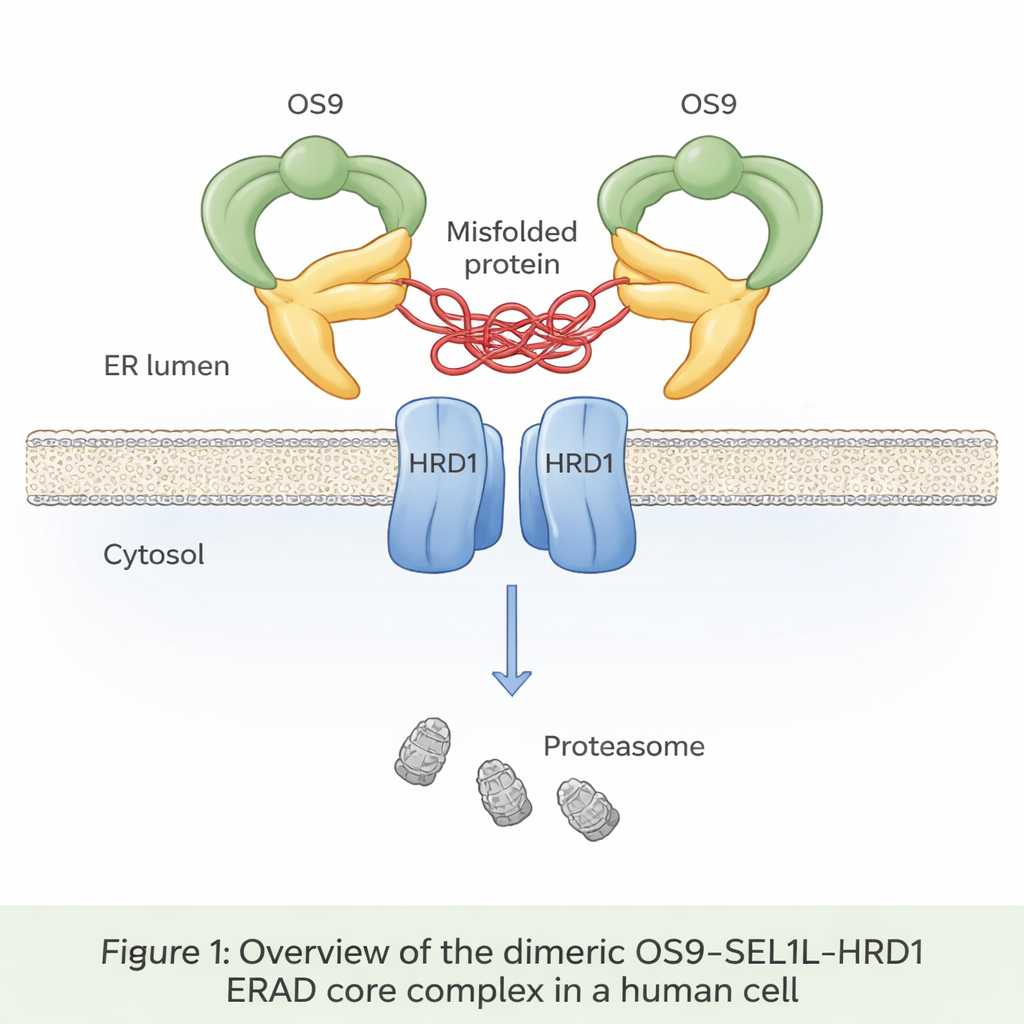
Ukryta taśma transportowa w komórce
Aż do jednej trzeciej wszystkich nowo powstałych białek trafia do przedziału zwanego retikulum endoplazmatycznym (ER), gdzie są fałdowane i sprawdzane. Białka fałdowane nieprawidłowo są zwykle rozpoznawane, wyciągane z ER i niszczone w procesie znanym jako degradacja związana z ER (ER‑associated degradation, ERAD). W sercu jednej z głównych ścieżek ERAD leży trio białek: OS9, SEL1L i HRD1. OS9 działa jako czujnik wadliwych, znakowanych cukrowo białek; SEL1L pełni rolę rusztowania; a HRD1 oznacza skazane białka małymi znacznikami ubiquitiny, kierując je do proteasomów — komórkowych jednostek utylizacji odpadów. Do tej pory nikt jednak nie widział w atomowych szczegółach, jak te trzy elementy współdziałają w komórkach ludzkich.
Ujawnienie kształtu rdzeniowej maszyny
Autorzy użyli krio‑elektronowej mikroskopii, techniki obrazowania zamrożonych błyskawicznie cząsteczek w rozdzielczości bliskiej atomowej, aby zobrazować oczyszczony z ludzkich komórek kompleks OS9‑SEL1L‑HRD1. Odkryli, że tworzy on dimer — zasadniczo dwie identyczne kopie połączone razem — zamiast występować jako oddzielne jednostki. Po stronie światła ER (wewnątrz ER) dwa cząsteczki OS9 i dwie SEL1L składają się w pierścień przypominający szczękę kraba z centralnym otworem, który najwyraźniej ma chwytać nieprawidłowo złożone białka. W obrębie samej błony dwie cząsteczki HRD1 łączą się w parę, tworząc wspólny kanał. To ułożenie umieszcza „szczękę” bezpośrednio nad drzwiami HRD1, tworząc ciągłą ścieżkę dla nieprawidłowych białek — od światła ER, przez błonę, w kierunku degradacji w cytosolu.
Jak drobne zmiany łamią duży system
Ponieważ mutacje w SEL1L i HRD1 wykryto u pacjentów z ciężkimi zaburzeniami rozwoju neurologicznego i innymi schorzeniami, zespół naniósł kilka wariantów związanych z chorobą na ich strukturę i przetestował, jak zachowują się w komórkach. Dwie mutacje SEL1L, G585D i S658P, znajdują się dokładnie w punktach kontaktu odpowiednio z OS9 i HRD1. W eksperymentach komórkowych G585D niemal zniszczyła zdolność SEL1L do wiązania OS9, podczas gdy S658P znacznie osłabiła jego interakcję z HRD1; połączenie obu mutacji praktycznie rozbija rdzeniowy kompleks, przy pozostawieniu innych partnerów nietkniętych. W rezultacie komórki miały trudności z oznaczaniem i usuwaniem zleżałego prekursora hormonu, co pozwalało wadliwym białkom utrzymywać się dłużej.
Mutacja chorobowa w kanałowej części błony
Struktura wykazała także, że trzeci segment transbłonowy HRD1 jest kluczowym interfejsem, gdzie dwie cząsteczki HRD1 stykają się, tworząc kanał. Naukowcy wprowadzili cysteinowe „uchwyty” w określonych pozycjach i użyli chemicznego sieciowania, aby potwierdzić, że te regiony stykają się w żywych komórkach, dowodząc, że HRD1 faktycznie dimeruje in vivo. Gdy zaburzyli pojedyncze, silnie konserwowane resztę (T93) w tym interfejsie, dimer rozpadł się, a aktywność ERAD zawaliła się, choć kompleks nadal łączył się z OS9 i SEL1L. Następnie przebadali nowo odkryty wariant u pacjenta, HRD1 A91D, znaleziony u dziecka z problemami sercowo‑oddechowymi. Ta zmiana, również w interfejsie dimeru, zmniejszyła dimeryzację HRD1 mniej więcej o połowę i poważnie upośledziła utylizację nieprawidłowych białek, znów bez zaburzania ogólnego wiązania partnerów.
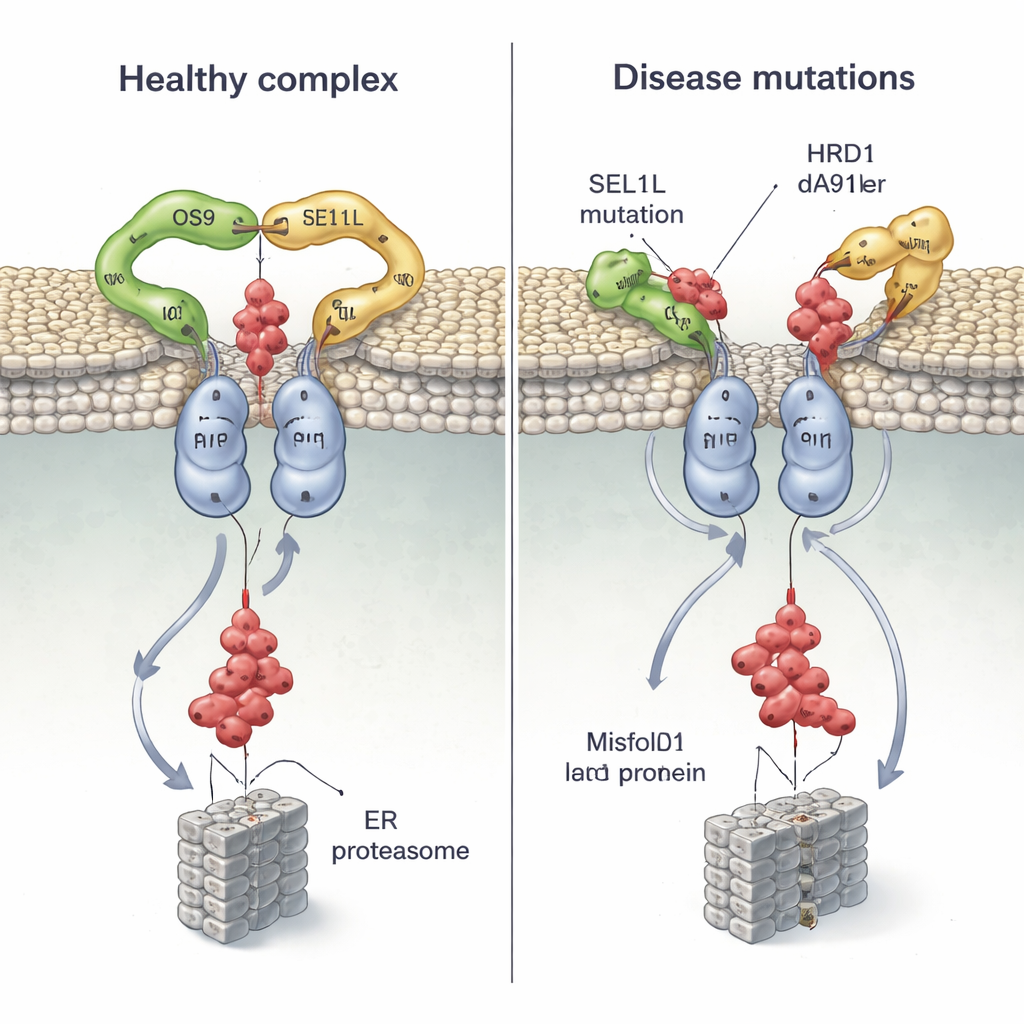
Nowe spojrzenie na kontrolę jakości białek i chorobę
Łącząc biologię strukturalną z testami komórkowymi, praca ta pokazuje, że kompleks OS9‑SEL1L‑HRD1 działa jako sparowana, dimerowa maszyna: chwytająca szczęka połączona ze wspólnym kanałem, który transportuje wadliwe białka poza ER. Mutacje, które rozluźniają uchwyt szczęki lub destabilizują parę HRD1, nie tylko nieznacznie obniżają wydajność — mogą skutecznie zablokować system, pozwalając na nagromadzenie uszkodzonych białek i przyczyniając się do chorób u ludzi. Dla osób niezwiązanych z dziedziną kluczowy wniosek jest taki, że nawet pojedyncze zmiany literowe w naszym DNA mogą subtelnie zdeformować kształt niezbędnych maszyn komórkowych, z dalekosiężnymi konsekwencjami dla rozwoju mózgu, odporności i funkcji narządów.
Cytowanie: Lin, L.L., Maldosevic, E., Zhou, L.E. et al. Structural basis and pathological implications of the dimeric OS9-SEL1L-HRD1 ERAD Core Complex. Nat Commun 17, 2064 (2026). https://doi.org/10.1038/s41467-026-68777-7
Słowa kluczowe: kontrola jakości białek, sito endoplazmatyczne, ERAD, kompleks SEL1L-HRD1, nieprawidłowe fałdowanie białek