Clear Sky Science · pl
Profilowanie delecji egzonów w pojedynczych komórkach ujawnia zdarzenia splicingu kształtujące ekspresję genów i dynamikę stanów komórkowych
Jak drobne zmiany w RNA mogą zmieniać zachowanie komórek
Nasze komórki nieustannie odczytują i składują instrukcje RNA, aby zdecydować, jakie białka produkować i jak reagować na stres, rosnąć czy dzielić się. W badaniu pokazano, że zmiana bardzo małych fragmentów tych komunikatów — pojedynczych segmentów zwanych egzonomami — może silnie przekształcić aktywność genów, a nawet przesunąć sposób, w jaki komórki przechodzą przez cykl komórkowy. Praca wprowadza potężne narzędzie pozwalające naukowcom przeszukać wiele takich drobnych wyborów splicingowych jednocześnie, komórka po komórce, otwierając nowe drogi do zrozumienia chorób i odkrywania celów terapeutycznych.
Wycinanie wybranych słów z genetycznego scenariusza
Geny zapisane są jako długie fragmenty DNA, lecz komórki nie czytają ich linearnie. Zamiast tego wycinają i sklejają mniejsze bloki, zwane egzonomami, aby zbudować cząstkę RNA. Poprzez wybór, które egzony zachować, komórki mogą wytwarzać wiele wersji białka z jednego genu, podobnie jak tworzenie różnych montaży filmu z tego samego materiału źródłowego. Wiele chorób, w tym rak i autyzm, wiąże się z błędami w tym procesie, jednak dla większości decyzji odnośnie ekzonów nadal nie wiemy, jakie mają rzeczywiste funkcje. Autorzy postawili sobie za cel zmienić ten stan rzeczy, budując system na dużą skalę, który potrafi usuwać określone egzony z wielu genów i następnie obserwować, w tysiącach pojedynczych komórek jednocześnie, jak te edycje wpływają na wewnętrzne okablowanie komórki.
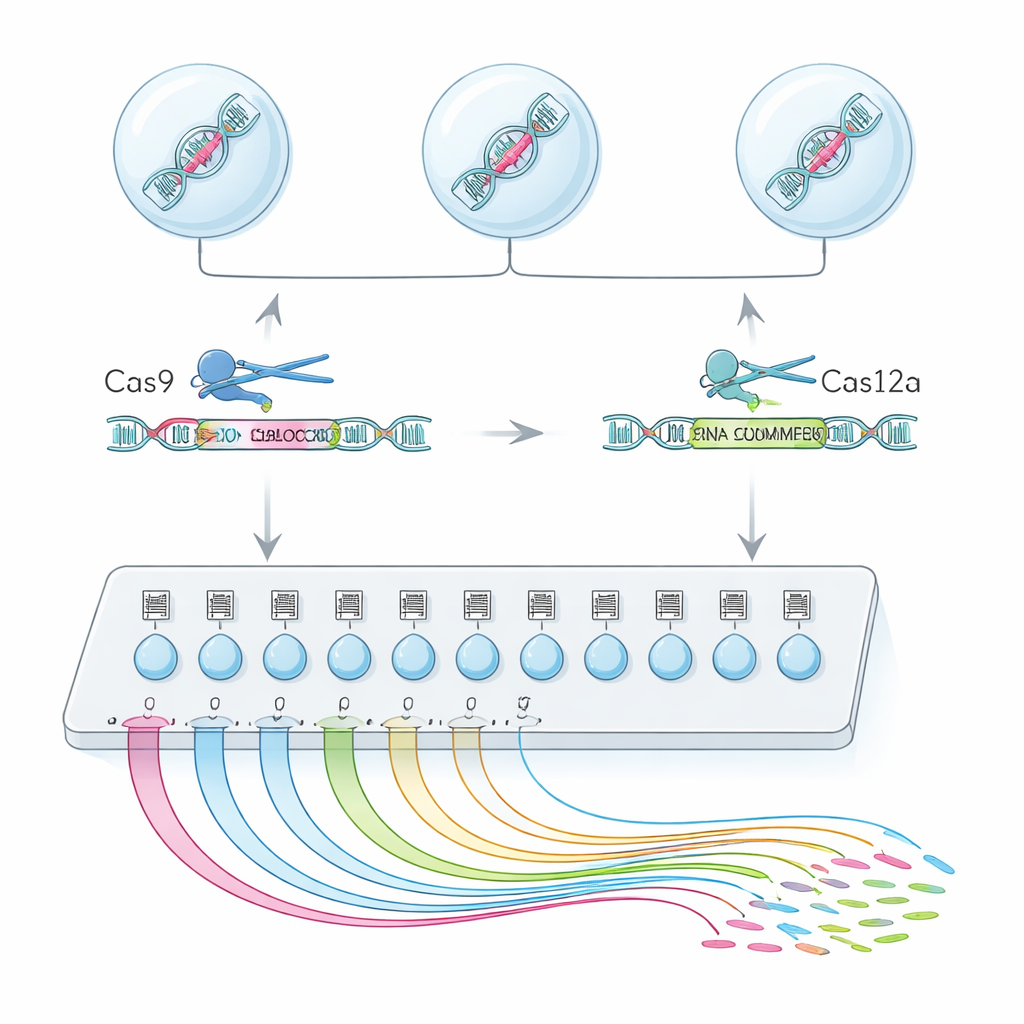
Silnik wyszukiwawczy funkcji egzonów działający w pojedynczych komórkach
Aby to osiągnąć, zespół połączył dwa enzymy edycji genomu, Cas9 i Cas12a, w hybrydową platformę nazwaną CHyMErA. Każdy enzym jest kierowany do DNA przez krótkie RNA pełniące rolę „adresów”. Kierując oba enzymy tak, by ciąć tuż przed i tuż po wybranym eksonie, można starannie usunąć ten segment, pozostawiając resztę genu nienaruszoną. Nowa metoda, scCHyMErA-Seq, łączy to precyzyjne cięcie z technologią sekwencjonowania RNA pojedynczych komórek. RNA każdej komórki jest przechwytywane w kropli razem z kodem kreskowym i przewodnikami RNA określającymi, który ekson został usunięty. Sekwencjonowanie ujawnia następnie, dla dziesiątek tysięcy komórek, zarówno edycję wykonaną w danej komórce, jak i szczegółowy wzór genów, które zostały włączone lub wyłączone.
Inżynieria narzędzia, aby widzieć oba ostrza nożyc
Kluczowym wyzwaniem było niezawodne wykrywanie przewodników Cas12a obok Cas9 w tej samej eksperymentalnej stacji pojedynczej komórki. Początkowe projekty albo nie wychwytywały przewodników Cas12a, albo uszkadzały wydajność edycji. Badacze rozwiązali ten problem, starannie przeprojektowując sekwencję uchwytu Cas12a, aby usunąć fragmenty, które przedwcześnie zatrzymywały transkrypcję, oraz dodając mały element stabilizujący RNA i ukierunkowany etap amplifikacji. Te zmiany zwiększyły możliwość wykrycia obu przewodników w około 90 procentach komórek, przy zachowaniu silnej efektywności usuwania egzonów. Dzięki tej zoptymalizowanej konfiguracji autorzy przeskanowali 224 egzony alternatywne w 161 genach ludzkich, profilując ponad 200 000 wysokiej jakości pojedynczych komórek.
Odkrywanie egzonów kontrolujących programy genowe i cykle komórkowe
Gdy zespół porównał aktywność genów w komórkach z edycjami do kontroli, niemal połowa testowanych eksonów wywołała znaczne przesunięcia w setkach innych genów. Egzony z genów zaangażowanych w przetwarzanie RNA i transkrypcję miały tendencję do grupowania się razem, dając podobne „odciski” ekspresyjne i ujawniając wspólne ścieżki biologiczne, takie jak budowa rybosomów czy degradacja RNA. W niektórych przypadkach usunięcie pojedynczego eksonu miało jasny i interpretowalny efekt: usunięcie eksonu w genach TAF5 lub LSM11 zaburzyło prawidłowe przetwarzanie RNA histonowych, prowadząc do nietypowego nagromadzenia się poliadenylowanych komunikatów histonowych. Zbiór danych wskazał także dziesiątki eksonów, których utrata zmieniała liczbę komórek znajdujących się w różnych fazach cyklu komórkowego, wiążąc konkretne zdarzenia splicingowe bezpośrednio z decyzjami o tym, kiedy komórka zatrzymuje się, kopiuje DNA lub przygotowuje do podziału.
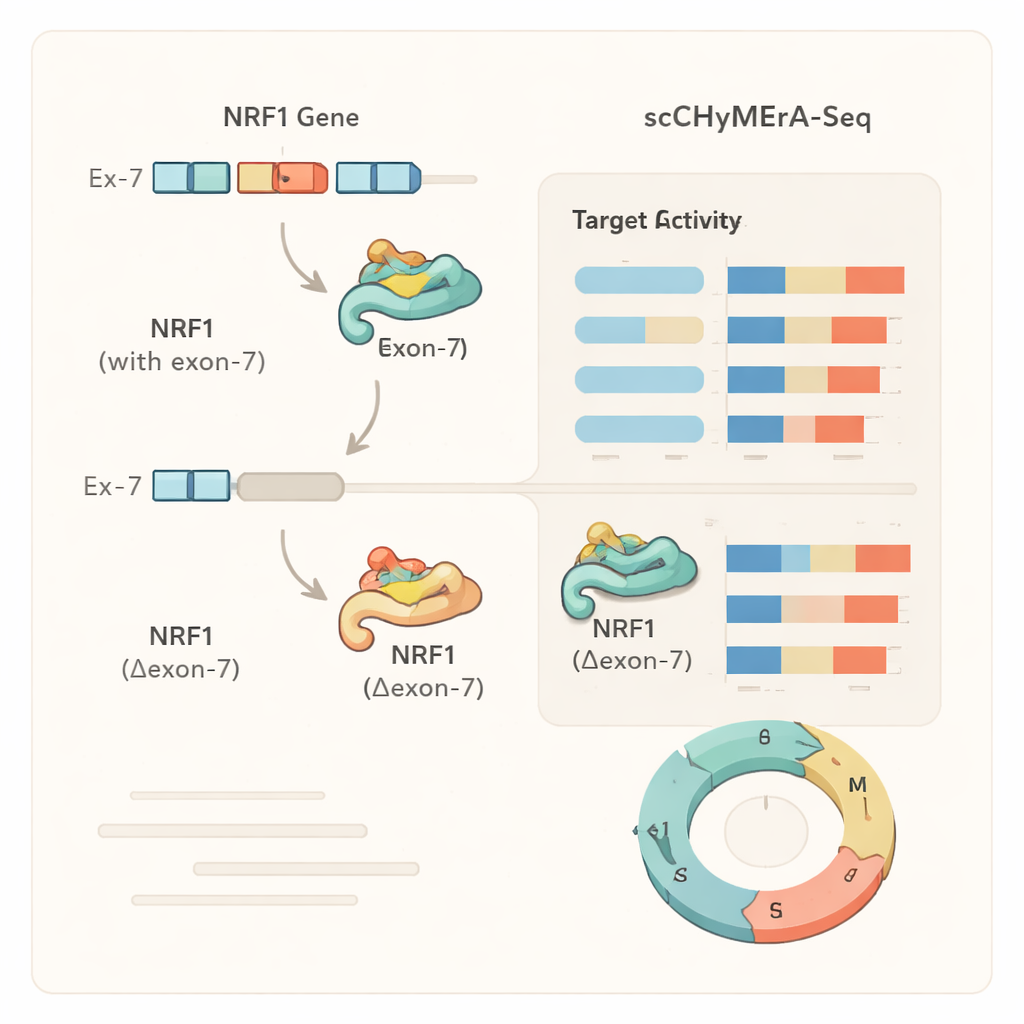
Studium przypadku: jeden ekson, który reguluje głównego nadzorcę
Jednym z uderzających przykładów był ekson 7 w genie NRF1, czynniku transkrypcyjnym kontrolującym wiele genów zaangażowanych w produkcję energii komórkowej. Ten ekson częściowo pokrywa region wiążący DNA NRF1. Gdy ekson 7 został usunięty, setki genów kontrolowanych przez NRF1 zmieniły swoją aktywność, a szczegółowe eksperymenty wykazały, że skrócone białko NRF1 znacznie słabiej wiązało swoje docelowe promotory w genomie. Autorzy zidentyfikowali także specyficzny regulator splicingu, SRSF3, który sprzyja włączeniu tego eksonu, ujawniając łańcuch od czynnika splicingu, przez wybór eksonu w NRF1, do szerokich zmian w programach genowych i metabolizmie komórkowym. Podobne analizy pokazały, że dla niektórych genów usunięcie eksonu naśladowało całkowite wyłączenie genu, podczas gdy w innych dawało bardziej subtelną, zależną od stanu zmianę, sugerując, że egzony alternatywne mogą delikatnie modulować funkcję białka zamiast po prostu je włączać lub wyłączać.
Dlaczego to ma znaczenie dla zdrowia i przyszłych terapii
Dla osoby niezajmującej się tym tematem kluczowy wniosek jest taki, że komórki polegają na włączaniu lub pomijaniu bardzo krótkich segmentów RNA, aby precyzyjnie regulować działanie genów, a te drobne regulacje mogą przesuwać istotne cechy, takie jak sposób podziału komórek czy reakcja na stres. Platforma scCHyMErA-Seq działa jak test laboratoryjny o dużej przepustowości dla tych wyborów splicingowych, wskazując, które egzony mają rzeczywisty wpływ funkcjonalny i jak przekształcają stany komórkowe. Ponieważ wiele nowotworów i zaburzeń neurologicznych wiąże się z nieprawidłowym splicingiem eksonów lub zmienionymi czynnikami transkrypcyjnymi, podejście to może pomóc w priorytetyzacji wariantów splicingowych do ukierunkowania przez przyszłe leki lub terapie RNA, oraz dostarczyć mapy pokazującej, jak drobne zmiany w genetycznym scenariuszu rozprzestrzeniają się na duże zmiany w zachowaniu komórek.
Cytowanie: Kumari, B., Damodaran, A.P., Guiblet, W.M. et al. Single-cell exon deletion profiling reveals splicing events that shape gene expression and cell state dynamics. Nat Commun 17, 1218 (2026). https://doi.org/10.1038/s41467-026-68774-w
Słowa kluczowe: splicing alternatywny, sekwencjonowanie RNA pojedynczych komórek, screening CRISPR, regulacja genów, cykl komórkowy