Clear Sky Science · pl
Nanozym naśladujący granazym B do celowanych przeciwnowotworowych zastosowań z użyciem nanowezików
Przeprojektowanie naturalnych zabójców raka
Nasz układ odpornościowy ma wyspecjalizowane komórki, które potrafią odnaleźć i zniszczyć komórki nowotworowe, lecz w wielu guzach litych mają trudności z dotarciem do wnętrza guza, szybko się wyczerpują lub atakują nieodpowiednie cele. W tym badaniu opisano całkowicie sztuczny system na skali nanometrowej, który imituje jedno z najsilniejszych narzędzi układu odpornościowego i dostarcza je bezpośrednio do komórek nowotworowych. Praca ma znaczenie, ponieważ wskazuje drogę do terapii przeciwnowotworowych zachowujących się jak żywe komórki odpornościowe, lecz wykonanych z trwałych, kontrolowalnych materiałów zamiast kruchych komórek ludzkich.
Przekształcenie naturalnego zabójcy w wzorzec
Limfocyty T cytotoksyczne, rodzaj białych krwinek, zabijają zagrożone komórki przy użyciu enzymu zwanego granazymem B. Gdy rozpoznają cel, tworzą małe otwory w błonie i wstrzykują granazym B, który uruchamia programy samobójcze wewnątrz komórki. Ta strategia leży u podstaw nowoczesnych terapii, takich jak komórki CAR-T, które mogą wyleczyć niektóre nowotwory krwi. Jednak w guzach litych komórki CAR-T często zawodzą, ponieważ nie docierają do wszystkich obszarów guza, ulegają wyczerpaniu lub celują w zdrowe tkanki przez pomyłkę. Autorzy postawili pytanie, czy można zbudować nieożywione urządzenie na skali nanometrowej, które odtworzy kluczową funkcję granazyma B — włączanie mechanizmu autodestrukcji komórki — bez polegania na żywych limfocytach T.
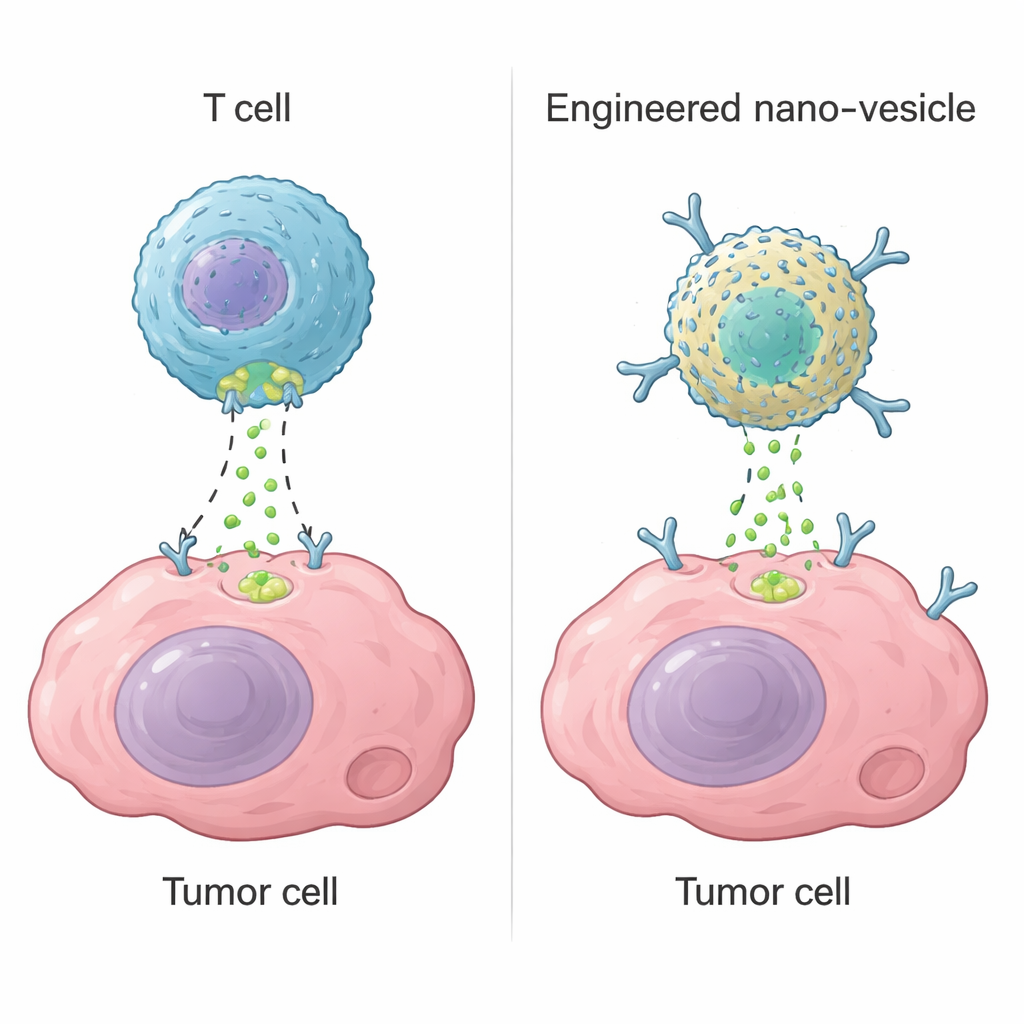
Projektowanie maleńkiego sztucznego enzymu
Zespół zaczął od ferrytyny, naturalnego białka tworzącego puste nanoklatki, którą łatwo wytwarzać w dużych ilościach. Poprzez wiązanie jonów palladu z ludzką ferrytyną stworzyli „nanozym” o właściwościach podobnych do enzymu. Dokładne badania strukturalne wykazały, że dwa atomy palladu osadzają się w specyficznej kieszeni na powierzchni białka, utrzymywane przez aminokwasy zawierające siarkę i azot oraz cząsteczki wody. Ten binuklearny ośrodek metalu działa jako sztuczne miejsce tnące, które rozpoznaje tę samą krótką sekwencję, którą wykorzystuje granazym B na kluczowym celu znanym jako kaspaza-3. W testach laboratoryjnych nanozym wydajnie odcinał kaspazę-3 w odpowiednim miejscu, aktywując ją, przy jednoczesnym pomijaniu białek blisko spokrewnionych. Sztuczny enzym był nieco mniej efektywny niż naturalny granazym B, ale zauważalnie bardziej stabilny w szerokim zakresie temperatur i kwasowości.
Przemycanie nanozymu do komórek guza
Enzymy takie jak granazym B działają tylko wtedy, gdy dotrą do wnętrza komórek nowotworowych. Aby to osiągnąć, badacze zapakowali swój palladowo–ferrytynowy nanozym wewnątrz lipidowych nanowezików — małych, miękkich pęcherzyków zbudowanych z cząsteczek podobnych do tłuszczu. Następnie pokryli te pęcherzyki fragmentami przeciwciał rozpoznających HER2, białko często nadmiernie eksprymowane w komórkach raka piersi i pęcherza. Gdy takie zamaskowane wezeikuly natrafiają na komórki bogate w HER2, ściśle się do nich wiążą i łączą z błoną komórkową, pozwalając ładunkowi nanozymu wślizgnąć się prosto do cytoplazmy zamiast być uwięzionym i strawionym w komórkowych przedziałach recyklingowych. Mikroskopia pokazała wezeikuly utrzymujące się przy powierzchni komórki, podczas gdy nanozym dyfundował do wnętrza, przygotowując grunt pod kontrolowaną autodestrukcję od środka.
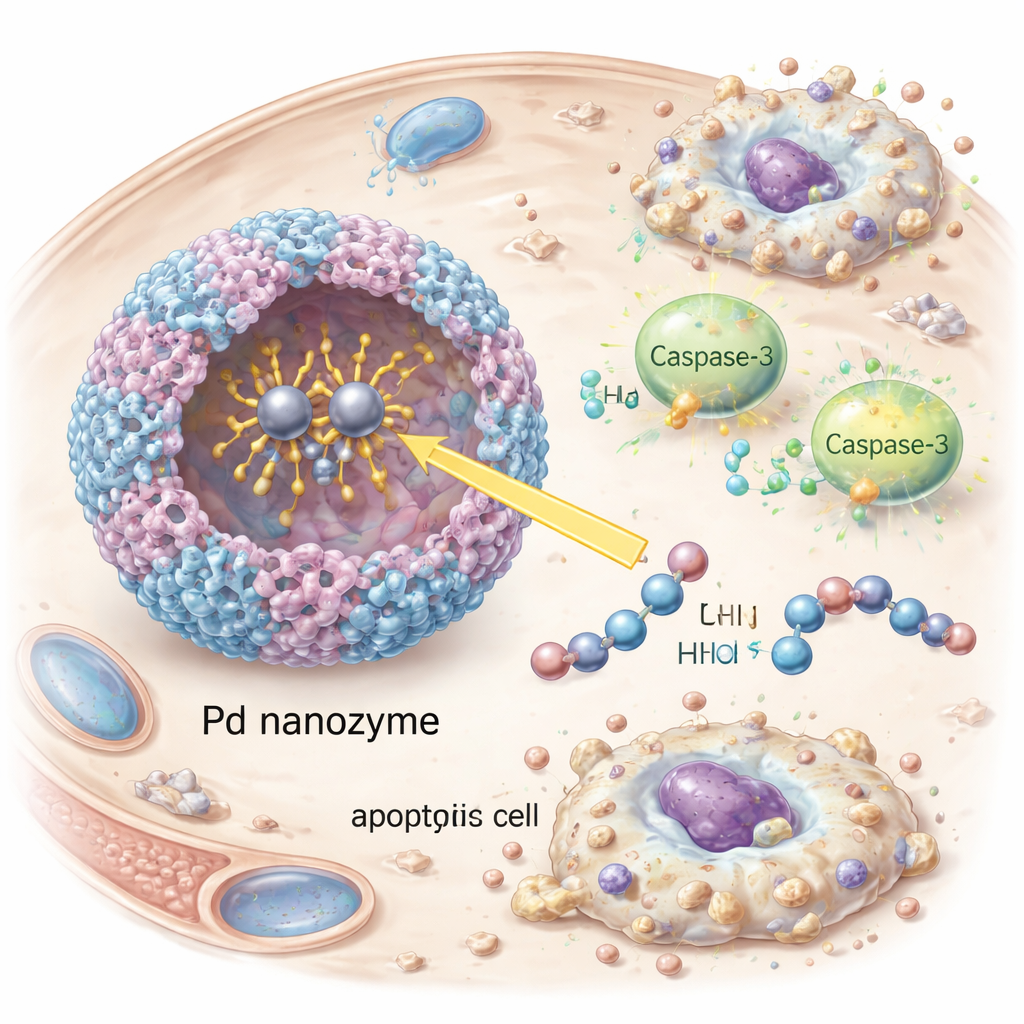
Precyzyjne uruchamianie samobójstwa komórek nowotworowych
Po dostaniu się do komórek nowotworowych nanozym aktywował kaspazę-3, centralnego egzekutora zaprogramowanej śmierci komórki. Badacze zaobserwowali pojawienie się aktywowanej kaspazy-3 i jej docelowego białka PARP, a także wyraźne oznaki apoptozy — kurczenie się i fragmentację komórek — w hodowanych komórkach nowotworowych HER2-dodatnich. Wyciszenie kaspazy-3 za pomocą interferencji RNA dramatycznie zmniejszyło śmiertelność komórek, potwierdzając, że efekt zależał od tej ścieżki, a nie od niespecyficznego uszkodzenia. U myszy z guzami HER2-dodatnimi przeciwciałem ozdobione wezeikuly krążyły dłużej we krwi, gromadziły się mocniej w guzach i skuteczniej spowalniały wzrost guza niż wezeikuly pozbawione albo przeciwciał celujących, albo ładunku nanozymu. Co ważne, leczone zwierzęta nie wykazały oczywistej utraty masy ciała, nieprawidłowości we krwi ani uszkodzeń tkanek w głównych narządach, co sugeruje korzystny profil bezpieczeństwa w tych wczesnych testach.
Co to może znaczyć dla przyszłej opieki nad chorymi na raka
Dla osób niezwiązanych z dziedziną główna wiadomość jest taka, że badacze zbudowali maleńkie, nieożywione urządzenie, które zachowuje się jak kluczowa część maszynerii układu odpornościowego do zabijania raka. Zamiast modyfikować żywe komórki T, opracowali stabilny nanoenzym, który aktywuje ten sam przełącznik samobójczy wewnątrz komórek nowotworowych i zapakowali go w inteligentną powłokę dostarczającą skierowaną na konkretne nowotwory. Choć wciąż wiele pracy przed dopuszczeniem do stosowania u ludzi, podejście to oferuje elastyczną platformę: w praktyce powłokę z przeciwciał można by wymienić, aby celować w inne markery nowotworowe, a sztuczny enzym można by dalej optymalizować. Badanie pokazuje obiecującą drogę do immunoterapii bezkomórkowej, w której starannie zaprojektowane nanomateriały, zamiast żywych komórek odpornościowych, są używane do namierzania i niszczenia guzów litych.
Cytowanie: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
Słowa kluczowe: nanomedycyna przeciwnowotworowa, immunoterapia, granazym B, nanozym, nowotwory HER2-dodatnie