Clear Sky Science · pl
Bioortogonalna chemia aktywowana reaktywnymi formami tlenu w systemach żywych umożliwiona przez dihydrotetrazyny chronione boronianem
Przekształcanie stresu komórkowego w precyzyjny przełącznik
Wiele chorób, od raka po schorzenia serca, charakteryzuje się komórkami będącymi w stanie stresu oksydacyjnego, produkującymi wysokie poziomy reaktywnych form tlenu, takich jak nadtlenek wodoru. Badanie pokazuje, jak chemicy mogą wykorzystać ten sam stres jako wbudowany przełącznik, który włącza silne terapie tylko tam, gdzie są potrzebne. Projektując składniki leków reagujące wyłącznie w tych zestresowanych środowiskach, naukowcy dążą do zabijania komórek nowotworowych lub niszczenia szkodliwych białek przy jednoczesnym oszczędzaniu tkanek zdrowych.
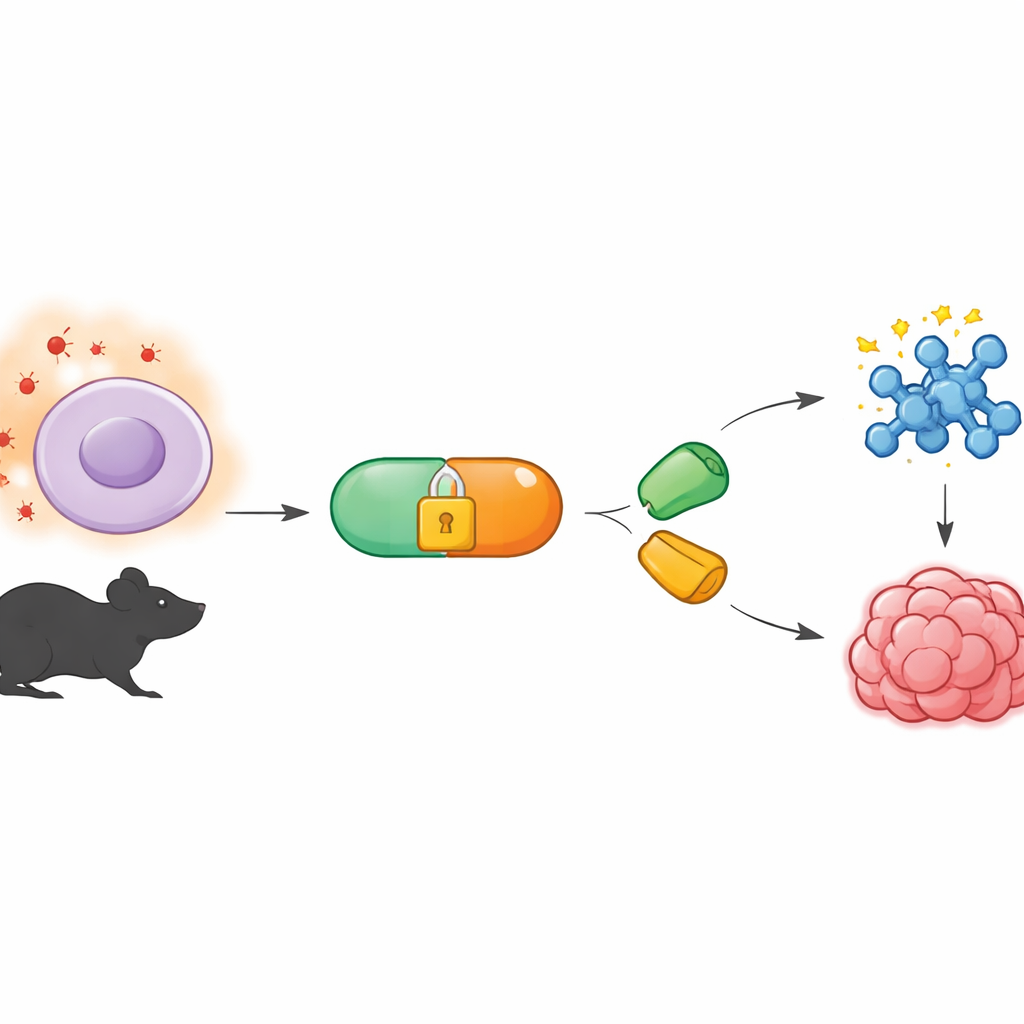
Chemiczne narzędzie działające cicho w tle
Praca opiera się na dziedzinie zwanej chemią bioortogonalną, która opracowuje reakcje możliwe do prowadzenia w obrębie żywych organizmów bez zakłócania normalnej biologii. Popularna wersja wykorzystuje specjalne pary cząsteczek, które łączą się jak elementy układanki, nawet w zatłoczonym wnętrzu komórki. Jednym z partnerów jest tetrazyna, która reaguje bardzo szybko z dopasowanym „pierścieniem”, zwanym dienofilem. Do tej pory wiele z tych reakcji kontrolowano przez naświetlanie lub dodawanie enzymów. Autorzy chcieli jednak systemu, który nasłuchuje własnych sygnałów chemicznych ciała — konkretnie nietypowo wysokich poziomów reaktywnych form tlenu występujących w guzach i innych chorych tkankach.
Budowa chemicznego wyzwalacza wrażliwego na ROS
Aby to osiągnąć, zespół stworzył prekursory tetrazyn, które nazwali BTz, chemicznie „zamknięte”, tak aby pozostawały nieaktywne w tkankach zdrowych. Klatka zbudowana jest z grupy boronianowej połączonej z zredukowaną formą tetrazyny. Gdy nadtlenek wodoru jest rzadki, BTz jest stabilny w wodzie i w hodowli komórek przez wiele godzin. Gdy jednak nadtlenek wodoru jest obfity — na poziomach podobnych do zmierzonych w guzach — grupa boronianowa ulega utlenieniu i rozpada się w sekwencji autodestrukcyjnej, odsłaniając aktywną tetrazynę. W eksperymentach w probówce stopniowe podwyższanie stężenia nadtlenku wodoru prowadziło do odpowiadającego wzrostu ilości aktywnej tetrazyny, co potwierdza, że reakcja jest selektywna i silnie zależna od dawki.
Wykorzystanie stresu komórkowego do zniszczenia białka napędzającego raka
Naukowcy najpierw użyli swojego przełącznika do kontrolowania nowoczesnej strategii lekowej zwanej celowaną degradacją białek. Dołączyli BTz do talidomidu, małej cząsteczki, która może rekrutować kompleks enzymatyczny odpowiedzialny za znakowanie białek do utylizacji. W komórkach nowotworowych ten kompleks BTz–talidomid pozostawał uśpiony aż do momentu wzrostu poziomu nadtlenku wodoru, gdy klatka otwierała się i powstawała aktywna tetrazyna. Ta tetrazyna następnie łączyła się z dopasowanym partnerem związanym z lekiem wiążącym BRD4, składając większe „chimeryczne” połączenie, które kierowało białko związane z rakiem BRD4 do mechanizmów usuwania komórkowego. W liniach komórkowych raka płuca i szyjki macicy poziomy BRD4 spadły gwałtownie tylko wtedy, gdy wszystkie części były obecne i dostępny był nadtlenek wodoru; blokowanie reaktywnych form tlenu zapobiegało degradacji, podkreślając, że proces jest rzeczywiście aktywowany stresem.
Dostarczanie toksycznego leku tylko tam, gdzie jest potrzebne
Następnie zespół przekształcił tę samą chemię w precyzyjny system dostarczania doksorubicyny, silnej, ale szkodliwej dla serca chemioterapii. Połączyli doksorubicynę z naprężonym partnerem pierścieniowym, tak aby utworzyć nieaktywny prolek. Gdy ten prolek napotkał BTz w środowisku bogatym w nadtlenek wodoru, powstała tetrazyna reagowała z pierścieniem w procesie „click-to-release”, łącząc elementy i uwalniając wolną doksorubicynę. W komórkach raka okrężnicy hodowanych w płytkach ten dwustopniowy system zabijał komórki niemal tak skutecznie jak wolny lek, ale tylko w obecności nadtlenku wodoru; bez niego komórki pozostawały w dużej mierze nienaruszone. Prostszy prolek doksorubicyny wrażliwy na nadtlenek wodoru był mniej skuteczny i mniej selektywny w tych testach, co uwypukla zaletę rozdzielenia detekcji i uwalniania na dwa skoordynowane etapy.
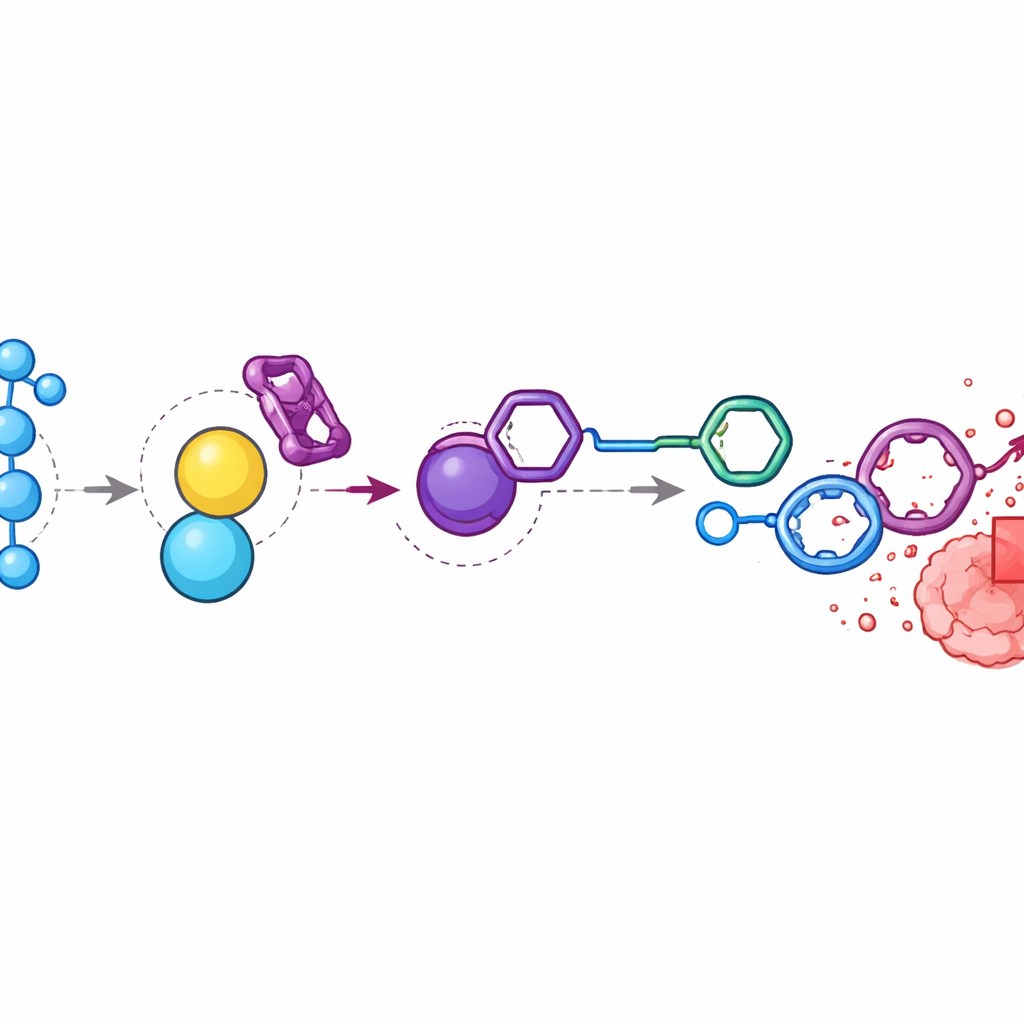
Skupienie chemioterapii wewnątrz guzów
U myszy z guzami okrężnicy badacze stwierdzili, że poziomy nadtlenku wodoru w guzach były niemal dziewięciokrotnie wyższe niż w otaczającym mięśniu. Wstrzyknęli prolek doksorubicyny i BTz w odpowiednio zaplanowanej sekwencji tak, aby oba składniki gromadziły się w pobliżu guza. Analiza chemiczna wykazała, że składniki w dużej mierze znikały z krwiobiegu i narządów, ale generowały wysokie poziomy wolnej doksorubicyny wewnątrz guzów. W porównaniu ze zwierzętami otrzymującymi standardową doksorubicynę, te leczone aktywowanym systemem wykazywały podobne lub lepsze kurczenie się guza, przy jednoczesnym utrzymaniu stabilnej masy ciała i unikaniu silnej toksyczności obserwowanej przy wyższych dawkach leku. Gdy zespół zablokował sygnał nadtlenku wodoru przez podanie katalazy, enzymu usuwającego nadtlenek wodoru, uwalnianie leku i selektywne nagromadzenie w guzie znacznie się zmniejszyły, potwierdzając, że stresem oksydacyjnym w miejscu guza jest główny mechanizm napędowy.
Od sygnału stresu do terapii precyzyjnej
Podsumowując, badanie pokazuje wszechstronną platformę chemiczną, która przekształca cechę choroby — nadmiar reaktywnych form tlenu — w precyzyjny element sterujący dla potężnych reakcji w systemach żywych. Dzięki utrzymywaniu reaktywnego uchwytu tetrazyny zablokowanego aż do napotkania nadtlenku wodoru, podejście pozwala badaczom budować złożone terapie wewnątrz ciała wyłącznie tam, gdzie są potrzebne, czy to aby rozmontować białko sprzyjające rakowi, czy uwolnić toksyczny lek wewnątrz guza. Ponieważ stres oksydacyjny odgrywa także rolę w starzeniu się, zapaleniu, cukrzycy i chorobach neurodegeneracyjnych, podobne reakcje reagujące na stres mogą ostatecznie zostać zaadaptowane do wielu schorzeń, w których precyzja i bezpieczeństwo mają kluczowe znaczenie.
Cytowanie: Ming, D., Zhang, J., Mu, B. et al. Reactive oxygen species-activated bioorthogonal chemistry in living systems enabled by boronate-caged dihydrotetrazines. Nat Commun 17, 2568 (2026). https://doi.org/10.1038/s41467-026-68771-z
Słowa kluczowe: bioortogonalna chemia, reaktywne formy tlenu, wiązanie tetrazynowe, celowane dostarczanie leków, PROTAC