Clear Sky Science · pl
Homotypiczna membranowo-napędzana elektrochemiczna mikrofluidyczna analiza pęcherzyków zewnątrzkomórkowych dla precyzyjnej diagnozy nowotworowej
Przekształcanie własnej zbroi nowotworu w narzędzie diagnostyczne
Błony otaczające komórki nowotworowe są wypełnione charakterystycznymi „flagami” molekularnymi. Badanie pokazuje, jak naukowcy mogą zdjąć tę zbroję, rozprowadzić ją na maleńkich złotych płytkach, a następnie użyć jej do wyłowienia z krwi rozpoznawczych cząstek. Efektem jest wysoce czuły test krwi, który może ujawnić nie tylko obecność raka piersi, lecz także jego podtyp — informację kluczową przy doborze właściwego leczenia.
Dlaczego podtyp raka piersi ma znaczenie
Rak piersi nie jest jednorodną chorobą. Guzy grupuje się w podtypy, takie jak dodatni receptor estrogenowy (ER+), HER2-dodatni czy potrójnie ujemny; każdy reaguje inaczej na terapię hormonalną, leki celowane czy chemioterapię. Dziś lekarze zwykle określają podtyp na podstawie biopsji tkankowej pobranej bezpośrednio z guza. Procedura ta jest inwazyjna, nie można jej często powtarzać i może nie uchwycić zmian zachodzących w przebiegu choroby. Test z krwi, który śledziłby sygnatury podtypów w czasie, pozwoliłby lekarzom wcześniej i precyzyjniej dostosowywać terapię.
Maleńcy posłańcy unoszący się we krwi
Komórki nowotworowe nieustannie zrzucają do krwi nanoskalowe pęcherzyki zwane pęcherzykami zewnątrzkomórkowymi (EV). EV niosą białka, lipidy i materiał genetyczny przypominający skład rodzicielskich komórek, co czyni je atrakcyjnymi kandydatami do „płynnych biopsji”. Jest jednak wyzwanie: EV pochodzące z różnych podtypów raka piersi mogą wyglądać bardzo podobnie, jeśli skupić się tylko na jednym lub dwóch markerach. Istniejące testy albo celują w wspólne markery — co utrudnia rozróżnienie podtypów — albo opierają się na złożonych testach genetycznych, które są powolne i mogą wprowadzać w błąd. Autorzy postanowili odczytać pełniejszy odcisk molekularny na powierzchni EV w sposób prosty i odporny na zakłócenia.
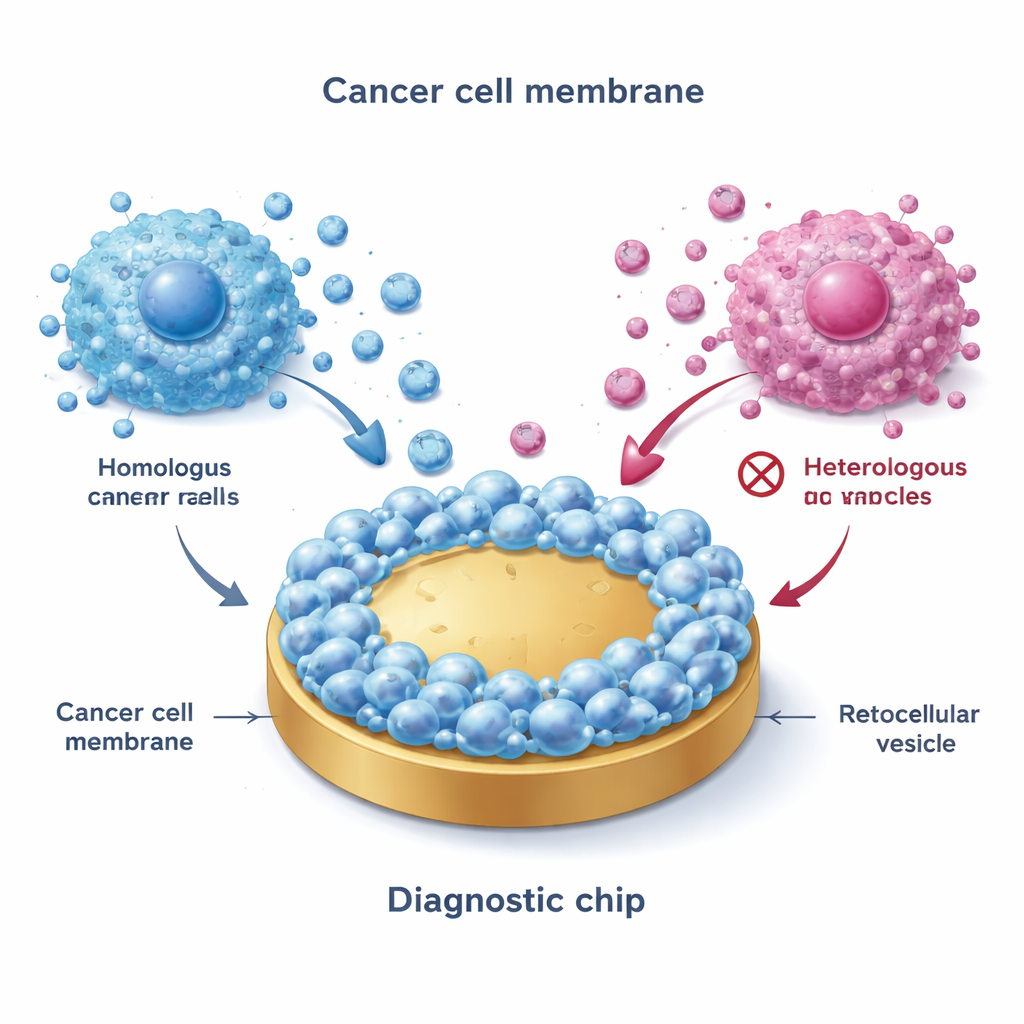
Budowa biomimetycznej sieci wędkarskiej
Zespół rozpoczął od pozyskania błon z hodowanych komórek raka piersi reprezentujących główne podtypy: ER+ (np. MCF-7), HER2-dodatni oraz potrójnie ujemny. Przy użyciu procesu zamrażania i rozmrażania rozbili komórki, izolowali błony zewnętrzne, a następnie zlanie tych błon na płaskie złote powierzchnie stworzyło „biomimetyczne interfejsy” wiernie naśladujące zewnętrze pierwotnych komórek nowotworowych. Co istotne, gdy EV przepływały nad tak powleczonymi powierzchniami, silnie przyczepiały się jedynie pęcherzyki z dopasowanych lub blisko spokrewnionych podtypów — zjawisko zwane wiązaniem homotypicznym. Zaawansowane obrazowanie i pomiary elektryczne potwierdziły, że powierzchnie pokryte błoną były bardziej chropowate, bardziej hydrofilowe i znacznie mniej podatne na nieswoiste przywieranie niż gołe złoto, co czyni je odpowiednimi do czystych pomiarów w złożonych płynach, takich jak krew.
Przekształcenie łapania pęcherzyków w sygnał elektryczny
Aby zamienić wiązanie na odczytywalny sygnał, badacze wykorzystali obficie występujące białko CD47 na powierzchni EV. Przymocowali przeciwciała przeciw CD47 do nanocząstek srebra za pomocą krótkiego mostka DNA, tworząc drobne elektroaktywne znaczniki. Po tym, jak powierzchnia pokryta błoną wychwyciła preferowane EV, znaczniki przyłączały się do CD47 na związanych pęcherzykach. Po ekspozycji na roztwór kwasu i następnie pomiarze elektrochemicznym srebro generowało ostry, łatwy do ilościowego zmierzenia prąd. Siła tego sygnału rosła w sposób liniowy w szerokim zakresie stężeń EV, aż do zaledwie kilkuset pęcherzyków na mililitr — znacznie czułość większa niż powszechne metody, takie jak zestawy ELISA czy śledzenie cząstek. Każdy typ błony nowotworowej dawał silny sygnał tylko z odpowiadającymi mu EV, nawet w obecności pęcherzyków z innych podtypów, płytek krwi czy niemających związku komórek.
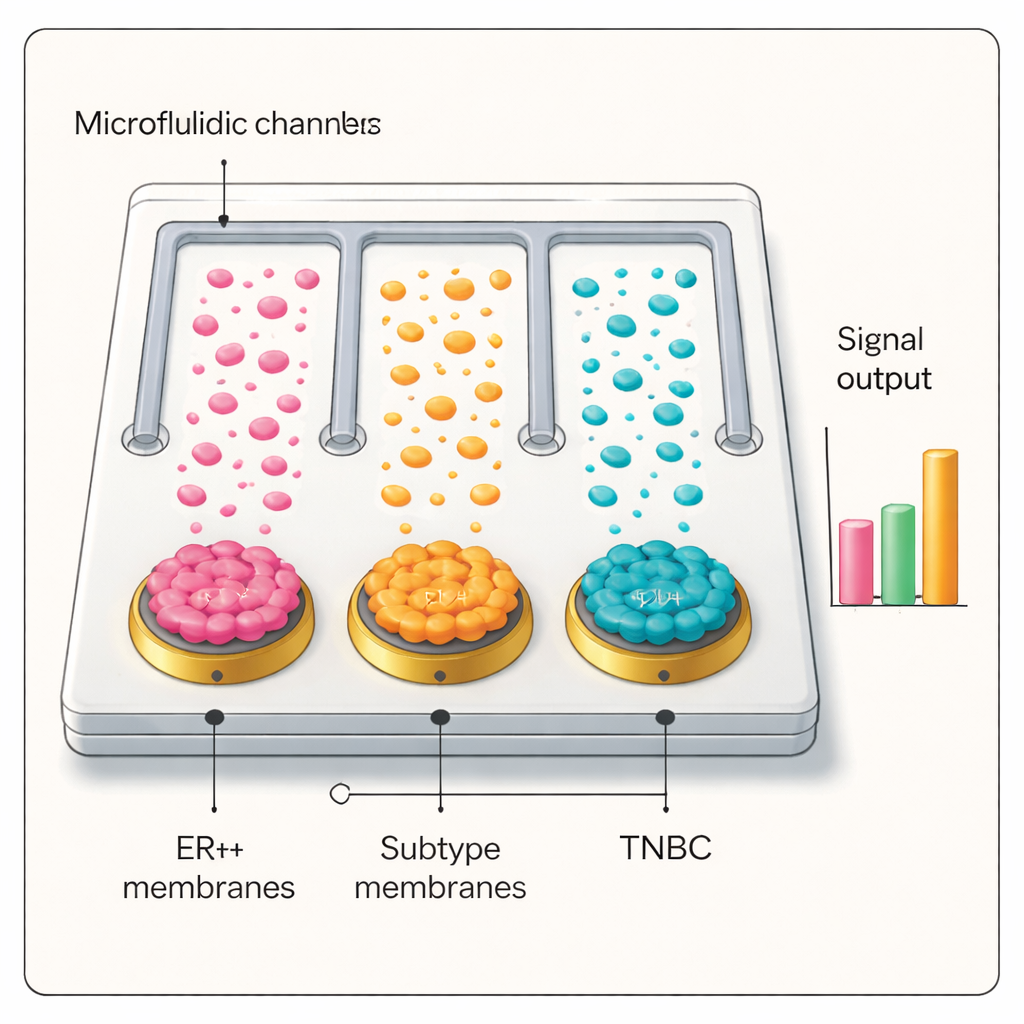
Od stołu laboratoryjnego do próbek krwi pacjentów
Wyposażeni w selektywny i czuły interfejs, badacze zbudowali chip mikrofluidyczny zawierający równoległe kanały, z których każdy był powleczony błoną innego typu komórek raka piersi, oraz kanał kontrolny bez powłoki. Gdy osocze od pacjentów przepuszczano przez chip i poddawano działaniu srebrno‑przeciwciałowych znaczników, jedynie kanał z błoną dopasowaną do podtypu guza pacjenta generował wysoki sygnał elektryczny. W zasłoniętych testach z udziałem kilkudziesięciu osób — w tym chorych na raka piersi ER+ i potrójnie ujemnego, pacjentów z łagodnymi zmianami piersi, chorych na raka płuca oraz zdrowych ochotników — platforma trafnie odróżniała przypadki nowotworowe od nienowotworowych i poprawnie identyfikowała podtypy raka piersi. W wielu przypadkach wydajność diagnostyczna dorównywała lub przewyższała standardową patologię i wykazała potencjał do określania stopnia zaawansowania choroby oraz śledzenia jej progresji.
Co to może oznaczać dla przyszłej opieki onkologicznej
Mówiąc prosto, badacze przekształcili zewnętrzną powłokę nowotworu w wysoce selektywną przynętę na maleńkie cząstki, które guzy uwalniają do krwi. Odczytując elektryczny podpis kanału, który „rozświetla się”, lekarze mogliby w przyszłości określić nie tylko, czy rak jest obecny, ale także, jaki to rodzaj — używając do tego jedynie próbki krwi. Choć system wymaga dalszych usprawnień — na przykład dodania większej liczby markerów i typów błon oraz integracji zaawansowanej analizy danych — wskazuje na przyszłość, w której rutynowe, minimalnie inwazyjne badania krwi pomogą kierować spersonalizowanym leczeniem nowotworów i monitorować zmiany guzów w czasie.
Cytowanie: Zou, Z., Jin, X., Yu, X. et al. Homotypic membrane-powered electrochemical microfluidic analysis of extracellular vesicles for precise cancer diagnosis. Nat Commun 17, 1953 (2026). https://doi.org/10.1038/s41467-026-68770-0
Słowa kluczowe: podtypy raka piersi, płynna biopsja, pęcherzyki zewnątrzkomórkowe, diagnostyka mikrofluidyczna, czujniki błon komórkowych