Clear Sky Science · pl
Obiegowe zespoły molekularne do obrazowania i zakłócania aparatu Golgiego
Przekształcenie komórkowego centrum wysyłkowego w cel strategiczny
W każdej komórce zwierzęcej znajduje się aparat Golgiego — zatłoczona stacja sortująca, która wykańcza, pakuje i wysyła tysiące białek i lipidów. Wiele komórek nowotworowych mocno polega na tym centrum, aby modyfikować sygnały wzrostowe i wydzielać czynniki kształtujące mikrośrodowisko guza. W artykule przedstawiono malutkie zaprojektowane molekuły, które trafiają do Golgiego, umożliwiają szybkie obrazowanie, a po odpowiedniej przebudowie mogą selektywnie zakłócać jego funkcje, osłabiając komórki nowotworowe przy stosunkowo mniejszym uszkodzeniu niektórych komórek zdrowych.
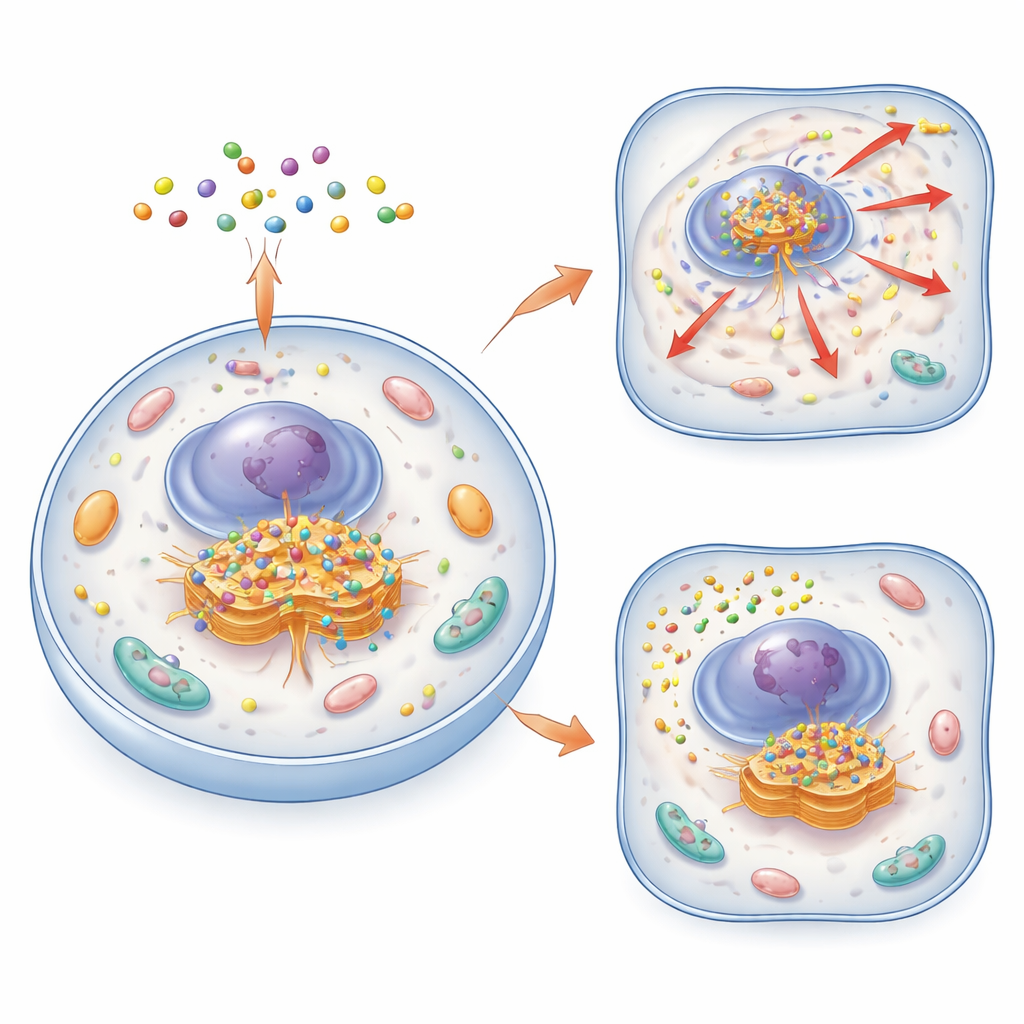
Nowy sposób znajdowania i obserwacji Golgiego
Autorzy stworzyli rodzinę małych, „inteligentnych” molekuł nazwanych obiegowymi zespołami molekularnymi, czyli CyMA. Molekuły te zbudowane są z krótkich peptydów, które mogą przenikać przez błony komórkowe i skłaniać się do zlepiania w drobne skupiska. W wersji „obrazującej” (CyMA-i) peptydy niosą barwnik fluorescencyjny, który silnie świeci, gdy molekuły się składają. Po wejściu do komórki enzymy usuwają ochronną czapeczkę z prekursora CyMA, odsłaniając reaktywną grupę. Enzymy rezydujące w Golgim przyłączają do tej grupy łańcuch lipidowy, co zwiększa lepkość molekuł i sprzyja ich samoagregacji dokładnie w obrębie Golgiego. Ponieważ proces ten jest szybki i wykorzystuje naturalne mechanizmy komórkowe, badacze mogą w ciągu kilku minut i przy bardzo niskich stężeniach sondy zarysować kształt Golgiego w żywych komórkach.
Bezużyteczny cykl, który przytwierdza molekuły do Golgiego
CyMA to nie tylko znaczniki — zaprojektowano je tak, by uczestniczyły w „bezowocnym cyklu” w Golgim. Jedna grupa enzymów przyłącza łańcuchy lipidowe do peptydu, podczas gdy inna je usuwa. W miarę jak komórka wielokrotnie dodaje i usuwa te łańcuchy, zmodyfikowane peptydy ciągle się składają i rozkładają in situ. To ciągłe „tam i z powrotem” tworzy na błonach Golgiego rdzeń o właściwościach stałych, podczas gdy pojedyncze molekuły nadal się wymieniają. Komórka musi nieustannie zużywać własne zasoby kwasów tłuszczowych, by podtrzymać ten cykl, co w praktyce „karmi” zespoły i pomaga im przetrwać. Równocześnie dodatkowe enzymy mogą powoli przecinać specyficzny ester w CyMA, zamieniając je w bardziej hydrofilne fragmenty, które odpływają. Ponieważ niektóre zdrowe komórki, jak hepatocyty czy pewne komórki układu odpornościowego, obfitują w takie esterazy, są one lepiej przygotowane do rozmontowania CyMA i w efekcie mniej nimi dotknięte.
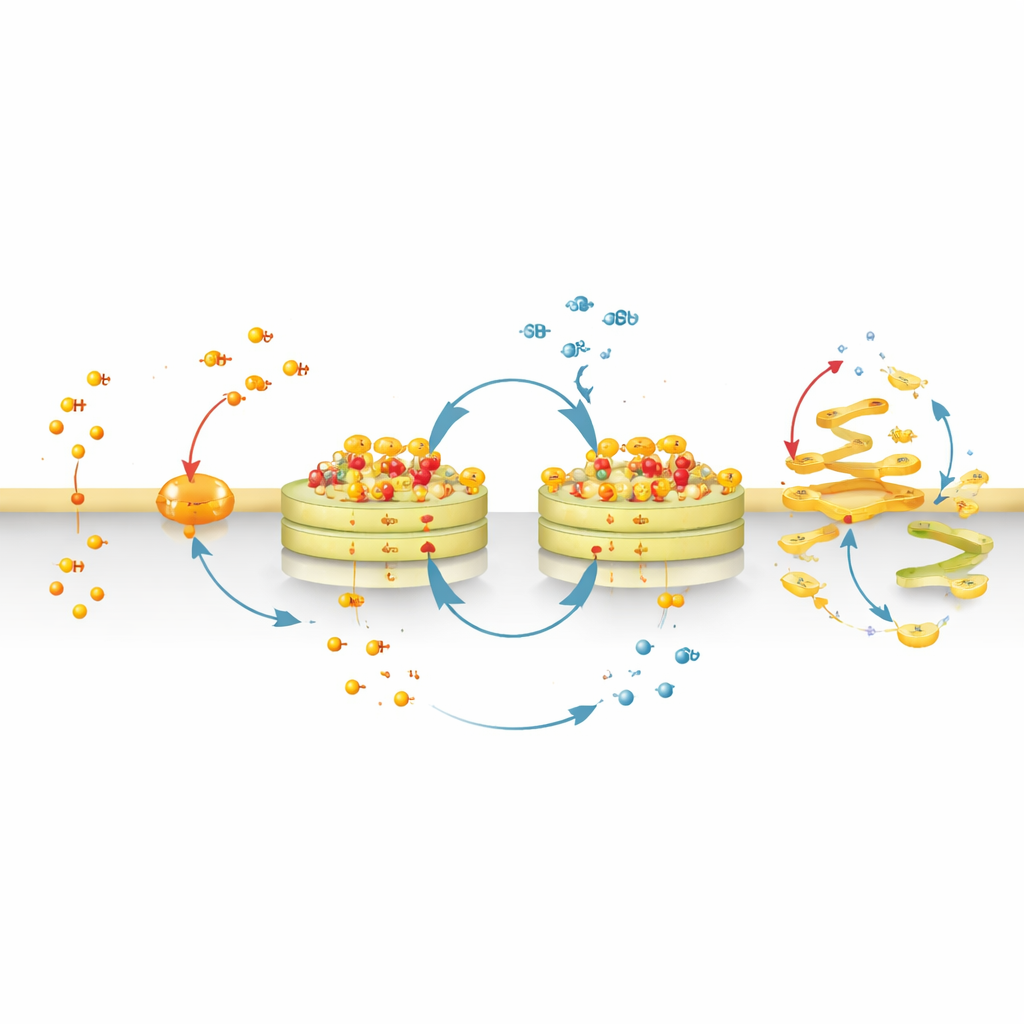
Od delikatnego narzędzia obrazującego do rozregulowania Golgiego
Wymieniając barwnik fluorescencyjny na silniej przyciągającą błony grupę chemiczną, zespół przekształcił CyMA-i w CyMA-d — wersję zakłócającą, która przestaje świecić, ale nadal cyklicznie się składa i tworzy agregaty w Golgim. Te zespoły fizycznie zaburzają strukturę Golgiego i ciągły przepływ pęcherzyków do niego i z niego. Białka, które normalnie przemieszczają się z retikulum endoplazmatycznego do Golgiego, a następnie na powierzchnię komórki, stają się uwięzione lub źle kierowane. Drogi przychodzące — od powierzchni komórki z powrotem do Golgiego lub z Golgiego do innych organelli — są również blokowane. W rezultacie kluczowe receptory powierzchniowe i molekuły sygnałowe albo nie docierają do swoich miejsc docelowych, albo gromadzą się w nieodpowiednich lokalizacjach wewnątrz komórki.
Zakłócanie sygnałów komórkowych i przesyłek wydzielniczych
W Golgim wiele białek otrzymuje kluczowe „wykończenia”, takie jak łańcuchy cukrowe czy łańcuchy lipidowe. Agregaty CyMA-d ograniczają prawidłową lipidację i glikozylację licznych białek, w tym znanych czynników nowotworowych, takich jak Ras i główne receptory kinaz tyrozynowych. Zmiany te psują szlaki promujące wzrost, takie jak AKT i mTOR. Równocześnie wydzielanie komórkowe zostaje stłumione: ważne czynniki jak TGF-β1 i VEGF, których guzy używają do tłumienia odporności i stymulacji angiogenezy, nie są już efektywnie uwalniane. Stres wynikający z tego rozpadu powoduje splątane sieci siateczki endoplazmatycznej, zmienione mitochondria, zahamowaną autofagię (system recyklingu komórkowego) oraz nagromadzenie uszkodzonych białek oznaczonych ubikwityną, co razem popycha komórki nowotworowe w kierunku śmierci.
Selekcja przeciwnowotworowa i obietnica terapii
Ponieważ CyMA-d wykorzystują wspólny zestaw enzymów i metabolitów, z których wiele komórek nowotworowych nadużywa, mogą zabijać szerokie spektrum typów guzów, w tym modele raka jajnika oporne na leki, przy bardzo niskich dawkach. Komórki o wysokim poziomie specyficznych esteraz jednak szybciej rozmontowują CyMA-d i są mniej uszkadzane, co daje wbudowaną drogę do selektywności. W trójwymiarowych sferoidach nowotworowych, kulturach pochodzących od pacjentów i modelach mysich CyMA-d zmniejszają guzy, ograniczają przerzuty i redukują gromadzenie się płynu w jamie brzusznej. W połączeniu z terapiami hamującymi punkty kontrolne układu odpornościowego dodatkowo poprawiają kontrolę nad guzem i przeżywalność. W istocie praca ta pokazuje, że budowanie dynamicznych materiałów wewnątrz Golgiego — zamiast celowania w pojedyncze białko — może jednocześnie wyłączyć wiele procesów krytycznych dla rozwoju nowotworu.
Co to oznacza dla przyszłych terapii
Dla osoby niebędącej specjalistą kluczowa idea jest taka, że autorzy przekształcili Golgiego z biernego obserwatora w aktywny cel terapeutyczny. Rekrutując własne enzymy komórki do składania i recyklingu malutkich prekursora w tym centralnym węźle, można albo bezpiecznie go uwidocznić, albo stopniowo przytłoczyć jego funkcję. Ta platforma o podwójnym zastosowaniu sugeruje nowy rodzaj leczenia: zamiast projektować pojedynczy lek przeciw jednemu białku, można tworzyć małe prekursory, które komórki przekształcają w samoorganizujące się materiały, zdolne do zakłócenia całych sieci komunikacji i transportu, od których nowotwory zależą, by rosnąć i się rozprzestrzeniać.
Cytowanie: Tan, W., Zhang, Q., Liu, Z. et al. Cycling molecular assemblies for Golgi imaging and disruption. Nat Commun 17, 2102 (2026). https://doi.org/10.1038/s41467-026-68768-8
Słowa kluczowe: Aparat Golgiego, zespoły molekularne, transport białek, terapia przeciwnowotworowa, ukierunkowanie organelli