Clear Sky Science · pl
Endotelialny PDLIM5 wspiera tworzenie filopodiów komórek końcowych i angiogenezę nowotworową poprzez regulację ACTN1/ACTN4-zależnego łączenia aktyny
Jak nowotwór zawłaszcza naczynia krwionośne
Nowotwór nie może rozrosnąć się poza niewielką skupioną masę bez przekonania pobliskich naczyń krwionośnych do dostarczania tlenu i składników odżywczych. Badanie to ujawnia, jak mało znane białko w wyściółce naczyń pomaga guzom rozgałęziać się, tworząc nowe, nieprawidłowe odgałęzienia. Zrozumienie tego procesu może otworzyć drogę do mądrzejszych terapii, które nie tylko głodzą guzy, lecz także poprawiają skuteczność immunoterapii.
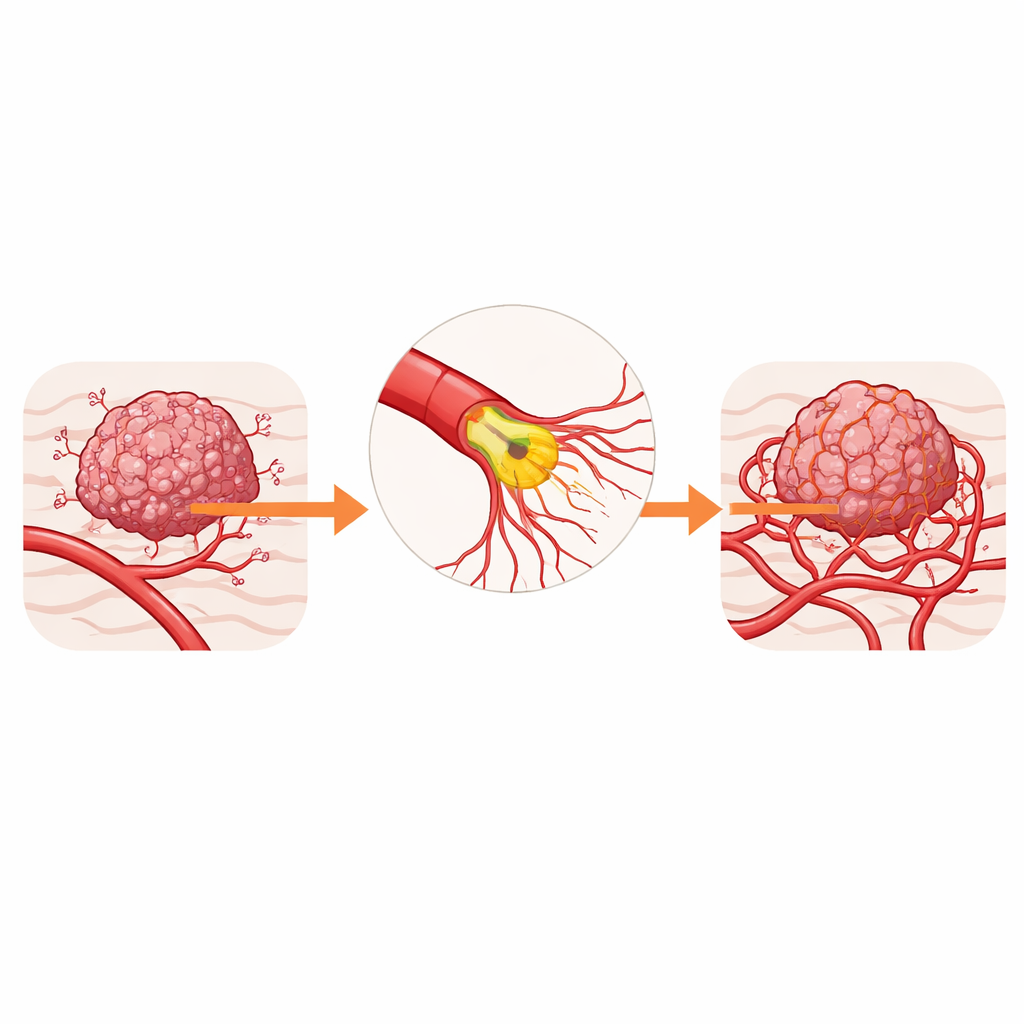
Ukryci architekci unaczynienia guza
Naczynia zasilające guzy zbudowane są ze wyspecjalizowanych komórek zwanych komórkami śródbłonka, które wyściełają wnętrze naczyń. Na czołowym odcinku każdego nowego rozgałęzienia znajduje się „komórka końcowa”, która wysyła długie, palcowate wypustki zwane filopodiami. Wypustki te wyczuwają chemiczne sygnały z guza i kierują wzrost pąków ku obszarom pozbawionym tlenu. W wielu nowotworach proces ten działa nadmiernie, tworząc nieszczelne, skręcone naczynia, które pogłębiają niedotlenienie i utrudniają dotarcie leków oraz komórek odpornościowych do guza.
Białko wzmacniające rozgałęzianie
Analizując pojedyncze komórki z ludzkich guzów płuc, badacze odkryli, że komórki śródbłonka związane z nowotworem silnie aktywują zestaw genów kontrolujących wewnętrzne rusztowanie komórkowe, zwłaszcza białko o nazwie PDLIM5. PDLIM5 występowało w naczyniach nowotworowych częściej niż w naczyniach zdrowych, a pacjenci, których naczynia guza wykazywały wyższe poziomy PDLIM5, mieli tendencję do krótszego przeżycia. W modelach mysich kilku rodzajów nowotworów zwiększenie ekspresji PDLIM5 w śródbłonku przyspieszało wzrost guzów i prowadziło do powstania gęstszych sieci naczyniowych, co sugeruje, że to białko działa jako silny czynnik napędzający rozwój naczyń nowotworowych.
Jak PDLIM5 buduje komórkowe „czujniki”
Aby sprawdzić, jak PDLIM5 wpływa na zachowanie naczyń, zespół skorzystał z systemów eksperymentalnych umożliwiających szczegółową obserwację nowych pąków, takich jak rozwijające się naczynia w siatkówce myszy oraz trójwymiarowe hodowle komórek śródbłonka. Gdy PDLIM5 była usunięta specyficznie w komórkach śródbłonka, pąki rozwijały się wolniej, było mniej komórek końcowych i powstawało znacznie mniej filopodiów. W skali mikroskopowej odkryto, że PDLIM5 łączy dwa kluczowe białka wiążące aktynę, ACTN1 i ACTN4, z długimi włóknami aktyny tworzącymi wewnętrzne rusztowanie komórki. To mostkowanie pomaga upakować włókna aktyny w sztywne pęczki, które podtrzymują filopodia. Mutacje w dwóch krytycznych miejscach PDLIM5 (oznaczonych S593 i F596) zerwały to połączenie, osłabiły wiązanie aktyny i uniemożliwiły PDLIM5 przywrócenie normalnego rozgałęziania, dowodząc, że ta molekularna „piątka” jest niezbędna do budowy komórkowych „czujników” komórki końcowej.
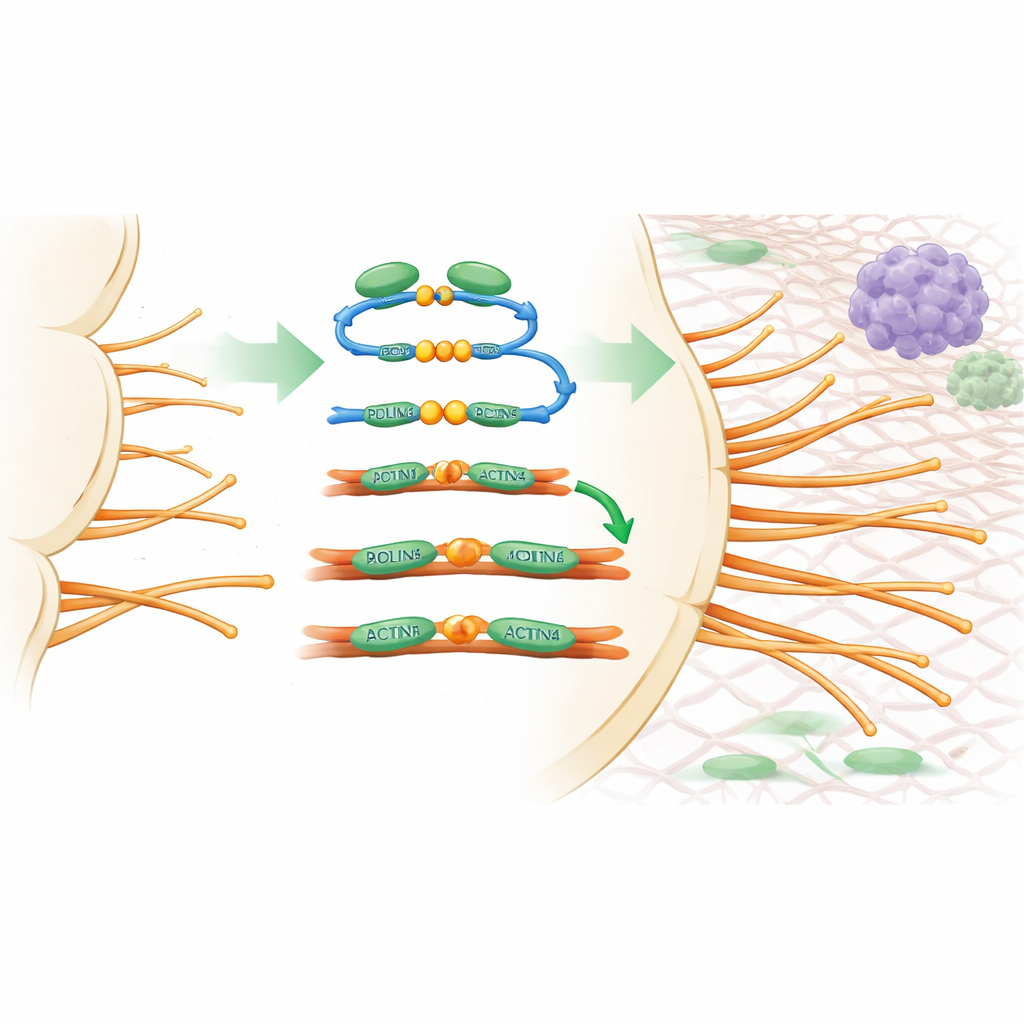
Przebudowa naczyń guza na korzyść układu odpornościowego
Co zaskakujące, zablokowanie PDLIM5 w śródbłonku dało efekty wykraczające poza samo spowolnienie wzrostu guza. Naczynia nowotworowe stały się bardziej regularne w kształcie, mniej nieszczelne i lepiej okryte przez stabilizujące komórki podporowe. W rezultacie poprawiło się dostarczanie tlenu, a obszary ciężkiego niedotlenienia zmniejszyły się. Te bardziej „znormalizowane” naczynia umożliwiły większy napływ komórek T układu odpornościowego do guza. Utrata PDLIM5 zmieniła także organizację cząsteczek adhezyjnych na komórkach śródbłonka, co ułatwiało przyczepianie się komórek T do ścian naczyń i przeciskanie się do tkanki guza. W mysiych guzach, które zwykle opierają się lekom blokującym punkty kontrolne, usunięcie PDLIM5 sprawiło, że leczenie przeciwciałem anty–PD-L1 stało się znacznie skuteczniejsze, zmniejszając guzy i jednocześnie zwiększając liczbę zarówno pomocniczych, jak i cytotoksycznych komórek T w ich wnętrzu.
Dlaczego ma to znaczenie dla przyszłej terapii nowotworów
Podsumowując, wyniki pokazują, że PDLIM5 działa jako centralny organizator rusztowania aktynowego komórki końcowej, umożliwiając intensywne tworzenie filopodiów i szybkie rozgałęzianie naczyń w kierunku guza. Usunięcie lub unieszkodliwienie PDLIM5 w komórkach śródbłonka spowalnia rozrost unaczynienia guza, prostuje i stabilizuje pozostałe naczynia, łagodzi niedobór tlenu i ułatwia napływ komórek odpornościowych do guza. Dla pacjentów sugeruje to, że leki zaprojektowane do zakłócenia partnerstwa PDLIM5–ACTN1/ACTN4 mogłyby zarówno pozbawiać nowotwory nowych naczyń, jak i przekształcać chaotyczne unaczynienie guza w sieć lepiej wspierającą chemioterapię oraz immunoterapię.
Cytowanie: Xu, Z., Shi, Y., Yang, Y. et al. Endothelial PDLIM5 promotes tip cell filopodia formation and tumor angiogenesis by regulating ACTN1/ACTN4-dependent actin bundling. Nat Commun 17, 2103 (2026). https://doi.org/10.1038/s41467-026-68765-x
Słowa kluczowe: angiogeneza nowotworowa, komórki końcowe śródbłonka, PDLIM5, cytoszkielet aktynowy, immunoterapia przeciwnowotworowa