Clear Sky Science · pl
Stabilizowany tandemowy chimera antygenowa wywołująca silną aktywność zmniejszającą transmisję malarii
Dlaczego zatrzymanie transmisji przez komary ma znaczenie
Obecnie stosowane szczepionki przeciwko malarii potrafią znacząco zmniejszyć ciężkie zachorowania i zgony u małych dzieci, jednak pozostawiają istotną lukę: osoby, które nie czują się chore, nadal mogą nosić pasożyty zakażające komary i podtrzymywać transmisję. To badanie przedstawia projekt szczepionki następnej generacji, którego celem nie jest ochrona tylko pojedynczej osoby, lecz przerwanie łańcucha zakażeń między ludźmi a komarami. Poprzez precyzyjne opracowanie sposobu prezentacji kluczowych białek pasożyta układowi odpornościowemu, badacze dążą do wytworzenia przeciwciał, które uczynią komary słabymi gospodarzami dla malarii, pomagając społecznościom zbliżyć się do eliminacji choroby.
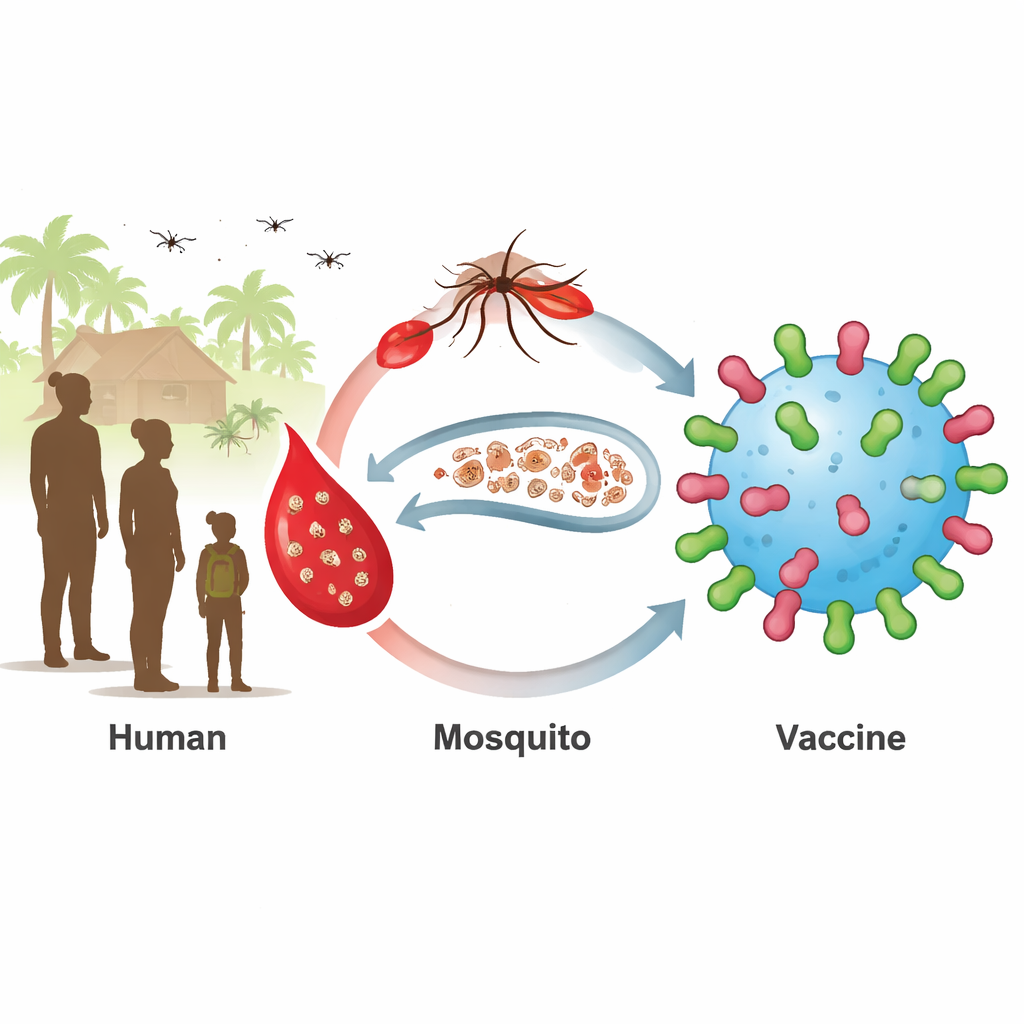
Ukryty rezerwuar, który podtrzymuje malarię
Obecne szczepionki przeciwmalaryczne koncentrują się na wczesnym etapie infekcji w wątrobie i krwi. Działają najlepiej u małych dzieci, ale starsze dzieci i dorośli często noszą dojrzałe, płciowe formy pasożyta, zwane gametocytami, bez objawów. Kiedy komary ukłują takie osoby, pobierają pasożyty i dalej je rozprzestrzeniają. Dwa białka powierzchniowe pasożyta, znane jako Pfs230 i Pfs48/45, znajdują się na tych stadiach i są atrakcyjnymi celami dla tzw. szczepionek blokujących transmisję. Szczepionki przeciw fragmentom tych białek weszły do badań klinicznych, ale miały trudności z wywołaniem silnych i trwałych odpowiedzi przeciwciał u wszystkich biorców.
Budowa sprytniejszej przynęty dla układu odpornościowego
Aby poprawić wcześniejsze projekty, autorzy zastosowali podejście biologii strukturalnej, badając w atomowych szczegółach, jak silne ludzkie przeciwciała wiążą Pfs230 i Pfs48/45. Zidentyfikowali małe regiony, czyli epitopy, które są szczególnie skuteczne w blokowaniu rozwoju pasożyta w komarach. Równie ważne było zmapowanie „niefunkcjonalnych” epitopów, które przyciągają przeciwciała wiążące, lecz niepowstrzymujące transmisji — w praktyce marnujących wysiłek immunologiczny. Wykorzystując modelowanie komputerowe i narzędzia inżynierii białek, połączyli najpotężniejszy region Pfs230 (jego pierwszy domen) z kluczowym regionem Pfs48/45 (jego trzecią domeną) w jednym, starannie ułożonym białku, które nazwali stabilizowaną tandemową chimera antygenową, w skrócie STAC.
Ukrywanie bezużytecznych celów, zachowanie użytecznych
Wyzwanie polegało na zaprezentowaniu tych dwóch domen razem w sposób naśladujący ich ułożenie na pasożycie, jednocześnie fizycznie ukrywając niefunkcjonalne powierzchnie, które normalnie są zakryte w nienaruszonym białku. Zespół iteracyjnie przeprojektowywał krótki łącznik i interfejs między domenami, testując każdą wersję pod kątem stabilności, prawidłowego fałdowania oraz zdolności do wiązania panelu dobrze scharakteryzowanych przeciwciał. Zaawansowane oprogramowanie projektowe sugerowało mutacje wzmacniające interfejs i poprawiające ekspresję w hodowanych komórkach. Badania strukturalne przy użyciu krystalografii rentgenowskiej, małego kąta rozproszenia rentgenowskiego oraz mikroskopii kriogenicznej elektronowej potwierdziły, że w końcowej konstrukcji STAC pożądane epitopy są prezentowane z wysoką wiernością, podczas gdy znane niepomocne miejsca są sterycznie zablokowane.
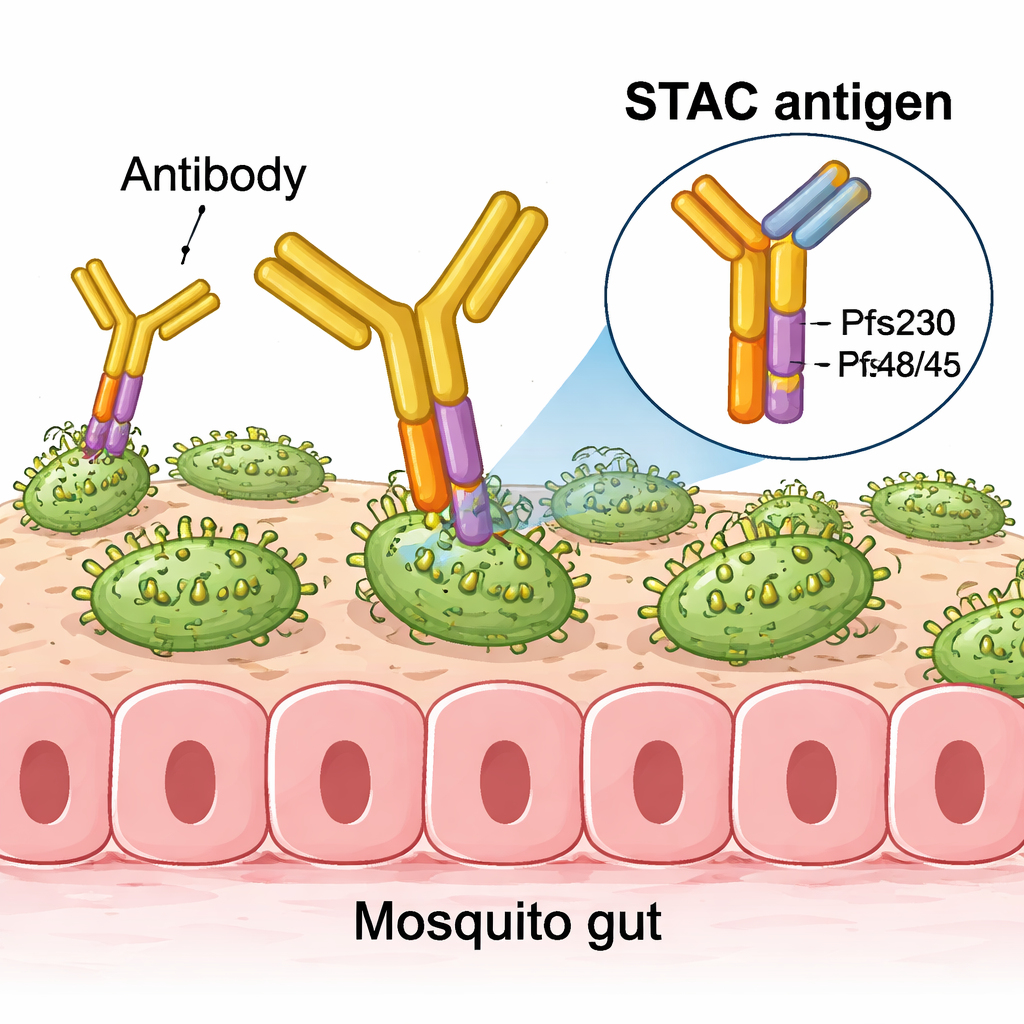
Od pojedynczych cząsteczek do potężnych nanocząstek
Testy na myszach wykazały, że gdy STAC był przyłączony do specjalistycznych liposomów lub do samo składających się nanocząstek białkowych, wywoływał silne odpowiedzi przeciwciał zdolne do znaczącego zmniejszenia rozwoju pasożyta w standardowych testach karmienia komarów. Przy równych lub niższych dawkach STAC często dorównywał lub przewyższał szczepionki wykorzystujące fragmenty Pfs230 i Pfs48/45 osobno — czy to podawane oddzielnie, zmieszane razem, czy współprezentowane na tej samej cząstce. W wysoce czułych testach, gdzie surowicę myszy rozcieńczano wielokrotnie, przeciwciała wywołane przez nanocząstki ozdobione STAC utrzymywały aktywność zmniejszającą transmisję lepiej niż te z innych formulacji, co wskazuje na szczególnie silne i ukierunkowane odpowiedzi.
Co to może znaczyć dla kontroli malarii
Dla nie‑specjalistów kluczowy pomysł jest taki, że STAC to zaprojektowana przynęta, która pokazuje układowi odpornościowemu dokładnie te części pasożyta malarii, które są najważniejsze do powstrzymania rozprzestrzeniania, jednocześnie ukrywając odciągające uwagę regiony, które nie pomagają. W modelach zwierzęcych ten projekt daje przeciwciała utrudniające pasożytom dokończenie cyklu życiowego w komarach, nawet gdy poziomy przeciwciał są stosunkowo niskie. Jeśli podobne wyniki potwierdzą się u ludzi, STAC mógłby stać się potężnym uzupełnieniem istniejących szczepionek przeciwmalarycznych: chroniąc zaszczepione osoby przed chorobą, a jednocześnie zmniejszając zakaźny rezerwuar w społeczności. Szerzej, praca pokazuje, jak szczegółowa wiedza strukturalna i inżynieria białek mogą posłużyć do tworzenia wieloskładnikowych szczepionek, które są skuteczne, stabilne i potencjalnie tańsze w produkcji.
Cytowanie: Ivanochko, D., Miura, K., Hailemariam, S. et al. A stabilized tandem antigen chimera that elicits potent malaria transmission-reducing activity. Nat Commun 17, 2010 (2026). https://doi.org/10.1038/s41467-026-68761-1
Słowa kluczowe: szczepionki przeciwmalaryczne, blokowanie transmisji, Pfs230, Pfs48/45, immunogen nanocząsteczkowy