Clear Sky Science · pl
Kluczowa rola osi NONO–HOXA1–Wnt w różnicowaniu kardiomiocytów
Dlaczego małe komórki serca są ważne dla nas wszystkich
Każde uderzenie serca zależy od miliardów wyspecjalizowanych komórek mięśniowych tworzących się w łonie matki. Gdy ten proces przebiega nieprawidłowo, noworodki mogą przyjść na świat z poważnymi wadami serca. W tym badaniu użyto ludzkich komórek macierzystych, aby odkryć istotny system kontrolny — zbudowany z cząsteczek NONO i HOXA1 oraz znanego sygnału Wnt — który pomaga wczesnym komórkom zdecydować się na los zdrowej tkanki mięśnia sercowego. Zrozumienie tej ukrytej sieci może w przyszłości prowadzić do lepszej diagnostyki i leczenia wad wrodzonych serca.
Od komórek‑pustej karty do wczesnych budowniczych serca
Naukowcy zaczęli od ludzkich indukowanych pluripotencjalnych komórek macierzystych — wszechstronnych komórek, które można nakłonić do przekształcenia się niemal w każdy typ komórki. Standardową procedurą skierowali je w stronę kardiomiocytów, bijących komórek serca. Po usunięciu genu NONO znacznie mniej komórek przyjęło tożsamość sercową. Kluczowe wczesne markery, które normalnie pojawiają się, gdy komórki wychodzą z prymitywnego stanu i zmierzają ku linii sercowej, były zdecydowanie zredukowane. Sekwencjonowanie RNA pojedynczych komórek wykazało, że wiele komórek pozbawionych NONO utknęło w pół drogi, w niedojrzałym stanie przypominającym mezendodermę, zamiast rozwijać się w pełni do postaci mięśnia sercowego.
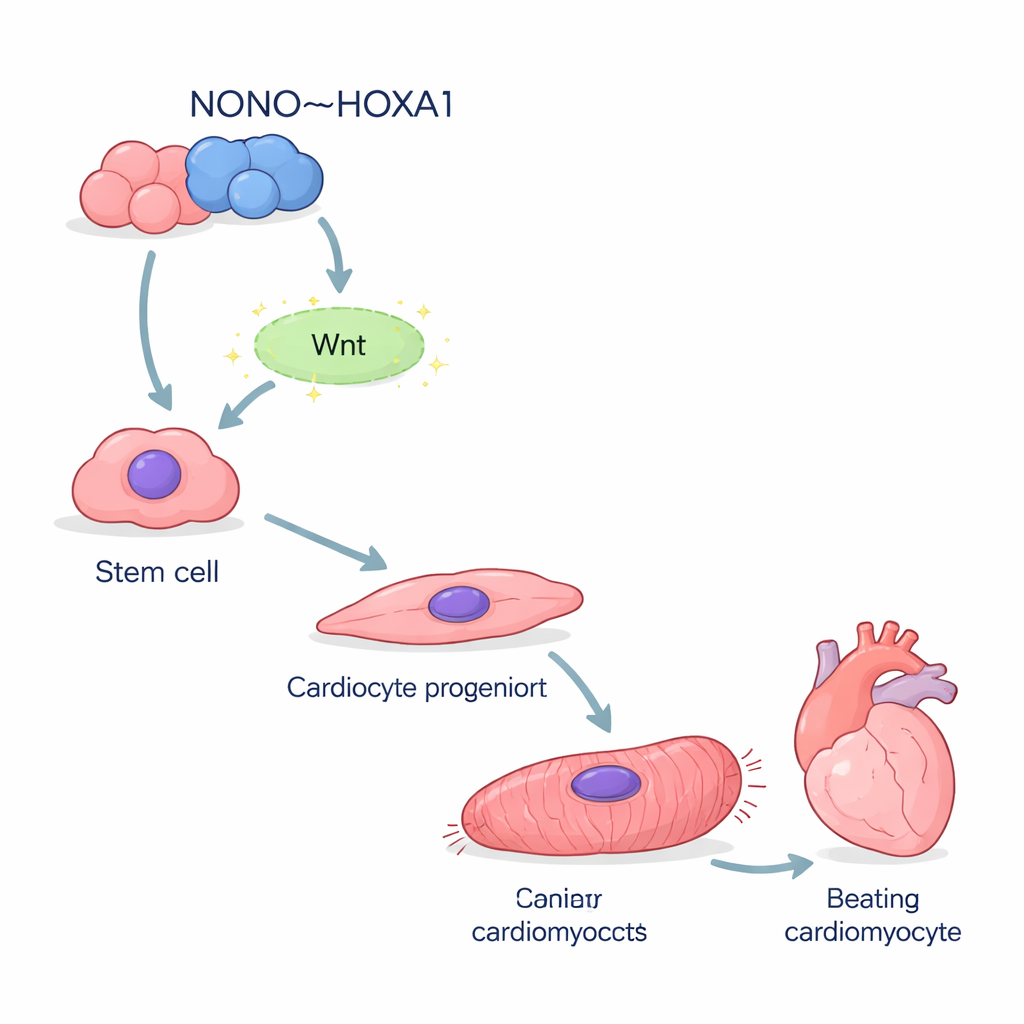
Gdy rusztowanie znika, komórki serca słabną
Te komórki, które mimo braku NONO stały się kardiomiocytami, były dalekie od prawidłowych. Wykazywały znacznie niższe poziomy białek strukturalnych budujących sarkomer — mikroskopową maszynerię napędzającą skurcz. Pod mikroskopem większość mutantów miała zdezorganizowane, pofragmentowane włókna kurczliwe zamiast regularnych prążków widocznych w komórkach normatywnych. Mikroskopia elektronowa potwierdziła, że zwyczajne „poprzeczki” Z‑dysku drabiny kurczliwej były brakujące lub zniekształcone. Funkcjonalnie komórki te biły wolniej i nieregularnie. Pomiary fal wapniowych — zdarzeń elektrycznych wyzwalających każde uderzenie serca — ujawniły nieregularne przebiegi z opóźnionymi szczytami i wolnym powrotem, co odzwierciedlało defekty w ekspresji genów odpowiadających za gospodarkę wapniową.
Ocalenie rozwoju i ujawnienie partnerstwa NONO–HOXA1
Aby sprawdzić, czy te problemy rzeczywiście wynikają z utraty NONO, zespół ponownie wprowadził NONO w kontrolowany, aktywowany lekiem sposób podczas pierwszych dwóch dni różnicowania. Krótkie podanie NONO w dużej mierze przywróciło wzrost wczesnych genów sercowych, zwiększyło odsetek bijących komórek serca i odbudowało zorganizowane sarkomery oraz Z‑dyski. Profilowanie ekspresji genów potwierdziło, że wiele genów związanych ze skurczem mięśni i rozwojem serca powróciło w kierunku poziomów normalnych. Natomiast pochodzące od pacjentów zmutowane wersje NONO nie zdołały uratować fenotypu, co wspiera hipotezę, że takie warianty powodują chorobę przez zakłócenie tego wczesnego programu. Eksperymenty wykazujące interakcje białek ujawniły następnie, że NONO fizycznie wiąże się z czynnikiem transkrypcyjnym HOXA1, a to połączenie stabilizuje HOXA1 i pomaga mu tworzyć dymery niezbędne do wiązania DNA.
Włączanie sygnału Wnt, by zadeklarować los sercowy
Mapowanie miejsc przyłączania tych białek w genomie pokazało, że NONO i HOXA1 często zajmują te same regiony regulacyjne, w tym kontrolujące ważne wczesne geny sercowe oraz geny szlaku Wnt. Gdy brakowało NONO, przyczepność HOXA1 do wielu z tych miejsc osłabła, szczególnie przy genach kierujących przodomozgowym mezenchymem precardiac — najwcześniejszą tkanką tworzącą serce. Dalszy szlak Wnt/β‑kateniny, który normalnie pomaga inicjować powstawanie mezodermy i rozwój serca, był również przytłumiony: mniej β‑kateniny akumulowało się w jądrze, a testy reporterskie reagujące na Wnt wykazywały osłabienie. Wzmocnienie sygnału Wnt przez podwyższenie dawki leku aktywującego Wnt w najwcześniejszych dniach różnicowania mogło częściowo zrekompensować brak NONO, przywracając większą liczbę komórek serca i zwiększając ekspresję genów sercowych.
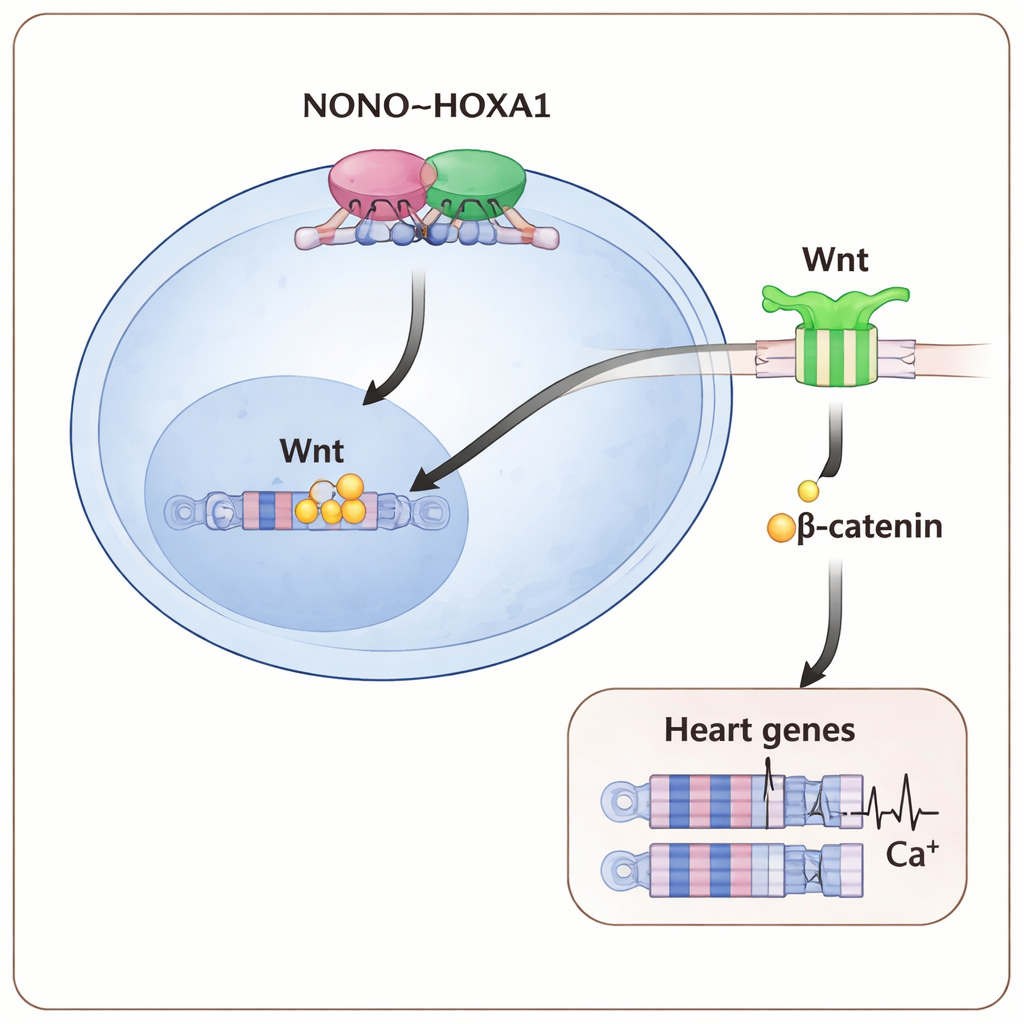
Co to znaczy dla rozumienia wad wrodzonych
Dla osób niezwiązanych z dziedziną główne przesłanie jest takie, że mały zespół molekularny — NONO działające ramię w ramię z HOXA1, dopracowujące sygnały Wnt — działa jak wczesny „regulator ruchu”, który mówi młodym komórkom, by stały się mięśniem sercowym i wyposaża je do prawidłowego bicia. Gdy którąkolwiek część tej osi NONO–HOXA1–Wnt zaburzyć, komórki wstrzymują się, kluczowe geny sercowe pozostają nieaktywne, a powstałe kardiomiocyty są strukturalnie i elektrycznie podatne na uszkodzenia. Te spostrzeżenia dostarczają jaśniejszego wyjaśnienia molekularnego, dlaczego mutacje w NONO wiążą się z wadami wrodzonymi serca, i wskazują możliwości manipulacji tym szlakiem w modelach z komórek macierzystych lub — w przyszłości — w terapii mającej na celu zapobieganie bądź naprawę wad serca.
Cytowanie: Feng, Z., Gao, Y., Gao, H. et al. Essential role of NONO-HOXA1-Wnt axis in cardiomyocyte differentiation. Nat Commun 17, 2013 (2026). https://doi.org/10.1038/s41467-026-68760-2
Słowa kluczowe: wrodzona wada serca, różnicowanie kardiomiocytów, szlak Wnt, modele serca z komórek macierzystych, regulacja genów