Clear Sky Science · pl
Elektrograniczna reaktywność na bodźce współlokalizuje się z głęboką stymulacją jądra półleżącego w przypadku zaburzenia używania opioidów
Dlaczego ta historia ma znaczenie
Uzależnienie od opioidów pozostaje śmiertelną epidemią, a wiele osób nadal zmaga się z silnymi pragnieniami zażycia narkotyku pomimo leków i terapii. Ten artykuł opisuje historię młodego mężczyzny, którego zespół leczniczy użył implantu mózgowego nie tylko do stymulowania mózgu, lecz także do jego słuchania. Znajdując specyficzny sygnał elektryczny związany z jego głodem opioidowym, udało się precyzyjnie dostroić głęboką stymulację mózgu tak, że działała lepiej, przy niższej mocy, i pomogła mu pozostać wolnym od narkotyków.
Słuchając pragnienia
Pacjentem był 25‑letni mężczyzna z długą historią ciężkiego uzależnienia od opioidów, rozpoczynającego się we wczesnej adolescencji, wraz z depresją, lękiem i innymi powikłaniami. Standardowe leczenie, w tym bardzo wysokie dawki metadonu, nie utrzymywały jego głodu pod kontrolą. Lata wcześniej otrzymał głęboką stymulację mózgu (DBS) w rejonie głębokim zwanym jądrem półleżącym, kluczowym węzłem w systemie motywacji i nagrody. Przy włączonej stymulacji jego pragnienia spadły i przez kilka lat pozostawał abstynentem od opioidów. Gdy jednak komplikacja chirurgiczna zmusiła lekarzy do usunięcia baterii, jego pragnienia powróciły w ciągu kilku tygodni, a ryzyko nawrotu gwałtownie wzrosło. To stworzyło rzadką możliwość: elektroda mózgowa mogła zostać tymczasowo podłączona do zewnętrznego sprzętu rejestrującego, pozwalając badaczom bezpośrednio mierzyć aktywność mózgu podczas doświadczania przez niego głodu.
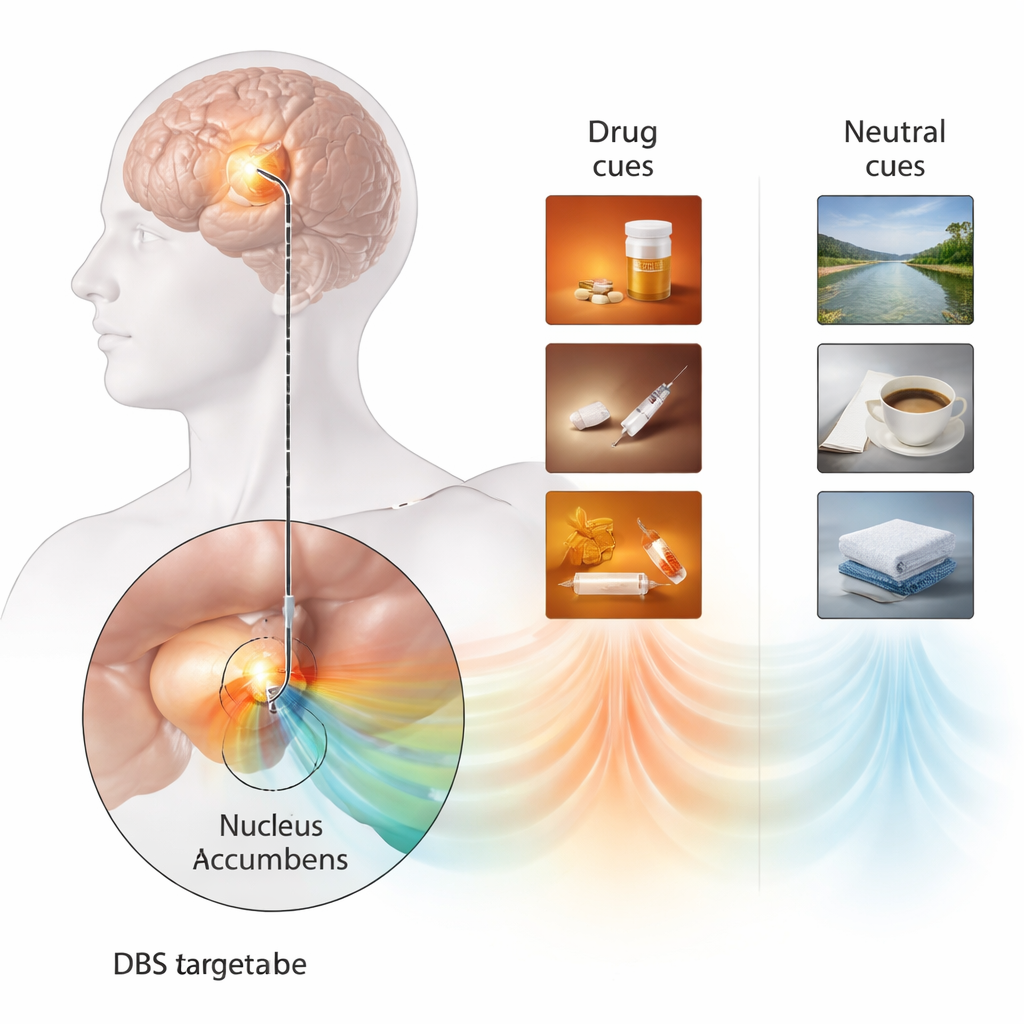
Spersonalizowane wyzwalacze ujawniają sygnał mózgowy
Aby uchwycić, jak wygląda głód w mózgu, zespół stworzył wysoce spersonalizowane zadanie reaktywności na bodźce. Zamiast ogólnych zdjęć narkotyków, przygotowali krótkie filmy ściśle odpowiadające jego przeszłemu używaniu — preferowanemu opioidowi, narzędziom do wstrzykiwania i rytuałom przygotowania — i skontrastowali je z uspokajającymi scenami przyrody. Po każdym sześciosekundowym klipie oceniać miał, jak silne jest jego pragnienie użycia opioidów. Jednocześnie elektroda DBS w jego jądrze półleżącym działała jak maleńki mikrofon, rejestrując lokalne rytmy elektryczne mózgu. Gdy odtwarzano filmy narkotykowe, w części brzusznej jądra półleżącego pojawiał się charakterystyczny rytm niskiej częstotliwości (w zakresie 1–6 Hz), obszar ten uważany jest za odpowiadający podobszarowi „shell”. Sygnał ten był znacznie słabszy podczas filmów neutralnych i nie obserwowano go w innych częściach elektrody. Co ważne, większa moc tego rytmu korelowała z wyższymi samoocenami pragnienia, co sugeruje, że był to bezpośredni marker mózgowy reaktywności na bodźce narkotykowe, a nie ogólny sygnał pobudzenia czy uwagi.
Przekształcanie stymulacji w narzędzie celowane
Kluczowe pytanie brzmiało, czy stymulacja w tym właśnie miejscu może stłumić rytm mózgowy związany z głodem i towarzyszące mu pragnienie. Zespół systematycznie testował różne pary styków elektrody, pytając w czasie rzeczywistym o poziom głodu, nastrój i efekty uboczne, stopniowo zwiększając natężenie stymulacji. Para styków brzusznych, leżąca w „shell” jądra półleżącego, okazała się trafieniem w sedno: dawała silną ulgę w pragnieniu i poprawę nastroju przy stosunkowo niskim prądzie, z minimalnymi efektami ubocznymi. Bardziej grzbietowe pary styków, w pobliskim pęczku włókien zwanym przednią odnogą torebki wewnętrznej, także pomagały, ale wymagały znacznie silniejszej stymulacji i wywoływały nieprzyjemne odczucia. Kierując się tymi testami, badacze powtórzyli zadanie reaktywności na bodźce, dostarczając krótkie impulsy stymulacji skorupki jądra półleżącego przed każdym filmem. W warunku „stymulowanym” wcześniej podwyższony rytm 1–6 Hz podczas bodźców narkotykowych został przyduszony w kierunku poziomów neutralnych, a jego średnie oceny pragnienia zmniejszyły się o ponad połowę.
Trwała zmiana przy lżejszym działaniu
Uzbrojeni w te zbieżne dowody — z anatomii, sygnałów mózgowych i zachowania — klinicyści na stałe przeprogramowali jego wszczepione urządzenie, by stymulowało skoncentrowanie w skorupce jądra półleżącego przy znacznie niższym prądzie niż wcześniej. W ciągu kolejnych sześciu miesięcy zgłaszał utrzymujące się zmniejszenie zarówno częstości, jak i intensywności pragnień opioidowych, utrzymywał abstynencję i spełniał kryteria wczesnej remisji, bez istotnych zmian nastroju, lęku czy energii. Modelowanie sieci mózgowej wykazało, że nowe ustawienia aktywowały mniejszą, bardziej skupioną objętość tkanki, jednocześnie angażując kluczową ścieżkę między jądrem półleżącym a obszarem pod płatami czołowymi zaangażowanym w emocje i wartościowanie. Dzięki większej wydajności stymulacji zapotrzebowanie na baterię zostało znacząco zredukowane, co jest istotną korzyścią dla młodego pacjenta, który prawdopodobnie będzie potrzebował długoterminowej terapii.
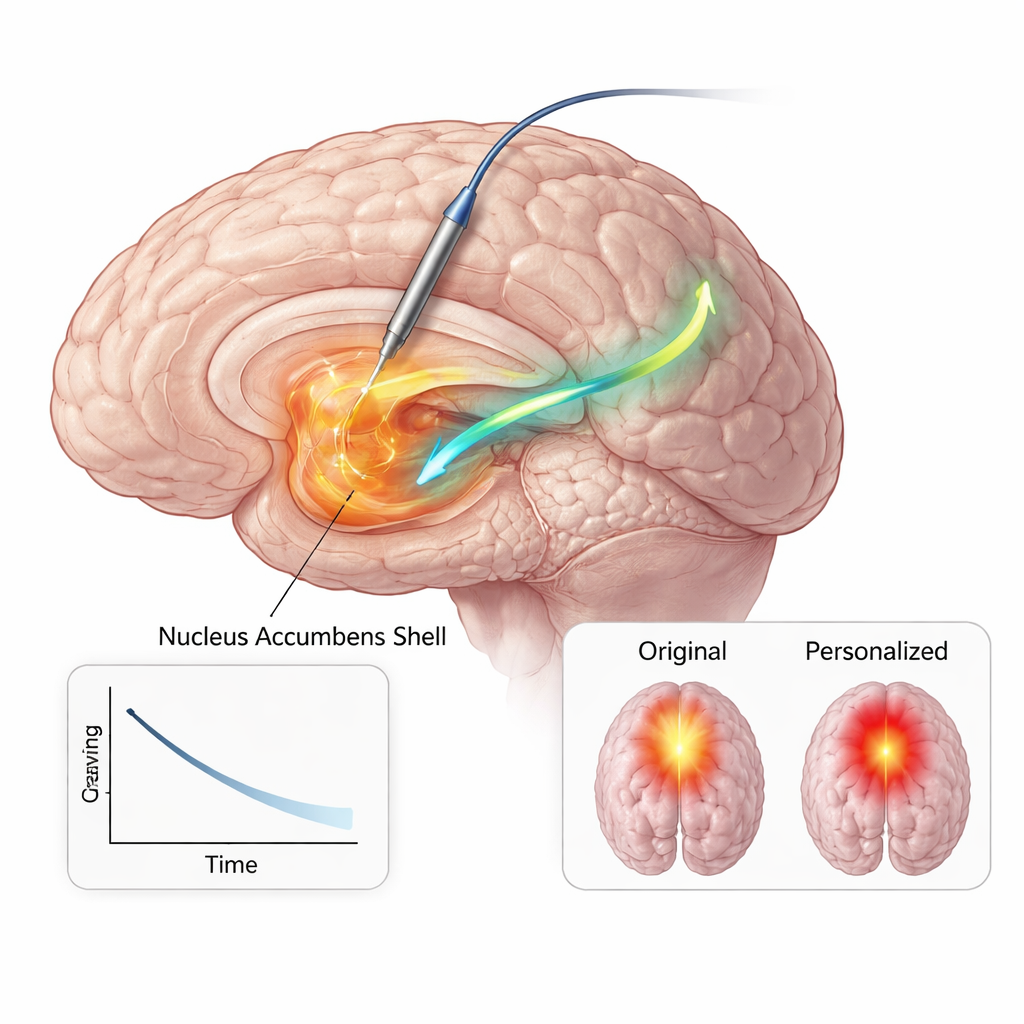
Co to może znaczyć dla przyszłej opieki
Ten przypadek N‑of‑1 nie dowodzi, że takie podejście zadziała u każdej osoby z uzależnieniem od opioidów, ale stanowi dowód zasadności. Pokazuje, że przynajmniej u jednej osoby specyficzny rytm elektryczny w centrum nagrody mózgu ściśle odzwierciedlał pragnienia opioidowe i mógł być wyciszony przez precyzyjnie ukierunkowaną stymulację, prowadząc do trwałej ulgi w objawach przy niższej dawce elektrycznej. Mówiąc prościej, zespół nauczył się „stroić” stymulator względem własnego sygnału głodu pacjenta. Jeśli podobne markery mózgowe zostaną znalezione i śledzone u większej liczby osób, a urządzenia zdolne zarówno do wykrywania, jak i stymulacji staną się szerzej dostępne, przyszłe terapie mogą spersonalizować stymulację mózgu dla uzależnień — reagując, gdy obwody pragnienia się aktywują, i potencjalnie pomagając ludziom wyprzedzać nawroty.
Cytowanie: Qiu, L., Nho, YH., Seilheimer, R.L. et al. Electrographic cue-reactivity co-localizes with accumbens deep brain stimulation in a case of opioid use disorder. Nat Commun 17, 1708 (2026). https://doi.org/10.1038/s41467-026-68758-w
Słowa kluczowe: uzależnienie od opioidów, głęboka stymulacja mózgu, jądro półleżące, biomarkery mózgowe, głód narkotykowy