Clear Sky Science · pl
Strukturalne podstawy odwracania widełek i regulacji RAD51 przez kompleks ligazy ubikwitynowej SCF z helikazą F-box FBH1
Jak komórki ratują zatrzymaną maszynerię kopiującą DNA
Za każdym razem, gdy komórka się dzieli, musi szybko i dokładnie skopiować miliardy liter DNA. Jednak ta maszyna kopiująca często napotyka problemy — uszkodzenia DNA, trudno przepisywalne sekwencje lub leczenie lekami mogą spowodować zatrzymanie procesu. W takich sytuacjach komórki polegają na zespołach naprawczych, które stabilizują i restartują widełki replikacyjne. W artykule przedstawiono, z niespotykaną dotąd szczegółowością strukturalną, jak jeden z takich liderów — kompleks białkowy zbudowany wokół helikazy FBH1 — przeformowuje zatrzymane DNA i utrzymuje pod ścisłą kontrolą inny kluczowy białkowy czynnik naprawczy, RAD51. Zrozumienie tej choreografii pomaga wyjaśnić, jak komórki unikają niebezpiecznych pęknięć genomu i dlaczego zaburzenia w tych czynnikach wiążą się z rakiem.
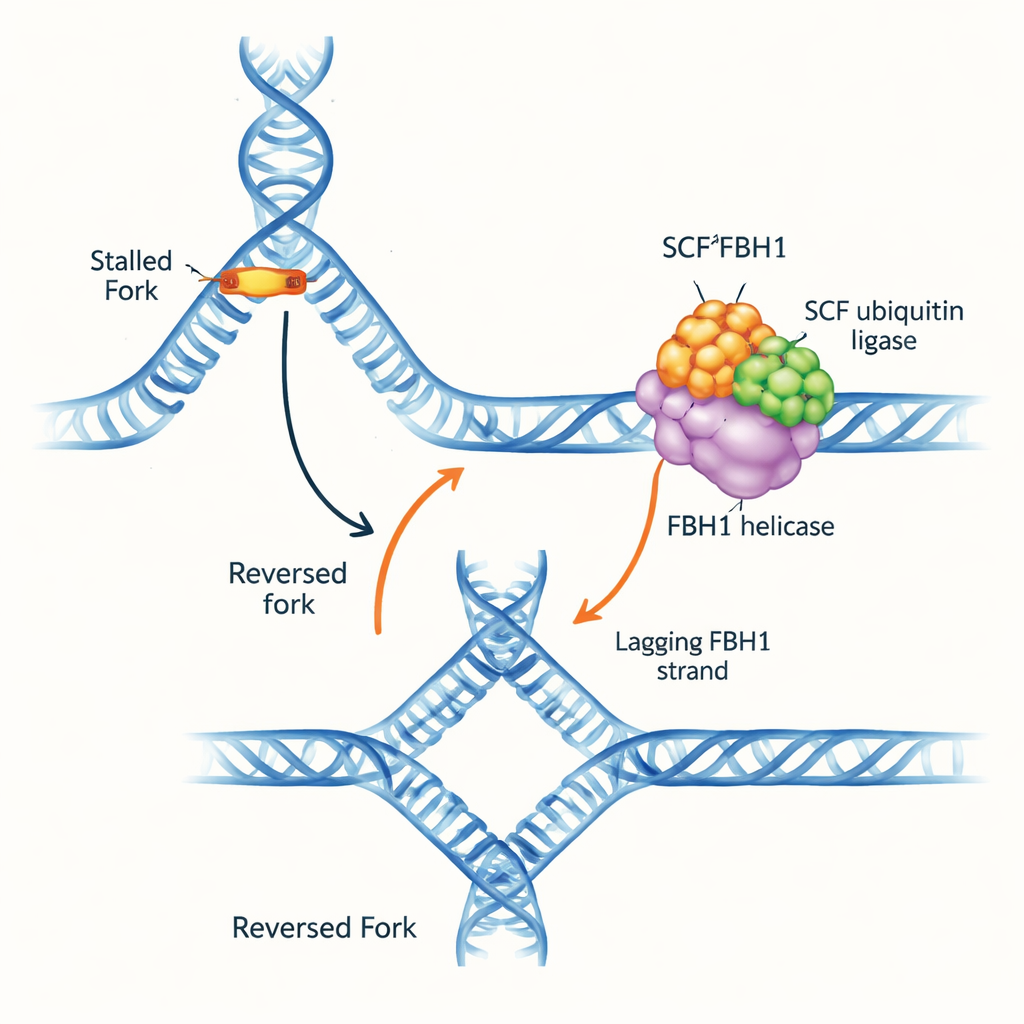
Korek na autostradzie DNA
Widełki replikacyjne DNA to struktury w kształcie litery Y, gdzie podwójna helisa jest rozwijana i kopiowana. Gdy widełka napotyka przeszkodę, może cofnąć się: nici rodzicielskie ponownie się zespajają, a nowo zsyntetyzowane nici łączą się ze sobą, tworząc czterodrogowe złącze DNA. To „odwracanie widełek” może zyskać czas na naprawę i bezpieczne wznowienie replikacji, ale jeśli jest źle zarządzane, tworzy kruche miejsca w DNA, które mogą pękać. Kilka molekularnych „silników” jest znanych z wykonania cofania widełek, chwytając za podwójną helisę przed widełką. FBH1 wyróżniał się jednak, ponieważ zachowuje się inaczej i często jest zmieniany w nowotworach, co sugeruje, że działa przez odrębną, istotną medycznie ścieżkę.
Specjalista od widełek z ulubioną stroną
Autorzy wyizolowali ludzki kompleks SCFFBH1, łączący helikazę FBH1 z modułem znakującym ubikwityną (SCF). Najpierw sprawdzili, jakie kształty DNA preferuje FBH1. Wykorzystując testy wiązania i rozwijania nici, pokazali, że SCFFBH1 wyraźnie preferuje rzeczywiste struktury przypominające widełki, zwłaszcza gdy na matrycy „opóźnionej” (kopiowanej fragmentarycznie) występuje krótki odcinek jednoniciowy. Na takich strukturach FBH1 rozwija DNA setki razy szybciej niż na prostym, luźnym końcu, co wskazuje, że właściwe zakotwiczenie się przy złączu widełek znacznie zwiększa aktywność jego silnika. Badania pojedynczych cząsteczek przy użyciu magnetycznych pęset potwierdziły, że kompleks może rozwijać, a następnie przemieszczać się wzdłuż nici jednoniciowej przez tysiące nukleotydów bez odpadania, działając jako potężny, procesywny motor.
Odwracanie widełek przez pociągnięcie od tyłu
Aby ustalić, jak ten motor faktycznie odwraca widełki, zespół badał sztuczne podłoża widełkowe z przerwami jednoniciowymi lub bez nich. W odróżnieniu od innych remodelatorów widełek, SCFFBH1 nie mógł działać na w pełni sparowanej widełce; wymagał przerwy na matrycy opóźnionej i poruszał się w kierunku 3′–5′ wzdłuż tej pojedynczej nici. Ten ruch „ciągnięcia od tyłu” skłania nici rodzicielskie do ponownego zespajania się, podczas gdy enzym pozostaje zakleszczony w złączu widełek. Struktura SCFFBH1 związana z zatrzymaną widełką, uzyskana metodą krioglobinowej mikroskopii elektronowej, pokazuje mechanizm: specjalna dodatnio naładowana powierzchnia — „motyw wiążący złącze” w jednej poddomenie FBH1 — osadza się dokładnie w punkcie rozgałęzienia, gdzie spotykają się trzy ramiona DNA. Gdy badacze zmienili dwa kluczowe aminokwasy w tym motywie, odwracanie widełek w próbówkach spadło około 25-krotnie, chociaż podstawowy mechanizm rozwijania nadal działał stosunkowo dobrze. W komórkach ta sama mutacja uniemożliwiła normalne spowolnienie widełek replikacyjnych w reakcji na lek wywołujący stres — cechę typową dla nieudanego odwracania widełek.
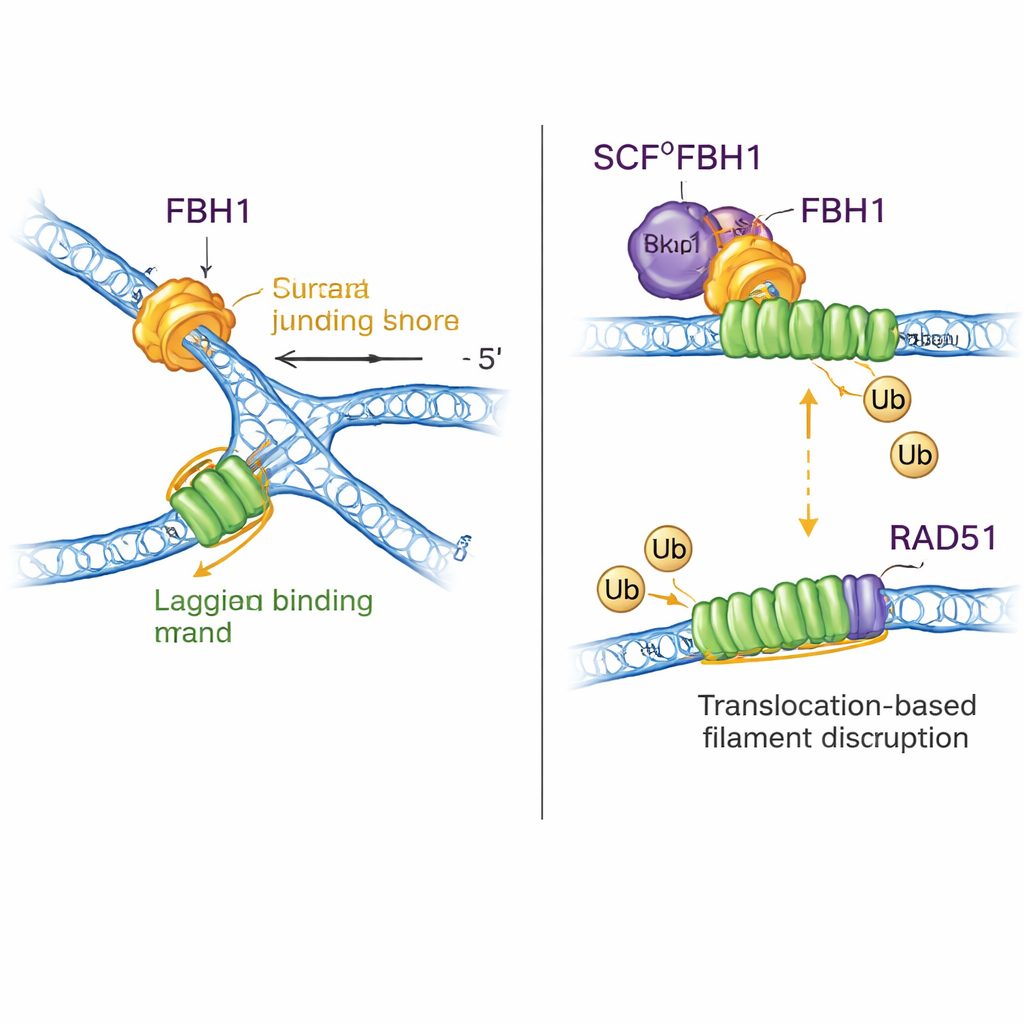
Podwójna rola: przeformowywanie DNA i usuwanie RAD51
FBH1 to nie tylko motor; w ramach kompleksu SCF pomaga też przyłączać małe znaczniki ubikwitynowe do białek. Nowe struktury składają prawie cały kompleks SCFFBH1–DNA i pokazują, że „głowa” transferująca ubikwitynę ligazy znajduje się mniej niż 45 angstremów od nici opóźnionej wychodzącej z FBH1. Poprzez dokowanie znanych struktur innych ligaz ubikwitynowych autorzy proponują, że taka geometria ustawia RAD51 — enzym tworzący filamenty na DNA, promujący rekombinację — dokładnie na linii ognia na nici opóźnionej zatrzymanej widełki. Wcześniejsze prace wykazały, że FBH1 mechanicznie zdejmuje RAD51 z DNA i jednocześnie może go znakować ubikwityną, aby ten nie wiązał się ponownie łatwo. Nowy model jednoczy te pomysły: gdy FBH1 ciągnie wzdłuż nici opóźnionej, przeformowując widełkę, sąsiedni moduł SCF może znakować podjednostki RAD51, pomagając demontować lub zapobiegać nadmiernym filamentom RAD51, które w przeciwnym razie blokowałyby prawidłowe przetwarzanie widełek.
Co to oznacza dla stabilności genomu i raka
W sumie badanie pokazuje, że SCFFBH1 odwraca zatrzymane widełki replikacyjne za pomocą mechanizmu odrębnego od innych znanych remodelatorów: mocno chwyta punkt rozgałęzienia, przemieszczając się wzdłuż matrycy opóźnionej od tyłu, co sprzyja bezpiecznemu ponownemu spleceniu nici rodzicielskich bez tworzenia długotrwałego, ruchomego czterodrogowego złącza. Jednocześnie wbudowana ligaza ubikwitynowa jest strategicznie ustawiona, by usuwać RAD51 z tej samej nici, zapobiegając niekontrolowanej rekombinacji podczas stresu replikacyjnego. Ponieważ FBH1 jest często tracony lub zmutowany w nowotworach, te strukturalne i mechanistyczne wnioski pomagają wyjaśnić, jak takie guzy kumulują uszkodzenia DNA i dlaczego mogą różnie reagować na leki wywołujące stres replikacyjny lub celujące w powiązane szlaki.
Cytowanie: Greer, B.H., Mendia-Garcia, J., Mullins, E.A. et al. Structural basis for fork reversal and RAD51 regulation by the SCF ubiquitin ligase complex of F-box helicase 1. Nat Commun 17, 2041 (2026). https://doi.org/10.1038/s41467-026-68752-2
Słowa kluczowe: stres replikacji DNA, odwracanie widełek, helikaza FBH1, regulacja RAD51, stabilność genomu