Clear Sky Science · pl
Zautomatyzowane mapowanie postępu wideł replikacyjnych DNA w komórkach ludzkich za pomocą ForkML
Dlaczego ważne jest śledzenie szybkości kopiowania DNA
Przy każdym podziale komórki ludzkiej trzeba szybko i precyzyjnie przepisać ponad trzy miliardy liter DNA. Jeśli ten proces spowalnia lub zastyga, może to uszkodzić genom i przyczyniać się do powstawania nowotworów oraz zaburzeń rozwojowych. Do tej pory naukowcy nie mieli prostego sposobu, by zobaczyć dokładnie, jak szybko poszczególne „mechanizmy kopiujące” poruszają się wzdłuż konkretnych odcinków ludzkiego DNA. Artykuł prezentuje ForkML — nową metodę, która wykorzystuje sekwencjonowanie nanopore i uczenie maszynowe do zautomatyzowanego pomiaru tego procesu w niespotykanej dotąd skali.
Obserwowanie „maszyn kopiujących” komórki w praktyce
DNA jest duplikowane przez maleńkie molekularne „widełki” replikacyjne, które przesuwają się wzdłuż podwójnej helisy, tworząc nowe nici. ForkML pozwala badaczom obserwować te widełki pośrednio — przez wprowadzenie nieszkodliwego znacznika chemicznego, BrdU, do nowo syntetyzowanego DNA w dwóch bardzo krótkich impulsach rozdzielonych stałym odstępem czasu. Ponieważ BrdU można wykryć w pojedynczych cząsteczkach DNA za pomocą sekwencerów nanopore, naukowcy widzą na każdej nici dwa „paski” z znacznikiem, odpowiadające przejściu widełek podczas dwóch impulsów. Mierząc odległość między tymi paskami i dzieląc przez znany odstęp czasowy, mogą obliczyć, jak szybko poruszała się dana widełka w tym fragmencie genomu. 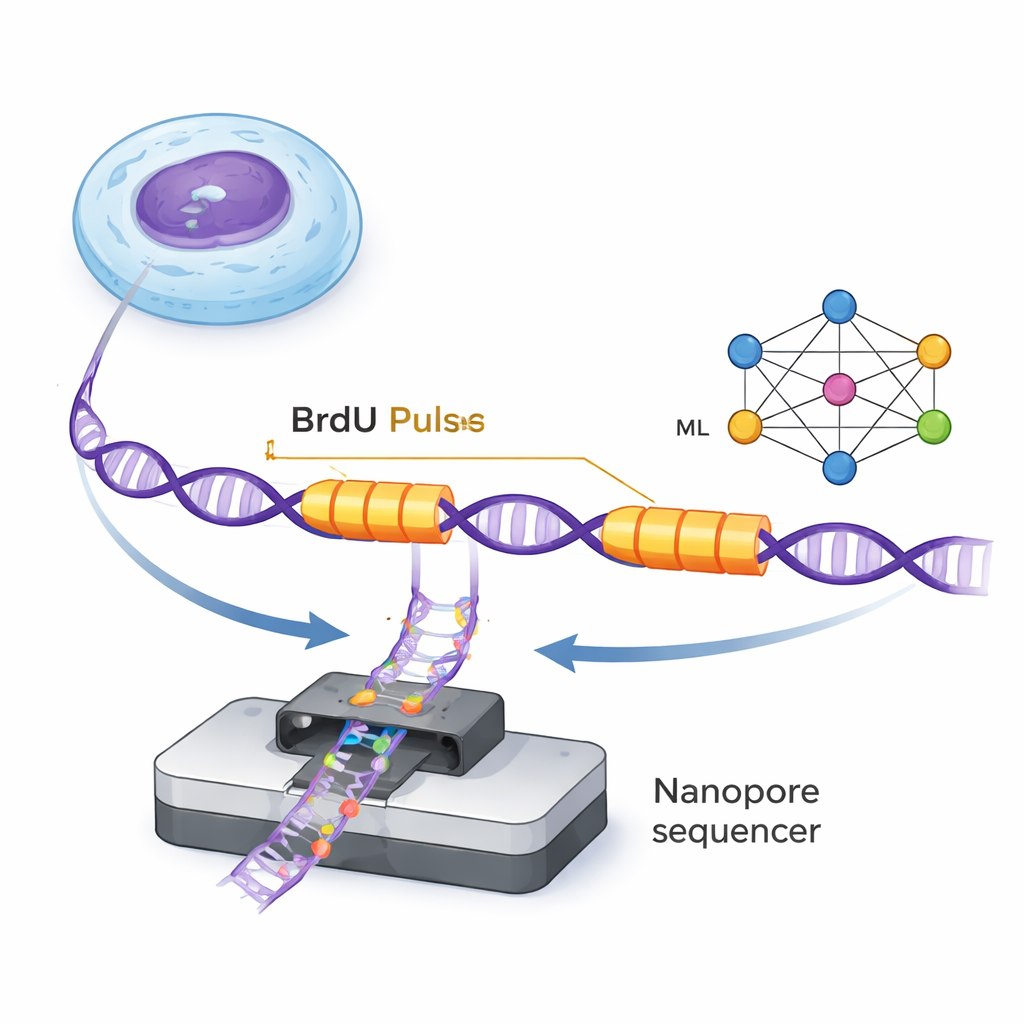
Nauka komputera czytania chemicznych śladów
W wcześniejszych pracach na drożdżach autorom udawało się wykrywać te ślady BrdU prostymi regułami, ale w komórkach ludzkich sygnały są słabsze i bardziej złożone. Eksperci nadal potrafią rozpoznać charakterystyczny wzorzec — gwałtowny wzrost obecności BrdU na początku impulsu, a potem łagodne obniżenie po wypłukaniu — ale ręczna analiza milionów fragmentów DNA jest niemożliwa. ForkML rozwiązuje ten problem, trenując sieć neuronową, formę uczenia maszynowego, na tysiącach ręcznie oznaczonych przykładów. Model uczy się klasyfikować każdy fragment DNA jako tło lub jako widełkę poruszającą się w prawo lub w lewo oraz bardzo dokładnie wyznaczać początek każdego impulsu BrdU. Dzięki temu można w pełni zautomatyzować mapowanie tysięcy indywidualnych pomiarów prędkości widełek z jednego przebiegu sekwencjonowania.
Pomiary stresu replikacyjnego i różnic w genomie
Stosując ForkML w linii komórkowej raka jelita grubego, zespół uzyskał ponad 2000 pomiarów prędkości widełek na eksperyment i stwierdził, że typowa widełka porusza się z prędkością około 1,2 kilobaza na minutę, co zgadza się z wcześniejszymi, mniej wydajnymi metodami. Gdy komórki potraktowano lekami znanymi z tego, że spowalniają replikację DNA, ForkML wyraźnie wykrył to spowolnienie, dowodząc, że metoda czułe mierzy stres replikacyjny. Ponieważ każda widełka jest mapowana z powrotem do pozycji w genomie referencyjnym, autorzy mogli powiązać prędkość z innymi cechami — na przykład z momentem, kiedy dany region normalnie replikuje się w cyklu komórkowym, z gęstością upakowania chromatyny oraz z aktywnością transkrypcyjną. 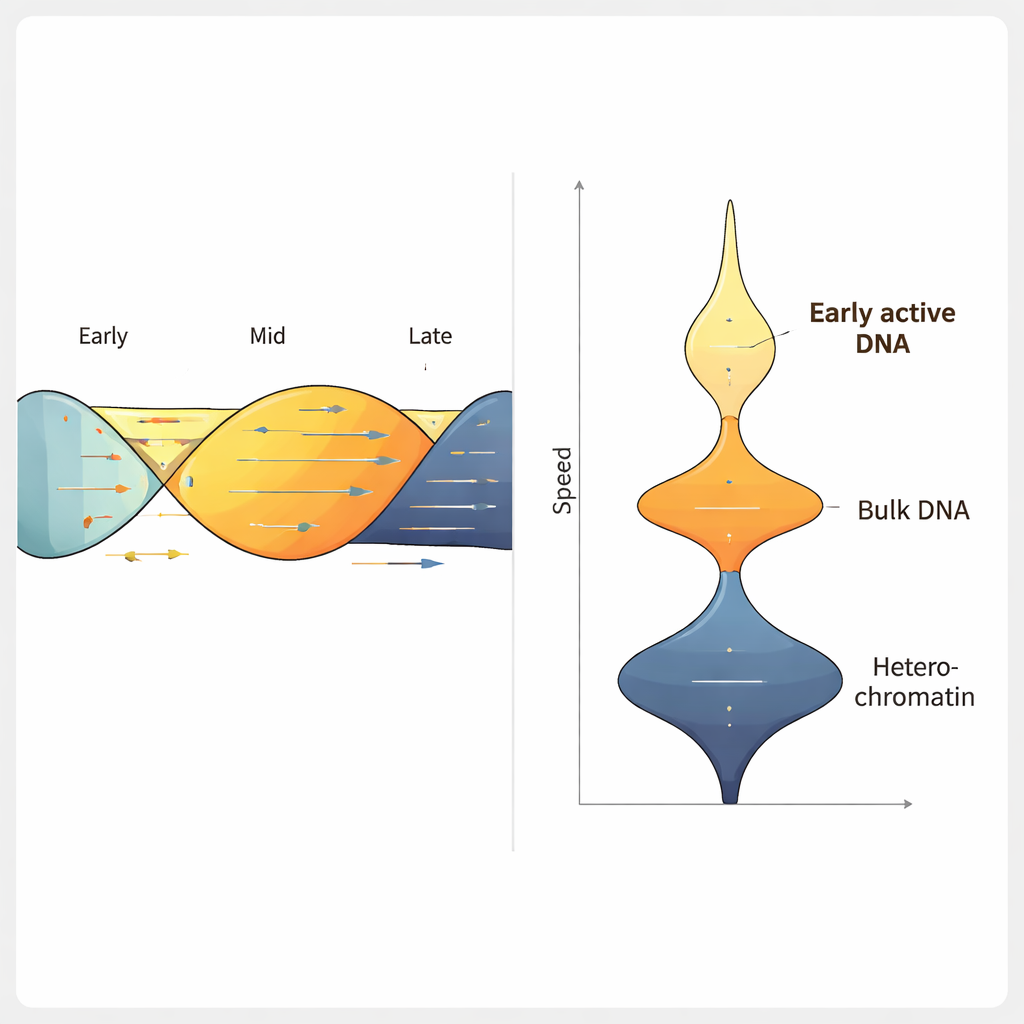
Ujawnianie miejsc startu replikacji i różnic między nićmi
Poza prędkością ForkML identyfikuje także miejsca, gdzie replikacja DNA się zaczyna i kończy, wykrywając punkty, w których widełki rozchodzą się lub zbliżają na tej samej cząsteczce. Mapując ponad 20 000 takich miejsc startu, autorzy potwierdzają, że komórki ludzkie stosują strategię mieszaną: część inicjacji zachodzi w dobrze zdefiniowanych strefach startowych, ale większość początków jest rozproszona po genomie. Łącząc kierunek ruchu widełki z informacją, która nić DNA została odczytana przez sekwencer, ForkML potrafi też rozróżnić tempo syntezy nici wiodącej i opóźnionej — coś, czego tradycyjne testy na włóknach nie umożliwiają. Testy na sześciu różnych liniach komórkowych ludzkich — zarówno prawidłowych, jak i nowotworowych — pokazują, że te same proste warunki znakowania BrdU działają szeroko i dostarczają wiarygodnych oszacowań prędkości w każdym przypadku.
Cyfrowa modernizacja klasycznej techniki
Dla nie-specjalistów ForkML można uznać za nowoczesną, cyfrową wersję klasycznego testu na włóknach DNA: stosuje podobne oznakowanie, ale zastępuje ręczną mikroskopię długodystansowym sekwencjonowaniem i uczeniem maszynowym. To zapewnia znacznie większą wydajność, bezpośrednie umiejscowienie każdego pomiaru w genomie oraz bardziej szczegółowe informacje o tym, gdzie i jak szybko kopiowane jest DNA. Ponieważ protokół jest prosty, zgodny z obecną aparaturą nanopore i łatwy do dostosowania do innych organizmów, ForkML ma szansę stać się standardowym narzędziem do badania replikacji DNA. W praktyce daje badaczom potężny sposób na powiązanie lokalnej prędkości kopiowania DNA — w stanie prawidłowym lub poddanym stresowi — z aktywnością genów, stanem chromatyny i zmianami w genomie związanymi z chorobami.
Cytowanie: Rojat, V., Ciardo, D., Tourancheau, A. et al. Automated mapping of DNA replication fork progression in human cells with ForkML. Nat Commun 17, 1975 (2026). https://doi.org/10.1038/s41467-026-68750-4
Słowa kluczowe: replikacja DNA, prędkość wideł replikacyjnych, sekwencjonowanie nanopore, znakowanie BrdU, uczenie maszynowe w genomice