Clear Sky Science · pl
Proteogenomiczny atlas 1032 przerzutów do mózgu identyfikuje podtypy molekularne, krajobrazy immunologiczne i wrażliwości terapeutyczne
Dlaczego nowotwory szerzą się do mózgu
W miarę poprawy opieki onkologicznej coraz więcej osób żyje na tyle długo, że ich guzy mają szansę rozsiać się w nowe lokalizacje, w tym do mózgu. Te przerzuty do mózgu są teraz częstym i często wyniszczającym powikłaniem, a mimo to lekarze nadal najczęściej leczą je głównie według miejsca powstania pierwotnego guza — płuca, piersi, skóry, jelita — zamiast według tego, jak nowotwór zaadaptował się do życia w mózgu. W tym badaniu zbudowano szczegółowy „atlas” ponad tysiąca przerzutów do mózgu, aby zrozumieć ich ukrytą biologię, interakcje z komórkami mózgu i układem odpornościowym oraz gdzie mogą leżeć nowe możliwości terapeutyczne.
Budowanie ogromnej mapy guzów mózgu
Naukowcy zebrali dane z 1032 przerzutów do mózgu pochodzących z różnych nowotworów pierwotnych, wraz z kilkudziesięcioma dopasowanymi guzami pierwotnymi i kilkoma agresywnymi pierwotnymi nowotworami mózgu do porównania. Połączyli kilka nowoczesnych podejść: sekwencjonowanie DNA i RNA, szeroko zakrojone pomiary białek i metabolitów, mapowanie jednego poziomu komórkowego i przestrzennego komórek nowotworowych i odpornościowych oraz miniaturowe organoidy pochodzące od pacjentów hodowane w laboratorium. Integrując wszystkie te warstwy, dążyli nie tylko do spisu genów, lecz do zobaczenia, jak całe systemy biologiczne zachowują się w przerzutach do mózgu.
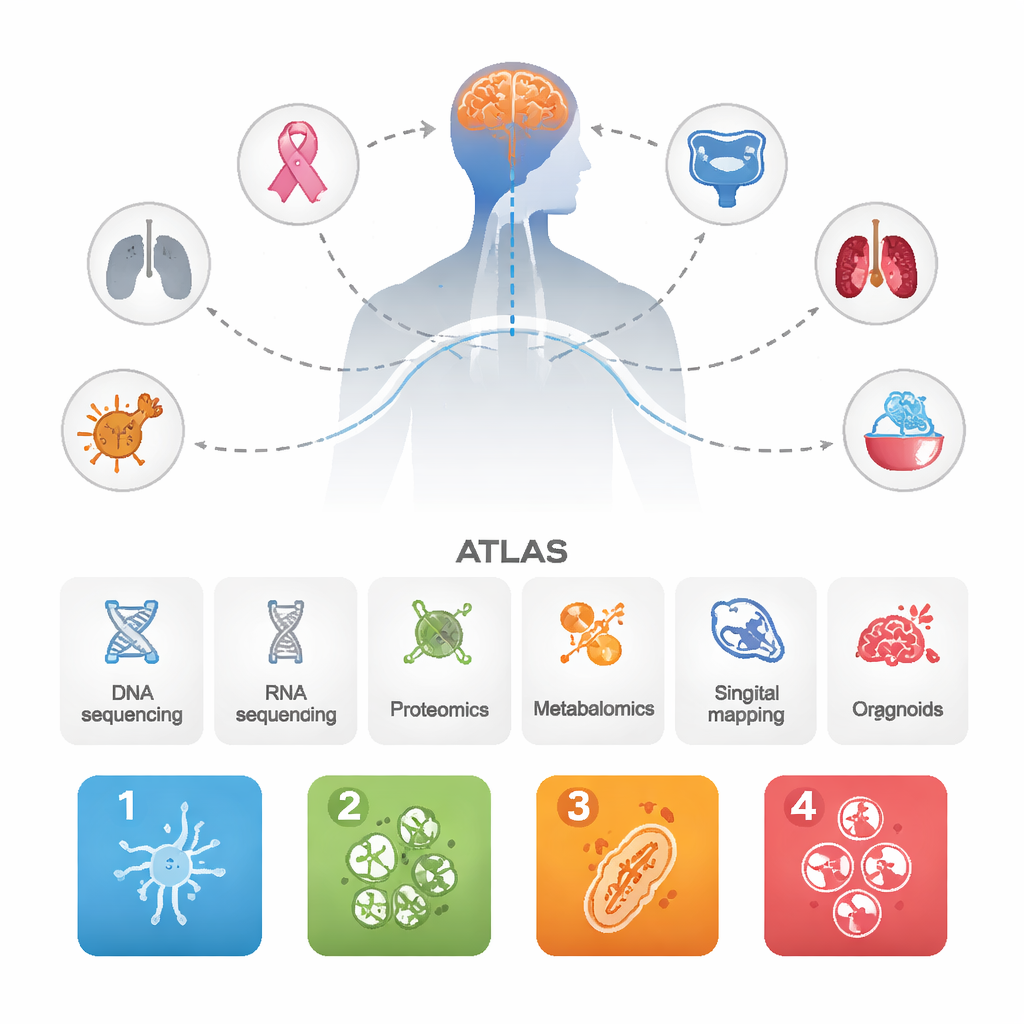
Cztery powtarzające się „osobowości” przerzutów do mózgu
Mimo pochodzenia z różnych narządów, przerzuty do mózgu wielokrotnie układały się w cztery główne podtypy molekularne. Pierwszy, nazwany BrMS1, ma charakter „neuronalny”: komórki nowotworowe i otaczająca tkanka wykazują wiele programów typowych dla mózgu i komórek nerwowych oraz względnie aktywny nadzór immunologiczny. BrMS2 to podtyp „zagospodarowany przez układ odpornościowy” — wypełniony komórkami odpornościowymi, szczególnie limfocytami T, i wykazujący program znany jako przejście nabłonkowo-mezenchymalne (EMT), który rozluźnia przyleganie komórek i przekształca lokalne środowisko. BrMS3 to podtyp „metaboliczny”, zdominowany przez wysoce aktywne komórki nowotworowe, które przeorganizowują swoje wykorzystanie energii — spalając paliwo ścieżkami takimi jak metabolizm kwasów tłuszczowych i fosforylacja oksydacyjna. BrMS4 to podtyp „proliferacyjny”, charakteryzujący się szybkim dzieleniem komórek, cechami przypominającymi komórki macierzyste i dużą niestabilnością genomową, ale uderzająco niską liczbą komórek odpornościowych.
Co ujawnia środowisko guza
Dzięki przybliżeniu na poziomie pojedynczych komórek i kontekstu przestrzennego zespół wykazał, że każdy podtyp osiedla się w odrębnym „sąsiedztwie” w mózgu. Zmiany BrMS1 są bogate w komórki wspomagające mózg, takie jak astrocyty i neurony, co sugeruje, że guz naśladuje i wykorzystuje normalną tkankę mózgową. Guzy BrMS2 natomiast są usiane gęstymi skupiskami limfocytów T, w tym wieloma „wygaszonymi” komórkami T wyrażającymi cząsteczki kontrolne jak PD-1, oraz mają aktywowane naczynia krwionośne i sygnały zapalne. Zmiany BrMS3 występują w strefach o intensywnym metabolizmie, podczas gdy BrMS4 tworzą wyspy szybko dzielących się komórek otoczone stosunkowo ubogim w komórki odpornościowe terenem. W całym badaniu stwierdzono, że w przerzutach do mózgu — ale nie w guzach pierwotnych — silna aktywacja przejścia nabłonkowo-mezenchymalnego często idzie w parze z większą infiltracją limfocytów T, co sugeruje, że ten program może pomagać otworzyć drogę dla komórek odpornościowych.
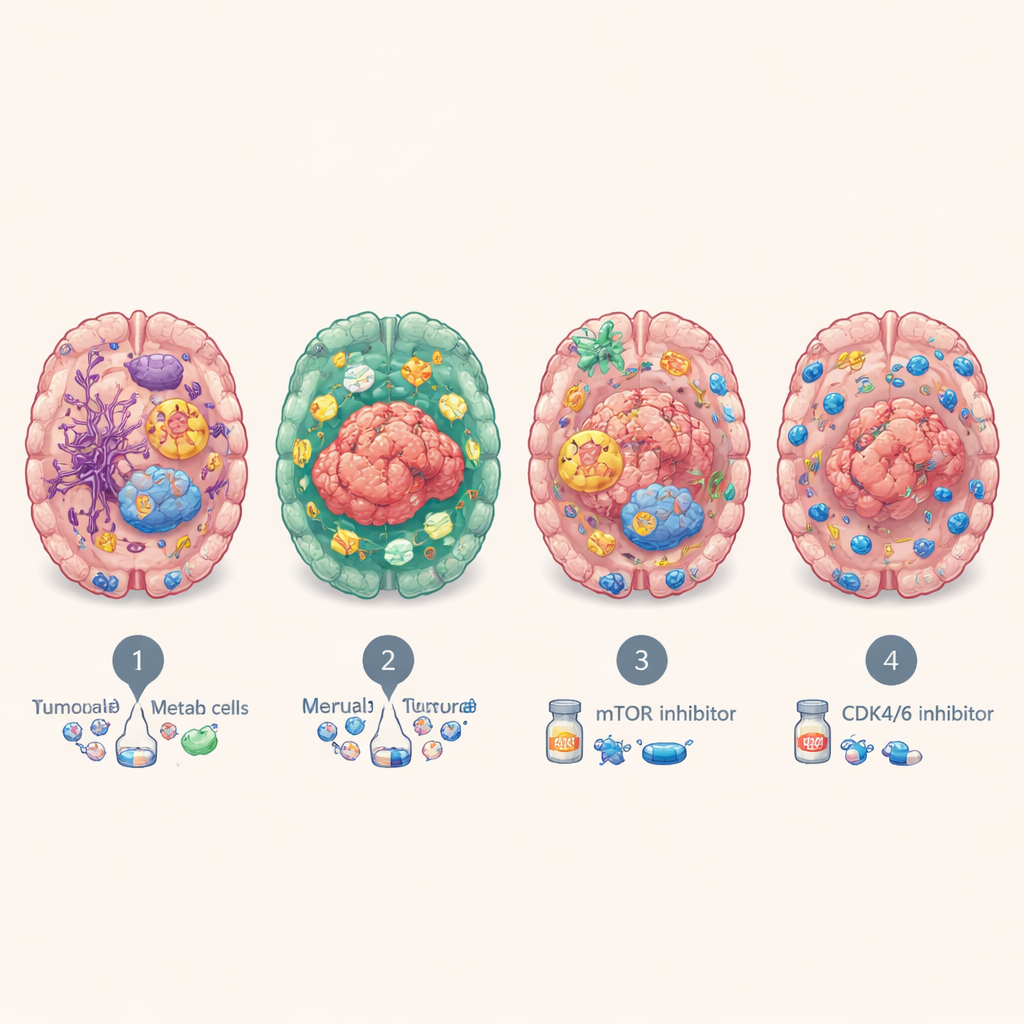
Wskazówki dotyczące leczenia i wyników pacjentów
Te molekularne „osobowości” miały znaczenie praktyczne. Pacjenci z immunologicznie zagospodarowanym podtypem BrMS2 mieli tendencję do dłuższego przeżycia niż ci z proliferacyjnym podtypem BrMS4, który konsekwentnie wiązał się z najgorszymi wynikami. Testując leki na organoidach pochodzących od pacjentów, zespół odkrył, że guzy metaboliczne BrMS3 były szczególnie wrażliwe na blokowanie ścieżki sygnałowej mTOR, która kontroluje wzrost komórek i metabolizm, natomiast szybko dzielące się guzy BrMS4 były bardziej podatne na inhibitory CDK4/6 — leki hamujące cykl komórkowy. Osobne analizy sugerowały, że guzy BrMS1 mogą lepiej reagować na radioterapię, a zapalne, bogate w punkty kontrolne środowisko BrMS2 mogłoby zwiększać korzyść z immunoterapii przywracającej aktywność „wygaszonym” limfocytom T — chociaż wymaga to potwierdzenia bezpośrednio u pacjentów z przerzutami do mózgu.
Co to oznacza dla osób z przerzutami do mózgu
Ten atlas pokazuje, że po dotarciu do mózgu komórki nowotworowe mają tendencję do konwergencji w kilka wspólnych stanów biologicznych, niezależnie od miejsca pierwotnego. Zrozumienie, czy przerzut u danego pacjenta jest neuronalny, bogaty w odporność, metaboliczny czy wysoce proliferacyjny, mogłoby w przyszłości ukierunkować bardziej dopasowane leczenie — na przykład wybór między radioterapią, immunoterapią czy lekami celującymi w metabolizm lub podział komórek. Choć te odkrycia nie zmieniają jeszcze standardów opieki, dostarczają szczegółowej mapy drogowej dla przyszłych badań i badań klinicznych mających na celu przekształcenie tych molekularnych słabości w lepsze, bardziej precyzyjne terapie dla pacjentów z przerzutami do mózgu.
Cytowanie: Yang, Z., Wei, S., Duan, H. et al. A proteogenomic atlas of 1032 brain metastases identifies molecular subtypes, immune landscapes, and therapeutic vulnerabilities. Nat Commun 17, 2038 (2026). https://doi.org/10.1038/s41467-026-68748-y
Słowa kluczowe: przerzut do mózgu, podtypy nowotworów, mikrośrodowisko guza, immunoterapia nowotworowa, metabolizm nowotworowy