Clear Sky Science · pl
Skład fosfolipidów silnie wpływa na składanie białek w formie β‑baryłek w oczyszczonych zewnętrznych błonach bakteryjnych
Dlaczego powłoki bakteryjne mają znaczenie
Odporne na leki „superbakterie” stanowią narastające zagrożenie, ponieważ wiele antybiotyków po prostu nie przenika przez ich twarde zewnętrzne osłony. W tym badaniu przyglądamy się uważnie jednemu kluczowemu elementowi tej obrony u bakterii Gram‑ujemnych, takich jak E. coli: ochronnej zewnętrznej powłoce wypełnionej białkami o kształcie baryłek i wyspecjalizowanymi tłuszczami. Rozkładając na czynniki, w jaki sposób mieszanka tych tłuszczów kontroluje budowę powłoki zewnętrznej, autorzy ujawniają słabe punkty, które można wykorzystać przy projektowaniu przyszłych antybiotyków.
Podwójna osłona
Bakterie Gram‑ujemne są nietypowe, ponieważ mają dwie błony. Błona wewnętrzna odpowiada za codzienne funkcje komórki, podczas gdy błona zewnętrzna działa jak wytrzymały płaszcz przeciwdeszczowy, który chroni przed wieloma toksynami i antybiotykami. Ta zewnętrzna warstwa składa się z dwóch typów lipidów: powszechnych fosfolipidów po stronie wewnętrznej oraz sztywnego cukrowo‑tłuszczowego związku zwanego lipopolisacharydem (LPS) po stronie zewnętrznej. Przewiercone przez tę powłokę są liczne białka „β‑baryłkowe” — puste cylindry tworzące pory i bramki dla składników odżywczych. Maszyna molekularna zwana BAM (od barrel assembly machine) odpowiada za fałdowanie tych białek i osadzanie ich w błonie zewnętrznej.
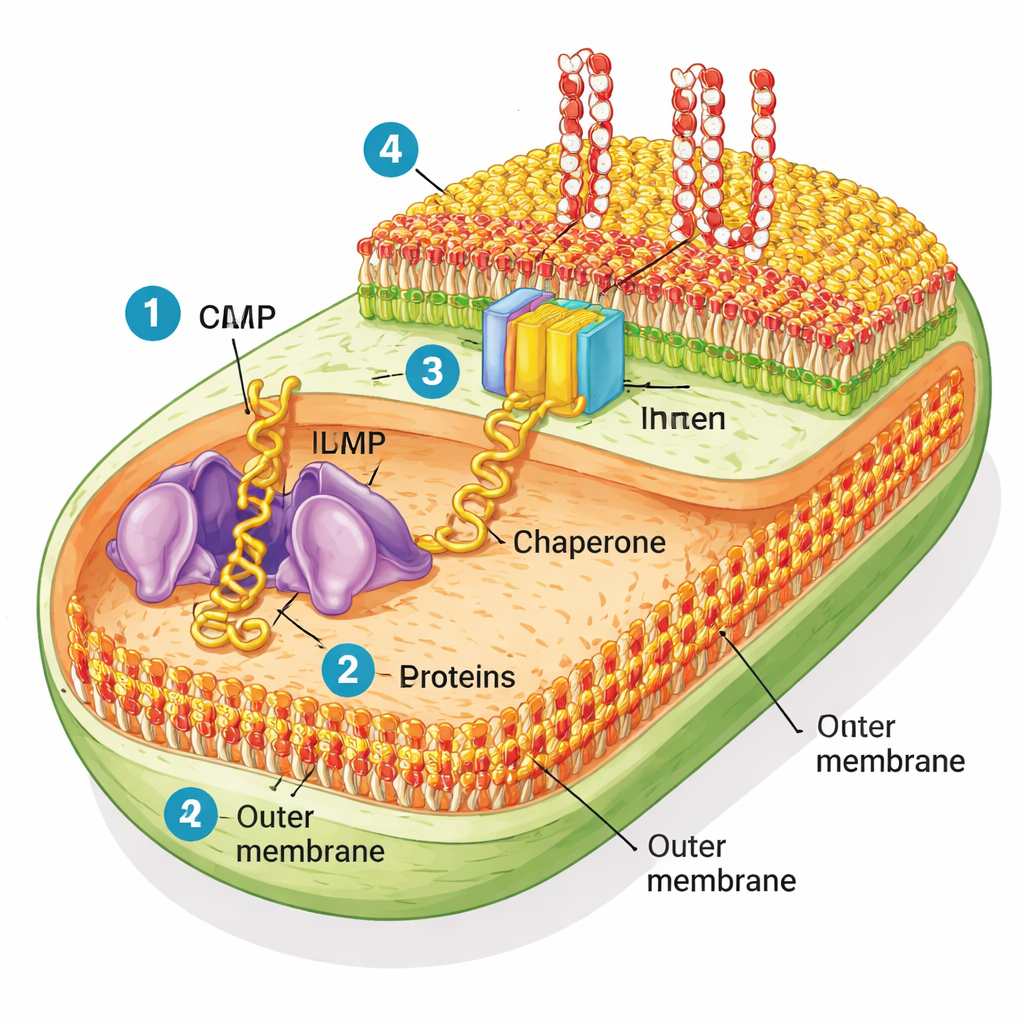
Odtworzenie powłoki bakteryjnej w probówce
Aby sprawdzić, jak dobrze BAM działa w realistycznych warunkach, badacze oczyszczali fragmenty błony zewnętrznej E. coli, tworząc maleńkie pęcherzyki, które nazywają „rodzimymi OM”. W odróżnieniu od prostych sztucznych błon używanych w wielu badaniach laboratoryjnych, te rodzimie błony zachowują pełny zestaw białek i lipidów. Zespół użył następnie systemu komórkowego pozbawionego komórek do syntezy nowych białek błony zewnętrznej od podstaw i obserwował, czy BAM w tych rodzimych pęcherzykach potrafi je fałdować i osadzać. Skoncentrowali się na modelowym białku β‑baryłkowym o nazwie EspP oraz kilku innych. Gdy obecne było białko pomocnicze SurA, BAM w rodzimych błonach skutecznie fałdował EspP, a proces ten został zablokowany przez znany antybiotyk celujący w BAM — darobactynę, co jest jasnym dowodem, że naturalna maszyna pozostała aktywna.
Gdy mieszanka tłuszczów szwankuje
Następnie autorzy zapytali, co się dzieje, gdy równowaga lipidowa błony zewnętrznej zostanie zaburzona. Badali mutanty E. coli pozbawione kluczowych systemów, które normalnie korygują nieprawidłowo umieszczone fosfolipidy w zewnętrznej warstwie. Jeden system, MlaA, odprowadza zabłąkane fosfolipidy z powrotem do błony wewnętrznej; inny, enzym PldA, rozcina je. Używając rodzimych błon z tych mutantów, zespół stwierdził, że napędzana przez BAM składanie EspP znacznie spadało w szczepach pozbawionych MlaA i była poważnie upośledzona przy braku PldA. Efekty te nie wynikały z utraty samego BAM ani innych głównych białek, które nadal występowały na normalnych poziomach, co wskazuje raczej na zmienione środowisko lipidowe jako sprawcę.
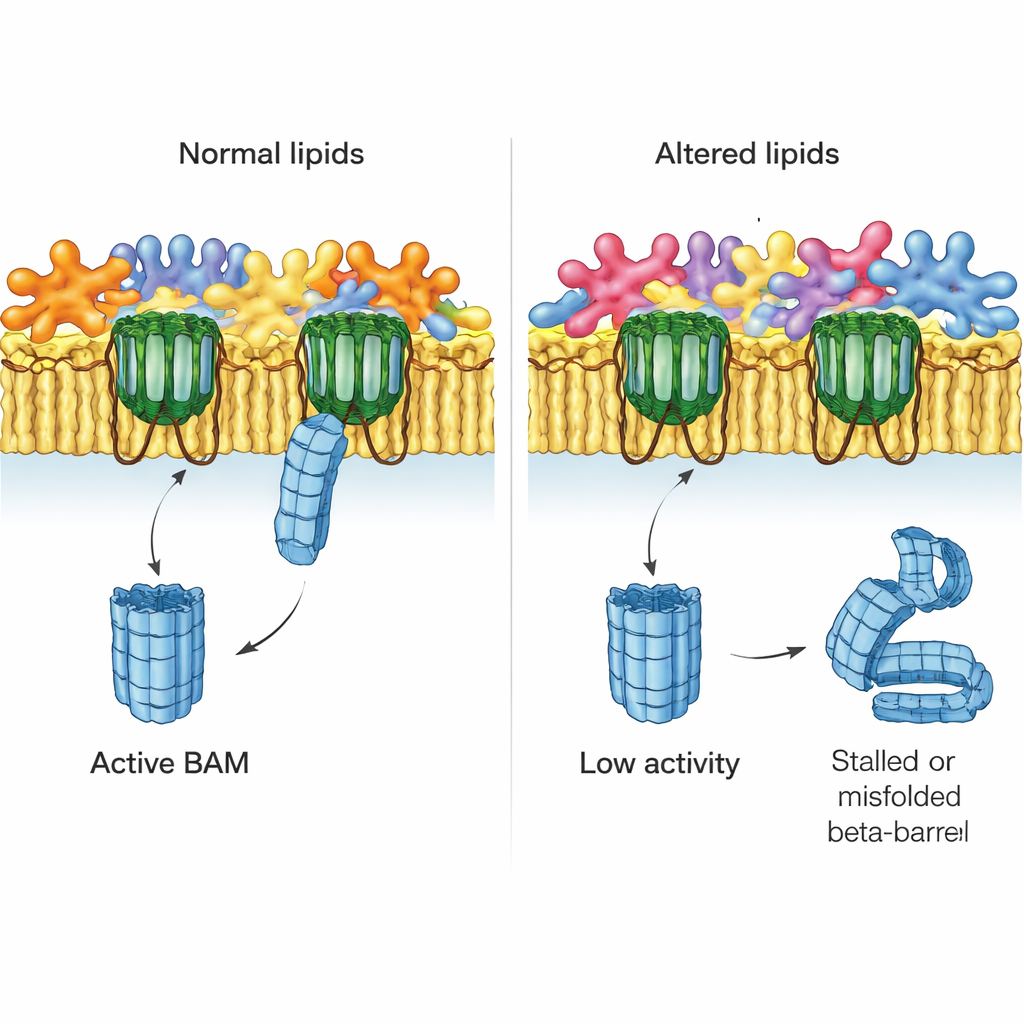
Szczegółowe mapowanie krajobrazu lipidowego
Aby powiązać funkcję z chemią, badacze opracowali czułą metodę spektrometrii mas do katalogowania setek pojedynczych fosfolipidów w całych komórkach i w oczyszczonych błonach zewnętrznych. W normalnej E. coli potwierdzili, że jeden typ lipidu (fosfatydyloetanoloamina, PE) jest wzbogacony w błonie zewnętrznej, podczas gdy inne (fosfatydylogliceryna i kardiolipina) są tam stosunkowo odtłuszczone. Odkryli także, że „lizo‑lipidy”, które mają tylko jeden łańcuch tłuszczowy i mają tendencję do wyginania błon, są zaskakująco skoncentrowane w błonie zewnętrznej. W szczepach mutantów, zwłaszcza tych pozbawionych PldA, te wzory zostały pomieszane: zwykłe różnice między błoną wewnętrzną a zewnętrzną zmalały lub nawet się odwróciły, a długości i typy łańcuchów tłuszczowych uległy przesunięciu. Szczepy z najbardziej zaburzonym profilem lipidowym były tymi, w których BAM działał najgorzej.
Implikacje dla strategii antybiotykowych
W sumie praca pokazuje, że błona zewnętrzna nie jest jedynie biernym szkieletem dla białek. Jej precyzyjny skład fosfolipidowy silnie wpływa na to, jak dobrze BAM potrafi budować pory β‑baryłkowe, które utrzymują bakterię przy życiu. Gdy równowaga lipidowa zostaje zaburzona, mniejsza liczba kompleksów BAM funkcjonuje prawidłowo, a niektóre działają wolniej. Choć żywe bakterie potrafią rekompensować takie zmiany w sposób, którego układ w probówce nie odtworzy, badanie to podkreśla, że regulacja lub zakłócenie specyficznych lipidów może osłabić bakteryjną powłokę. Ta wiedza otwiera nowe możliwości dla leków, które albo bezpośrednio celują w BAM, albo subtelnie zaburzają lipidy błony zewnętrznej, czyniąc nawet najsilniejsze bakterie Gram‑ujemne bardziej podatnymi.
Cytowanie: Nilaweera, T.D., Brandes, N.T., LaCroix, I.S. et al. Phospholipid composition strongly affects the assembly of β barrel proteins into purified bacterial outer membranes. Nat Commun 17, 1915 (2026). https://doi.org/10.1038/s41467-026-68743-3
Słowa kluczowe: Bakterie Gram‑ujemne, białka błony zewnętrznej, składanie β‑baryłek, lipidy bakteryjne, oporność na antybiotyki