Clear Sky Science · pl
Kynurenina pośredniczy w toksyczności jelit wywołanej chemioterapią poprzez modulację mikrobioty jelitowej
Dlaczego to ma znaczenie dla osób poddawanych chemioterapii
Chemioterapia ratuje życie, ale często wiąże się z wyniszczającymi dolegliwościami jelitowymi — bólem, biegunką, utratą wagi — które mogą zmusić lekarzy do zmniejszenia dawek lub przerwania leczenia. Badanie odkrywa ukryty łańcuch zdarzeń między krążącym we krwi związkiem chemicznym, komórkami układu odpornościowego i mikrobiotą jelitową, co pomaga wyjaśnić, dlaczego powszechny lek przeciwnowotworowy, oksaliplatyna, może tak mocno uszkadzać jelita, i wskazuje nowe sposoby ochrony pacjentów bez osłabienia terapii przeciwnowotworowej.
Chemiczna więź między leczeniem a uszkodzeniem jelit
Naukowcy zaczęli od pacjentów z rakiem jelita grubego leczonych chemioterapią opartą na oksaliplatynie. Porównali próbki krwi osób, które rozwinęły ciężkie objawy jelitowe, z tymi, które lepiej tolerowały leczenie. Przy użyciu ukierunkowanego profilowania chemicznego stwierdzili, że kilka produktów rozpadu aminokwasu tryptofanu było wyższych w grupie o dużej toksyczności, a jeden związek — L‑kynurenina — wyróżniał się jako najsilniej podwyższony. Pacjenci z większą ilością L‑kynureniny we krwi mieli też więcej objawów stanu zapalnego i niższe liczby białych krwinek, co sugeruje, że ta cząsteczka może być bezpośrednio związana ze szkodami wywołanymi leczeniem.
Ustalenie przyczynowości na modelach mysich
Aby wyjść poza korelacje, zespół sięgnął po modele mysie. Gdy zdrowe myszy otrzymywały wysokie dawki oksaliplatyny, rozwijały klasyczne objawy uszkodzenia jelit: utratę wagi, skrócenie okrężnicy, obrzęk ściany jelita, mniejszą liczbę dzielących się komórek i więcej komórek umierających w wyściółce jelitowej. U tych myszy stwierdzono też gwałtowny wzrost L‑kynureniny we krwi, co odzwierciedla dane ludzkie. Gdy badacze podawali dodatkową L‑kynureninę myszy leczonym oksaliplatyną, uszkodzenia jelit nasilały się — jednocześnie zdolność leku do niszczenia guzów pozostawała nienaruszona. Natomiast usunięcie lub zablokowanie enzymu IDO1, który organizm wykorzystuje do przekształcania tryptofanu w L‑kynureninę, sprawiło, że myszy były znacznie bardziej odporne na toksyczność jelitową, a jednocześnie dalej korzystały z efektu chemioterapii.
Komórki odpornościowe i mikroby jelitowe w ogniu krzyżowym
Idąc dalej, naukowcy badali, które komórki odpowiadają za nadmierną produkcję L‑kynureniny podczas leczenia. Odkryli, że oksaliplatyna pobudza pewne komórki odpornościowe (limfocyty CD8) do uwalniania białka sygnalizacyjnego interferonu‑gamma, co następnie włącza IDO1 w pobliskich komórkach mieloidalnych — klasie białych krwinek. Myszy zaprojektowane tak, by brak IDO1 dotyczył tylko ich komórek mieloidalnych, wytwarzały znacznie mniej L‑kynureniny i były chronione przed uszkodzeniem jelit, podczas gdy usunięcie IDO1 wyłącznie w komórkach wyściółki jelitowej miało mały efekt. Równocześnie zmienił się skład mikrobioty jelitowej. U normalnych myszy oksaliplatyna i wysokie poziomy L‑kynureniny wiązały się z utratą pożytecznej bakterii Lactobacillus johnsonii. Natomiast u myszy z obniżonym poziomem L‑kynureniny utrzymywały się wyższe poziomy L. johnsonii. Kiedy mikroby jelitowe zostały zniszczone antybiotykami, ochronny efekt niskiej L‑kynureniny zniknął, a przeszczepienie bakterii od myszy o niskim poziomie L‑kynureniny do myszy normalnych sprawiło, że biorcy stali się bardziej odporni na uszkodzenia jelit spowodowane oksaliplatyną.
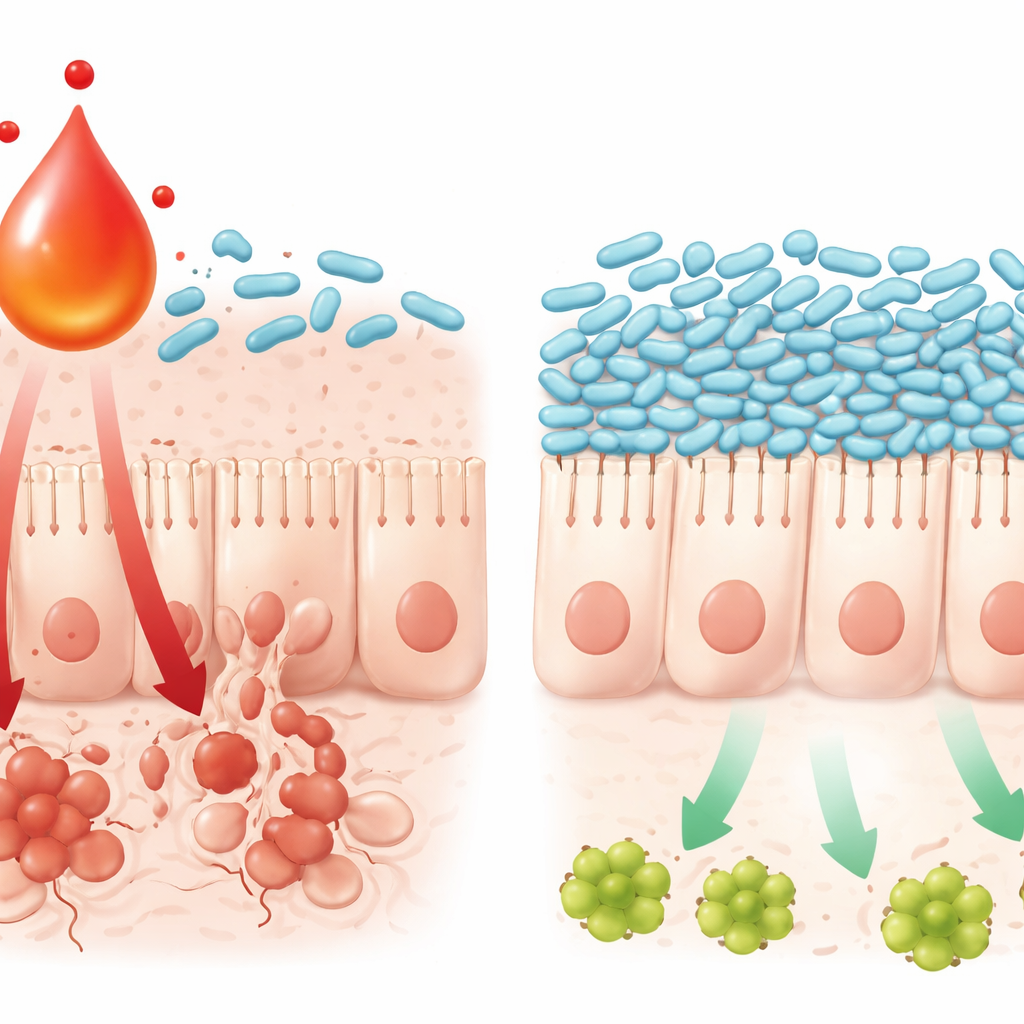
Jak jeden metabolit napędza śmierć komórek w jelicie
Badanie śledziło także, jak ta interakcja chemii i mikrobioty uszkadza wyściółkę jelitową. Wysokie poziomy L‑kynureniny wiązały się ze zwiększoną aktywnością znanej ścieżki zapalnej w tkance jelitowej, szlaku TNFα/JNK, który kieruje komórki ku zaprogramowanej śmierci. W hodowlach komórkowych połączenie oksaliplatyny z L‑kynureniną sprawiało, że komórki jelitowe częściej aktywowały tę ścieżkę i umierały, podczas gdy dodanie bakterii L. johnsonii osłabiało sygnał i chroniło przeżycie komórek. Sama L‑kynurenina mogła hamować wzrost i osłabiać mechanizmy przetrwania L. johnsonii w warunkach laboratoryjnych, co pomaga wyjaśnić, dlaczego bakteria zanika, gdy metabolit się kumuluje. Razem te odkrycia opisują samowzmacniający się cykl: chemioterapia wywołuje sygnalizację odpornościową, komórki odpornościowe zwiększają produkcję L‑kynureniny, to zaburza przyjazne bakterie jak L. johnsonii, a zmieniona społeczność mikrobiologiczna z kolei wzmacnia sygnały zapalne prowadzące do śmierci komórek jelit.
Nowe sposoby ochrony pacjentów podczas leczenia
Co zachęcające, praca wskazuje też praktyczne strategie. Leczenie myszy lekiem Epacadostat, który hamuje IDO1, obniżało poziomy L‑kynureniny i wyraźnie zmniejszało uszkodzenia jelit wywołane oksaliplatyną, nie osłabiając kontroli nad guzami. W podejściu uzupełniającym zespół zmodyfikował niechorobotwórczy szczep E. coli tak, aby nadprodukowal enzym rozkładający L‑kynureninę w jelicie. Myszy otrzymujące te inżynierowane bakterie były podobnie chronione przed toksycznością jelitową, znów bez kompromisów dla efektu przeciwnowotworowego chemioterapii. Suplementacja samą L. johnsonii również łagodziła objawy i zachowywała strukturę jelita.
Co to oznacza dla osób z rakiem
Podsumowując, badanie ujawnia, że pojedynczy metabolit wywołany leczeniem — L‑kynurenina — działa jako kluczowy pośrednik między chemioterapią, układem odpornościowym, mikrobiotą jelitową i uszkodzeniem jelit. Pokazując, że zablokowanie jej produkcji, zwiększenie jej rozkładu lub przywrócenie ochronnych bakterii może osłabić szkodliwy wpływ chemioterapii na jelita, badania otwierają drogę do terapii wspomagających, które pomogą pacjentom zachować siły i komfort w trakcie walki z rakiem.
Cytowanie: Xie, H., Yang, J., Wu, J. et al. Kynurenine mediates the chemotherapy-induced intestinal toxicity through modulation of gut microbiota. Nat Commun 17, 2087 (2026). https://doi.org/10.1038/s41467-026-68741-5
Słowa kluczowe: skutki uboczne chemioterapii, mikrobiom jelitowy, metabolizm tryptofanu, L-kynurenina, rak jelita grubego