Clear Sky Science · pl
Zarządzanie przepływem elektrolitu zwiększa wydajność ciągłej elektrosyntezy oksymów powyżej 95%
Uczynienie prekursorów tworzyw zielonymi
Nylon‑6 przenika nasze życie codzienne — od ubrań i dywanów po części samochodowe. Jeden z jego kluczowych składników, oksym cykloheksanonu, zwykle wytwarzany jest drogami opartymi na paliwach kopalnych i generującymi niebezpieczne produkty uboczne. W badaniu tym zbadano, jak zastąpić te metody procesem napędzanym prądem, który może pracować w trybie ciągłym, generować mniej odpadów i osiągać bardzo wysoką wydajność, wskazując drogę do czystszej produkcji codziennych tworzyw.
Dlaczego dzisiejsze składniki nylonu są problemem
Aby otrzymać nylon‑6, przemysł najpierw produkuje oksym cykloheksanonu, który następnie przekształca się w kaprolaktan — bezpośredni prekursor nylonu. Konwencjonalne zakłady pozyskują kluczowy odczynnik pośredni, hydroksyloaminę, redukując tlenki azotu za pomocą dwutlenku siarki i wodoru. Podejście to wiąże się z dużym śladem węglowym, niską efektywnością wykorzystania atomów oraz poważnymi problemami bezpieczeństwa i zanieczyszczenia. Alternatywna chemia oparta na nadtlenku wodoru unika niektórych zagrożeń, ale polega na drogim i niestabilnym utleniaczu. Przy prognozowanej globalnej zdolności produkcyjnej nylonu‑6 na poziomie milionów ton rocznie, znalezienie bezpieczniejszej, niskoemisyjnej drogi do oksymu cykloheksanonu jest pilnym wyzwaniem.
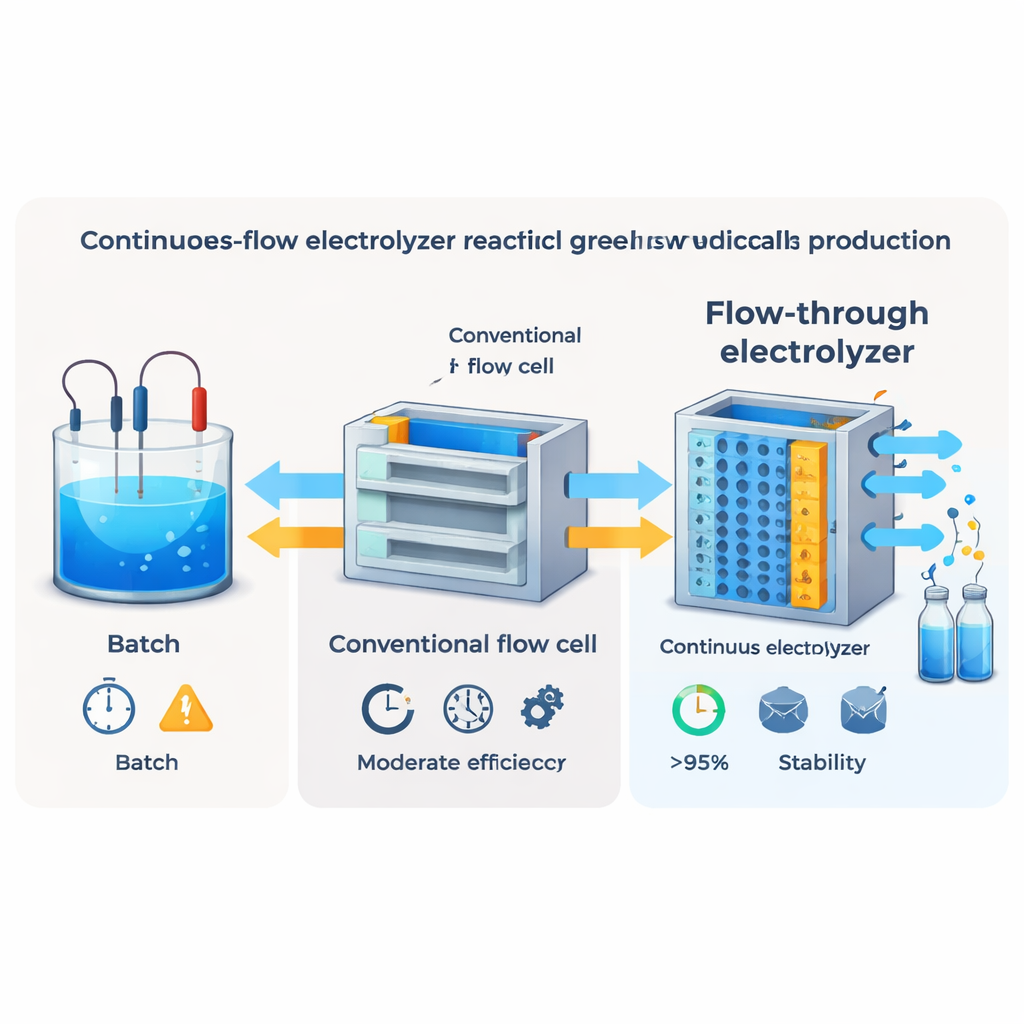
Wykorzystanie elektryczności do napędzania czystszej chemii
Autorzy wykorzystują rosnącą dostępność odnawialnej energii elektrycznej, by przeprojektować sposób wytwarzania oksymu cykloheksanonu. Zamiast dostarczać hydroksyloaminę z zewnątrz, generują ją bezpośrednio z jonów azotynowych w wodzie na elektrodzie, gdzie elektrony zasilane z źródła prądu redukują azotyny etapami do hydroksyloaminy. Świeżo powstała hydroksyloamina reaguje następnie z cykloheksanonem, dając pożądany oksym. Wcześniejsze demonstracje laboratoryjne wykazały, że ta ścieżka działa, ale opierały się na małych ogniwach partiowych o ograniczonej skalowalności i pozostawiały rozbieżność między szybkością powstawania hydroksyloaminy a szybkością jej reakcji, co prowadziło do przeciętnej wydajności w urządzeniach ciągłego przepływu.
Katalizatory jednoatomowe jako narzędzia precyzyjne
Aby poprawić wydajność, zespół najpierw poszukiwał wysoce selektywnego katalizatora. Stworzyli rodzinę materiałów „jednoatomowych”, w których pojedyncze atomy metali (kobalt, żelazo lub mangan) są zakotwiczone na azotem-dopowanym podłożu węglowym. Szczegółowe badania rentgenowskie i mikroskopowe potwierdziły, że metale są rozproszone atomowo, a nie zlepione w cząstki. W testach w standardowym ogniwie elektrochemicznym wyróżniała się wersja kobaltowa: wytwarzała oksym cykloheksanonu z efektywnością faradyczną powyżej 80 procent i niemal doskonałą selektywnością węglową, co oznacza, że praktycznie każdy atom węgla z cykloheksanonu trafiał do produktu docelowego. Zaawansowana spektroskopia i symulacje komputerowe wyjaśniły przyczynę: kobalt wiąże kluczowe pośrednie związki zawierające azot wystarczająco silnie, by skierować reakcję ku hydroksyloaminie, ale nie tak mocno, by nadmiernie je zredukować do amoniaku lub marnować elektrony na wytwarzanie wodoru gazowego.
Przemyślenie sposobu przepływu cieczy
Nawet doskonały katalizator nie zrekompensuje słabego dopływu reagentów. W konwencjonalnych ogniwach przepływowych z membraną ciecz przemyka obok, zamiast przepływać przez porowatą elektrodę, więc cząsteczki muszą powoli dyfundować do miejsc aktywnych. Badacze użyli symulacji dynamiki płynów i eksperymentów, by przeprojektować ogniwo tak, aby elektrolit był wymuszony do przepływu przez samą elektrodę. Ta architektura „flow‑through” znacznie skraca odległości dyfuzji i tworzy silny przepływ konwekcyjny przez katalizator. W porównaniu ze standardowymi układami „flow‑by” nowy projekt zwiększył prędkość cieczy wewnątrz elektrody o rzędy wielkości i podniósł efektywność faradyczną dla oksymu cykloheksanonu powyżej 95 procent, nawet przy prądach istotnych z przemysłowego punktu widzenia.
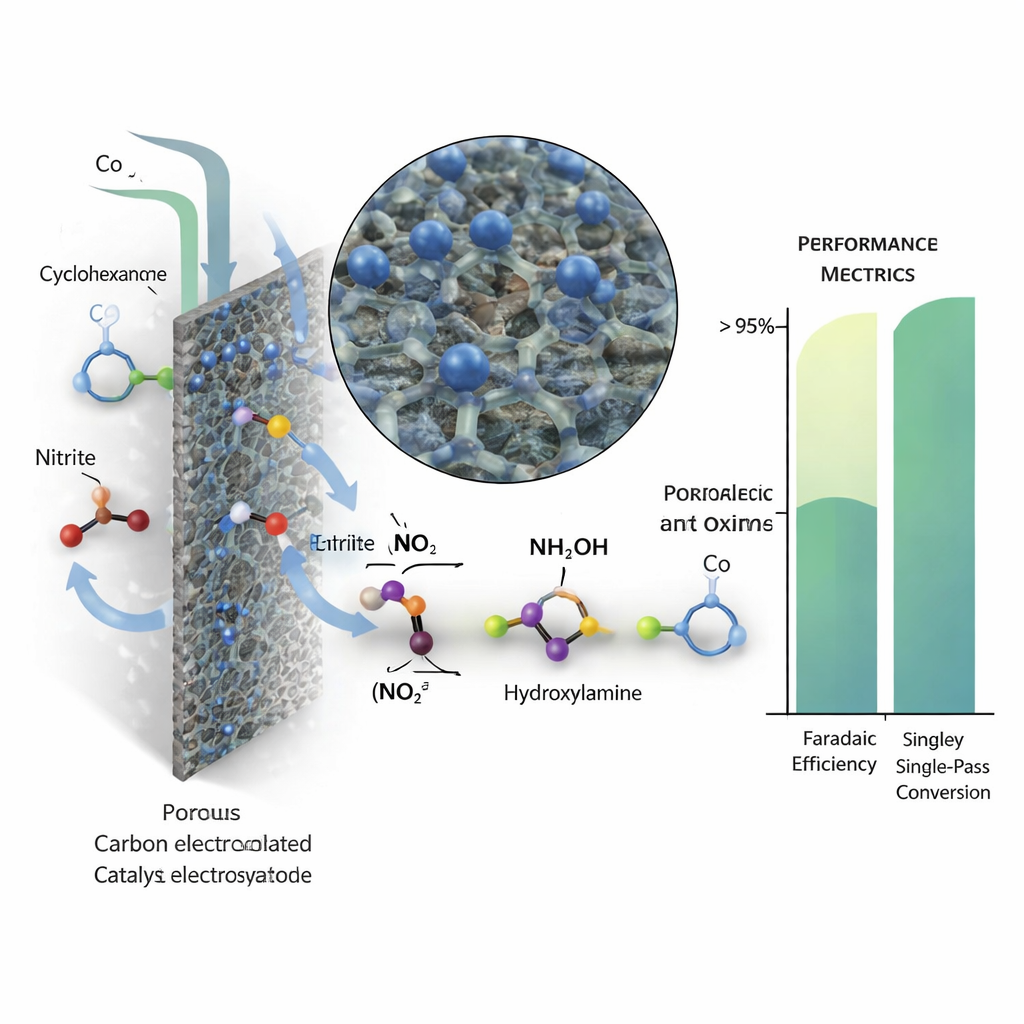
Wykorzystanie każdego przebiegu
Aby proces ciągły był praktyczny, jedno przejście cieczy przez ogniwo musi przekształcić większość cykloheksanonu, unikając skomplikowanych pętli recyrkulacji. Zespół pokazał, że poprzez staranne dostrojenie prędkości przepływu i stężenia azotynu można zrównoważyć szybkość powstawania hydroksyloaminy z dostawą cykloheksanonu. W zoptymalizowanych warunkach jednoprzebiegowa konwersja przekroczyła 95 procent przy jednoczesnym utrzymaniu wysokiej efektywności faradycznej. System pracował stabilnie przez 110 godzin, produkując ponad 16 gramów surowego oksymu o wysokiej czystości, a katalizator kobaltowy zachował swoją atomową strukturę. Analiza techno‑ekonomiczna sugeruje, że przy dalszych poprawach wydajności i skali oraz przy dostępie do taniej odnawialnej energii elektrycznej proces mógłby wytwarzać oksym cykloheksanonu po koszcie zgodnym z produkcją nylonu na dużą skalę.
Co to znaczy dla codziennych materiałów
Dla czytelników niebędących specjalistami przekaz jest prosty: poprzez staranne zarządzanie przepływem cieczy w reaktorze elektrochemicznym oraz zastosowanie precyzyjnie dostrojonego katalizatora jednoatomowego autorzy przekształcają zanieczyszczający, oparty na paliwach kopalnych etap produkcji nylonu w wydajny proces napędzany elektrycznością. Ich konstrukcja przepływowa wyciska więcej produktu z każdego elektronu i każdej kropli cieczy, a analiza pokazuje realistyczną drogę do opłacalności. Poza tym konkretnym związkiem ta sama strategia — łączenie inteligentnych katalizatorów z przemyślanymi architekturami przepływu — może pomóc w elektryfikacji i oczyszczeniu wielu innych procesów chemicznych na dużą skalę, które leżą u podstaw współczesnego życia.
Cytowanie: Li, J., Wang, X., Yang, X. et al. Managing electrolyte flow boosts the efficiency of continuous oxime electrosynthesis to over 95%. Nat Commun 17, 1970 (2026). https://doi.org/10.1038/s41467-026-68738-0
Słowa kluczowe: elektrosynteza, przepływowy elektrolizer, katalizator jednoatomowy, prekursor nylonu, zielona chemia