Clear Sky Science · pl
Kataliza niklowa prowadząca do dywergentnych sulfonacji węglanu propargylowego
Dlaczego ta chemia ma znaczenie poza laboratorium
Związki zawierające siarkę są centralnym elementem wielu współczesnych leków, środków ochrony roślin i zaawansowanych materiałów. Jednak wytwarzanie tych związków w sposób precyzyjny, wydajny i elastyczny bywa trudne. Artykuł opisuje metodę katalizowaną niklem, która potrafi zamienić proste substraty w kilka różnych rodzin cząsteczek bogatych w siarkę, wszystkie z ściśle kontrolowaną strukturą 3D. Taka kontrola może przyspieszyć odkrywanie leków i pomóc chemikom w konstruowaniu złożonych cząsteczek w sposób czystszy i bardziej zrównoważony.
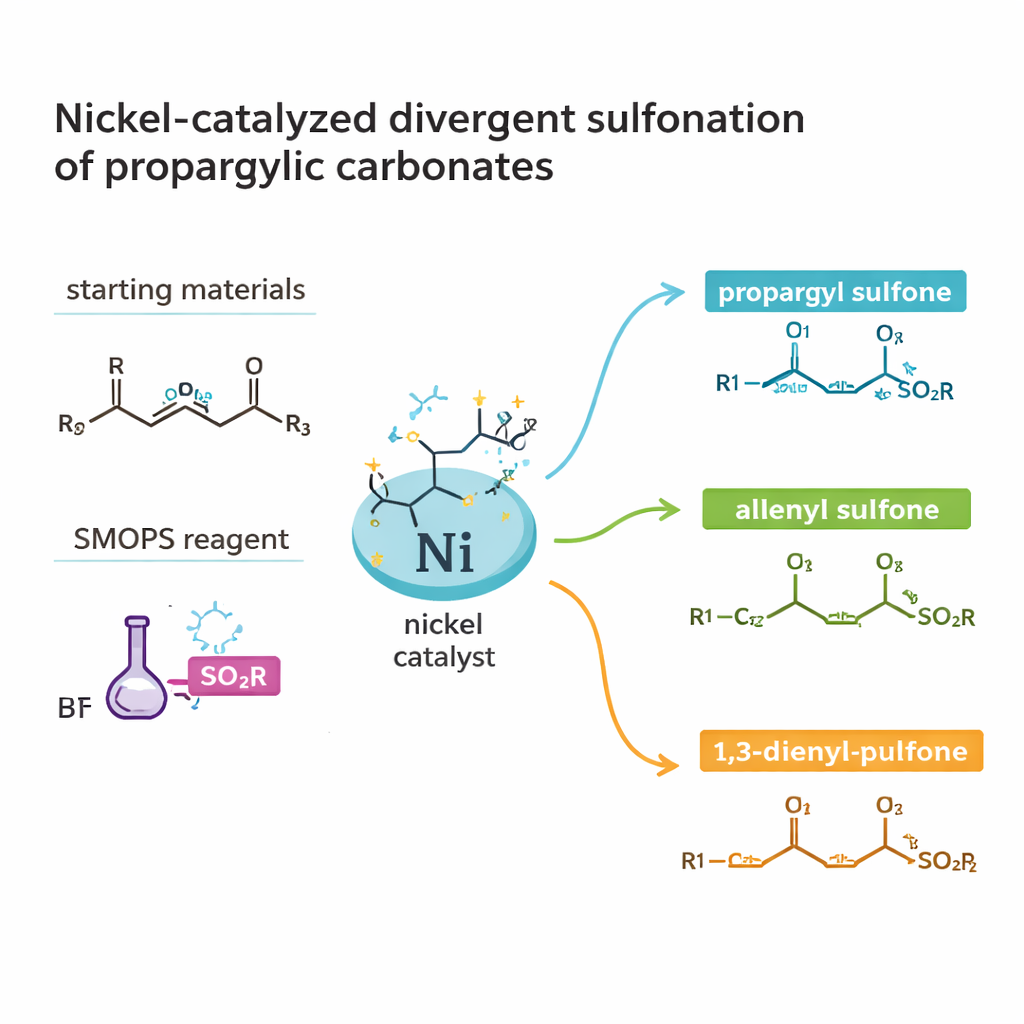
Budowanie użytecznych cząsteczek z prostych elementów
Praca koncentruje się na klasie związków zwanych sulfonami i sulfinianami, które zawierają siarkę związaną z tlenem i węglem. Struktury te występują w wielu bioaktywnych produktach naturalnych i farmaceutykach, ale tradycyjne drogi prowadzące do nich bywają długie i marnotrawne. Autorzy skupiają się na szczególnie wartościowym podtypie: chiralnych sulfinianach, których enancjomery mogą zachowywać się w organizmie zupełnie inaczej. Zamiast zaczynać od już złożonych bloków budulcowych, używają dwóch łatwo dostępnych partnerów: węglanów propargylowych (rodzaj krótkiego łańcucha węglowego z wbudowaną grupą opuszczającą) oraz komercyjnego źródła siarki znanego jako SMOPS. Łącząc je w obecności katalizy niklowej, dążą do uzyskania wysoko wartościowych produktów zawierających siarkę w zaledwie jednym lub dwóch krokach.
Jeden system katalityczny, trzy rodziny produktów
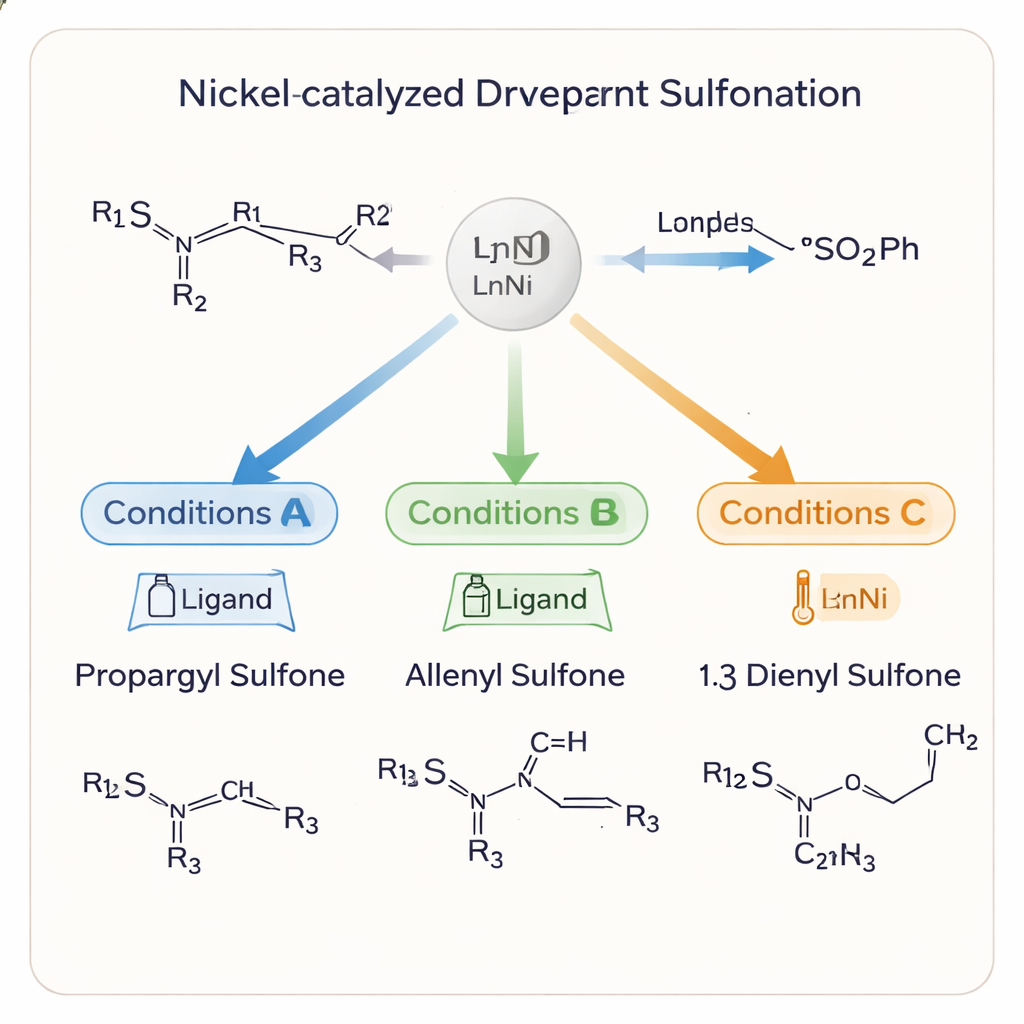
Uderzającą cechą badania jest to, że te same podstawowe składniki można skierować do tworzenia trzech odmiennych typów produktów: propargylowych sulfonów, allenowych sulfonów oraz 1,3-dienylowych sulfonów. Każde z tych szkieletów węglowych prowadzi do innej chemii i aktywności biologicznej dalej w syntezie. Poprzez staranny dobór liganda wiążącego nikiel, rozpuszczalnika, temperatury i dodatków, zespół potrafi „sterować” reakcją w stronę jednego z wyników. W łagodnych warunkach w acetonitrylu i z chiralnym ligandom fosfinowym otrzymują propargylowe sulfony w wysokim plonie i z doskonałą kontrolą nad konfiguracją. Obróbka tych produktów tlenkiem glinu delikatnie przekształca potrójne wiązanie w allen, ponownie bez utraty informacji chiralnej. Zmiana liganda i rozpuszczalnika zamiast tego kieruje proces do 1,3-dienylowych sulfonów, wydłużając szkielet węglowy.
Badanie zakresu i elastyczności
Aby sprawdzić, jak ogólne jest to podejście, badacze zmieniali obu partnerów reakcji. Pokazali, że wiele różnych sulfinianów sodu, w tym proste alkilowe, arylowe i bardziej złożone systemy pierścieniowe, reaguje czysto i daje chiralne produkty z wysoką nadmiarowością enancjomerów. Podobnie szeroki zestaw węglanów propargylowych z różnymi podstawnikami na pierścieniu aromatycznym lub łańcuchu węglowym działa dobrze, chociaż niektóre substraty z bardzo dużymi grupami lub końcowymi alkinami wykraczają poza obecny zakres metody. Zespół pokazuje również, że ilości można zwiększać bez utraty wydajności czy selektywności, co jest kluczowym krokiem w stronę praktycznego zastosowania. Ten szeroki zakres pozwala chemikom podłączać wiele różnych fragmentów i szybko uzyskiwać bibliotekę pokrewnych związków zawierających siarkę.
Przekształcanie bloków budulcowych w złożone cele
Ponad samo wytwarzanie tych sulfonów, autorzy pokazują, jak łatwo można je przekształcać w inne użyteczne struktury. Hydrogenacja konwertuje potrójne wiązanie w alkany lub alkeny przy zachowaniu centrum chiralnego przy siarce. Proste reakcje następcze przekształcają jednostki sulfonowe w sulfiniany, sulfonamidy i sulfonylowe fluorki — motywy powszechnie występujące w chemii medycznej i w reakcjach przypominających „click”. Jako demonstrację, używają swojej metody jako kluczowego kroku w zwartej syntezie chiralnego β-sulfinylohydroksamowego kwasu, typu cząsteczki znanej z hamowania enzymów bakteryjnych. Ta droga omija kilka starszych, bardziej uciążliwych etapów i podkreśla siłę syntetyczną posiadania chiralnych sulfinianów „na żądanie”.
Jak reakcja wybiera ścieżkę
Zespół bada również, jak i dlaczego reakcja przełącza się między produktami. Eksperymenty śledzące przebieg w czasie pokazują, że propargylowy sulfon zwykle powstaje jako pierwszy, a następnie może ulec przekształceniu w allen i ostatecznie w 1,3-dien pod pewnymi warunkami. Katalizator niklowy, wraz z wybranym ligandem i dodatkiem, kontroluje, które pośrednie produkty są faworyzowane i jak grupa siarkowa przesuwa się wzdłuż łańcucha węglowego. Tlenek glinu, na przykład, pozwala na przebieg przekształcenia alkin→allen w bardzo niskiej temperaturze przy zachowaniu trójwymiarowego ułożenia atomów. Uproszczony mechanizm sugeruje, że subtelne zmiany warunków reakcji przekierowują wspólny pośredni kompleks niklowy różnymi ścieżkami, co wyjaśnia, jak jeden system może dawać wiele ściśle określonych produktów.
Co to oznacza dla przyszłych leków i materiałów
Dla nie‑specjalistów kluczowy wniosek jest taki, że ta metoda katalizowana niklem zapewnia wszechstronną „centralkę” chemiczną: z tych samych prostych wyjściowych elementów chemicy mogą wybrać, jaki szkielet bogaty w siarkę chcą otrzymać, i uzyskać go w jednym, wysoce selektywnym kroku. Ponieważ produkty te są doskonałymi blokami budulcowymi dla leków i innych funkcjonalnych cząsteczek, podejście może skrócić drogę od koncepcji do kandydata. Pokazuje też, jak staranny dobór katalizatora i warunków może przekształcić kiedyś trudną transformatę w rutynowe narzędzie, otwierając drzwi do szybszego, czystszego budowania złożonych, chiralnych związków zawierających siarkę.
Cytowanie: Gu, W., He, Z., Wang, H. et al. Nickel-catalyzed divergent sulfonations of propargylic carbonate. Nat Commun 17, 1882 (2026). https://doi.org/10.1038/s41467-026-68720-w
Słowa kluczowe: kataliza niklem, chiralne sulfony, synteza asymetryczna, projektowanie reakcji organicznych, fragmenty przypominające leki