Clear Sky Science · pl
Oparte na reakcji click oznaczanie gromadzenia się cząsteczek w Escherichia coli
Dlaczego małym lekom trudno dotrzeć do niebezpiecznych bakterii
Współczesna medycyna opiera się na antybiotykach, a mimo to niektóre z najgroźniejszych bakterii są obecnie chronione przez wytrzymałe zewnętrzne ściany, które skutecznie blokują wiele leków. Bakterie Gram‑ujemne, takie jak Escherichia coli, mają szczególnie efektywną barierę zewnętrzną, co utrudnia projektowanie leków, które rzeczywiście przedostaną się do wnętrza i dotrą do swoich celów. W pracy tej przedstawiono nowy test laboratoryjny, nazwany testem CHAMP, który umożliwia naukowcom szybkie zmierzenie, jak dobrze tysiące różnych małych cząsteczek omijają te mechanizmy obronne i gromadzą się we wnętrzu żywych komórek E. coli.
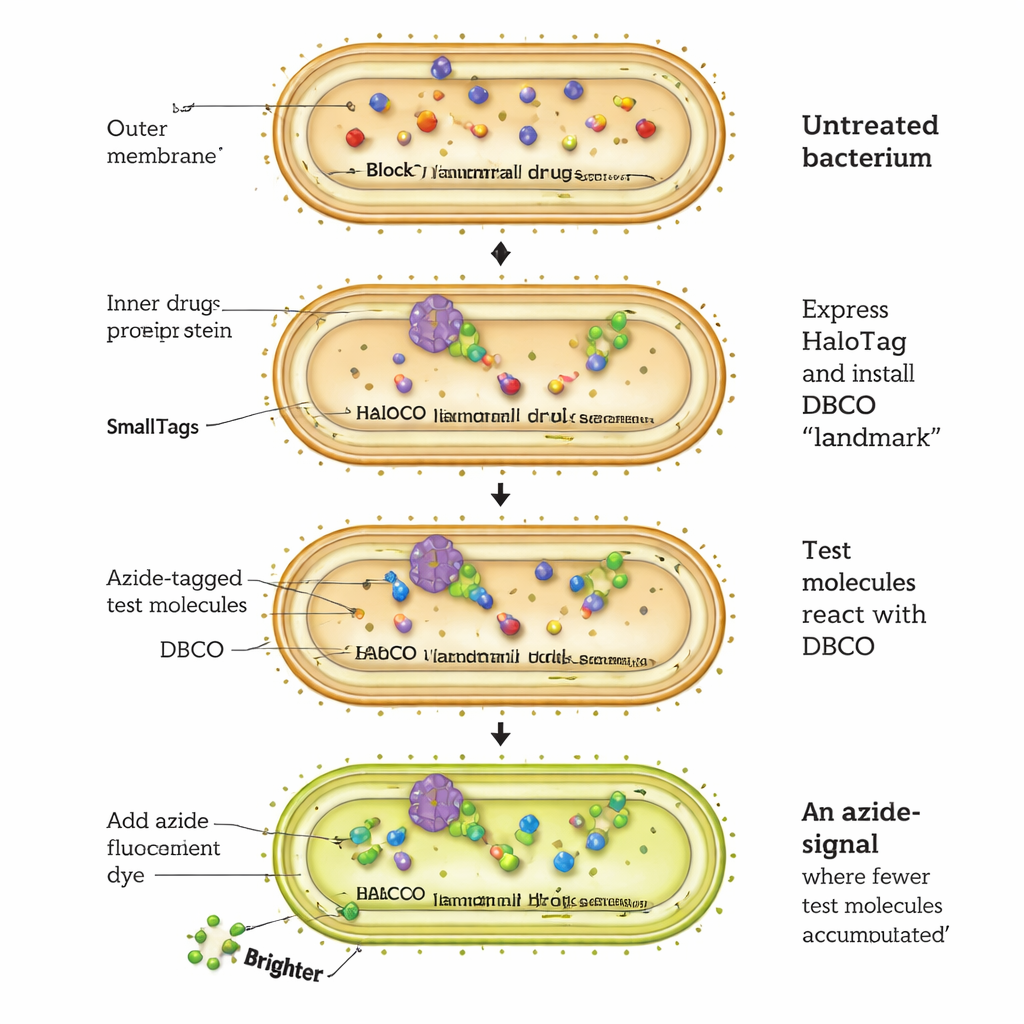
Nowy sposób obserwowania, jak leki wnikają do komórek bakteryjnych
Tradycyjne odkrywanie antybiotyków opierało się na związkach naturalnych i prostych testach wzrostu, które określały, czy bakterie przeżyły czy zginęły. Takie testy nie ujawniają jednak, jaka ilość leku faktycznie dostała się do komórki ani gdzie się on znalazł po wejściu. Autorzy postanowili opracować bezpośrednią, szeroko stosowalną metodę śledzenia wnikania leków do cytosolu bakterii — płynnego wnętrza, w którym znajduje się wiele miejsc docelowych antybiotyków. Ich celem było wyjście poza surowe odczyty, takie jak minimalne stężenie hamujące, które mieszają efekty wnikania leku, wiązania z celem i dalszych procesów biologicznych, oraz uzyskanie czystego pomiaru akumulacji wewnątrzkomórkowej.
Przekształcanie bakterii w małe rejestratory chemiczne
Test CHAMP działa poprzez przeprogramowanie białka bakteryjnego zwanego HaloTag, aby pełniło rolę molekularnego „miejsca docelowego”. Komórki E. coli są genetycznie zmodyfikowane tak, by produkować HaloTag w cytosolu. Badacze najpierw przyłączają specjalny uchwyt chemiczny — „spięty” alkin DBCO — do HaloTag przy pomocy krótkiego łańcucha chloroalkanu. Następnie eksponują bakterie na testowane cząsteczki, z których każda niesie bardzo małą grupę azydową. Tylko te cząsteczki, które przedrą się przez zewnętrzną i wewnętrzną błonę oraz dotrą do cytosolu, mogą zareagować z uchwytem DBCO w wysoce selektywnej reakcji „click”, trwale oznaczając HaloTag. Na koniec komórki traktuje się fluorescencyjnym barwnikiem z grupą azydową, który może przyłączyć się jedynie do pozostałych, nieobsadzonych DBCO. Im jaśniejsze fluorescencja, tym mniej testowanych cząsteczek dotarło do cytosolu; ciemniejsze komórki wskazują na lepszą akumulację.
Badanie, jak chemia i biologia kształtują wnikanie leków
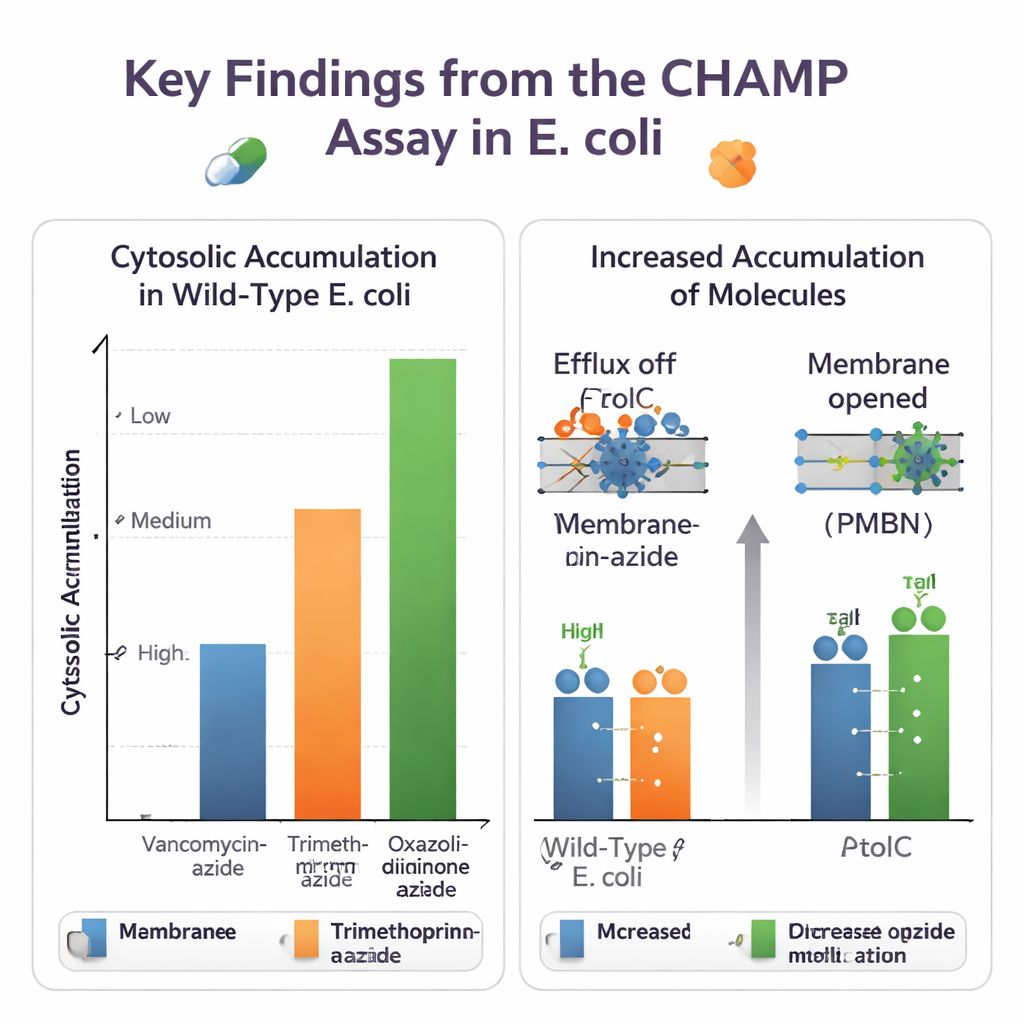
Wykorzystując CHAMP, zespół najpierw dopracował ekspresję HaloTag, ilość kotwicy DBCO oraz dobór barwników fluorescencyjnych, aby uzyskać duże i wiarygodne okno sygnału. Następnie użyli zestawów blisko spokrewnionych małych cząsteczek, aby zobaczyć, jak chemiczne modyfikacje wpływają na wnikanie. Przekształcenie kwasów karboksylowych w amidy oraz dodawanie lub usuwanie grup aminowych mogło zauważalnie zmienić poziomy w cytosolu. W wielu przypadkach aminy pierwotne zwiększały akumulację, co odzwierciedla niezależne „zasady eNTRy” opracowane przez inne grupy. Test poradził sobie także z wersjami rzeczywistych antybiotyków oznaczonymi azydem, ujawniając duże różnice: masywne leki, takie jak wankomycyna, ledwo docierały do cytosolu, podczas gdy mniejsze antybiotyki, takie jak pochodne trimetoprimu i niektóre oksazolidynony, wnikały znacznie łatwiej.
Demaskowanie obrony bakterii, która wypompowuje leki na zewnątrz
Ponieważ metoda działa na żywych, genetycznie programowalnych bakteriach, pozwala rozplątać role różnych mechanizmów obronnych. Autorzy porównali normalne E. coli ze szczepami pozbawionymi TolC — kluczowego elementu głównej wielolekowej pompy wypompowującej — oraz z komórkami traktowanymi małocząsteczkowym inhibitorem TolC. Dla novobiocyny i kilku innych antybiotyków oznaczonych azydem CHAMP wykazał wyraźnie wyższą akumulację w cytosolu po wyłączeniu TolC, potwierdzając, że te związki są substratami effluxu. Testowali także sposoby poluzowania bariery zewnętrznej błony, zarówno chemicznie za pomocą peptydu PMBN, jak i genetycznie przez nadekspresję szerokiego poru. Wiele cząsteczek, które wcześniej akumulowały się słabo, wykazało duże przyrosty po permeabilizacji błony, co podkreśla, jak wnikanie i efflux współdziałają, kształtując wewnętrzne poziomy leku.
Skalowanie do tysięcy cząsteczek w poszukiwaniu wzorców i reguł
Aby zademonstrować prawdziwą wysoką przepustowość, badacze przeskanowali komercyjny zestaw 404 związków z grupą azydową oraz niestandardową bibliotekę 1 152 molekuł niosących azyd. Mierzyli akumulację w kilku kontekstach bakteryjnych, w tym w komórkach nieleczonych, traktowanych PMBN, hiperporinowanych oraz hiperporinowanych pozbawionych TolC. Porównując tę samą cząsteczkę w różnych warunkach, mogli odróżnić zmiany wynikające z biologii komórkowej od różnic w szybkości reakcji click. Łącząc dane CHAMP z analizą komputerową, powiązali pewne cechy fizykochemiczne — takie jak polarna powierzchnia, zdolność do tworzenia wiązań wodorowych i konkretne szkielety pierścieniowe — ze silniejszym rozpoznawaniem przez efflux oparty na TolC. Tego rodzaju profilowanie na dużą skalę zaczyna wyznaczać zasady projektowania molekuł, które albo unikają pomp, albo skuteczniej korzystają z porin.
Co to oznacza dla przyszłych antybiotyków
Mówiąc prosto, praca ta przekształca E. coli w czujnik o wysokiej przepustowości, który informuje dokładnie, jaka ilość testowanego związku dociera do części komórki, gdzie znajduje się wiele miejsc docelowych leków. CHAMP nie zastępuje testów określających, czy bakterie zostają zabite, ale wypełnia istotną lukę, rozdzielając „dostanie się do środka” od „wywołania efektu”. Dzięki możliwości zmierzenia ponad tysiąca molekuł w różnych mutantnych lub chemicznie zmodyfikowanych szczepach w ciągu dni, badacze mogą systematycznie poznać, które cechy chemiczne sprzyjają wnikaniu, redukują efflux lub korzystają z partnerów zaburzających błonę. Ta wiedza powinna przyspieszyć projektowanie nowych antybiotyków i leków pomocniczych, które potrafią przełamać potężne mechanizmy obronne patogenów Gram‑ujemnych, zanim oporność pozbędzie się kolejnych pozycji armamentu antybiotykowego.
Cytowanie: Ongwae, G.M., Liu, Z., Feng, S. et al. Click-based determination of accumulation of molecules in Escherichia coli. Nat Commun 17, 2008 (2026). https://doi.org/10.1038/s41467-026-68717-5
Słowa kluczowe: oporność na antybiotyki, Escherichia coli, przepuszczalność leków, pompy wypompowujące, chemia click