Clear Sky Science · pl
Kacheksja nowotworowa w niedrobnokomórkowym raku płuca z mutacją STK11/LKB1 zależy od wydzielanego przez guz GDF15
Dlaczego niektóre raki płuca wywołują groźną utratę masy
Nowotwór nie zawsze rośnie tylko cicho w jednym miejscu. U wielu osób stopniowo okrada organizm z tłuszczu, mięśni, siły i energii w stanie zwanym wyniszczeniem lub kacheksją. W tym badaniu postawiono pilne pytanie dla pacjentów z powszechną postacią raka płuca: dlaczego niektóre guzy wywołują tak ciężką utratę masy, a inne nie? Badacze odnajdują przyczynę w sygnale stresowym wytwarzanym przez niektóre nowotwory i pokazują, że zahamowanie tego sygnału u zwierząt w dużym stopniu zatrzymuje, a nawet odwraca wyniszczenie.
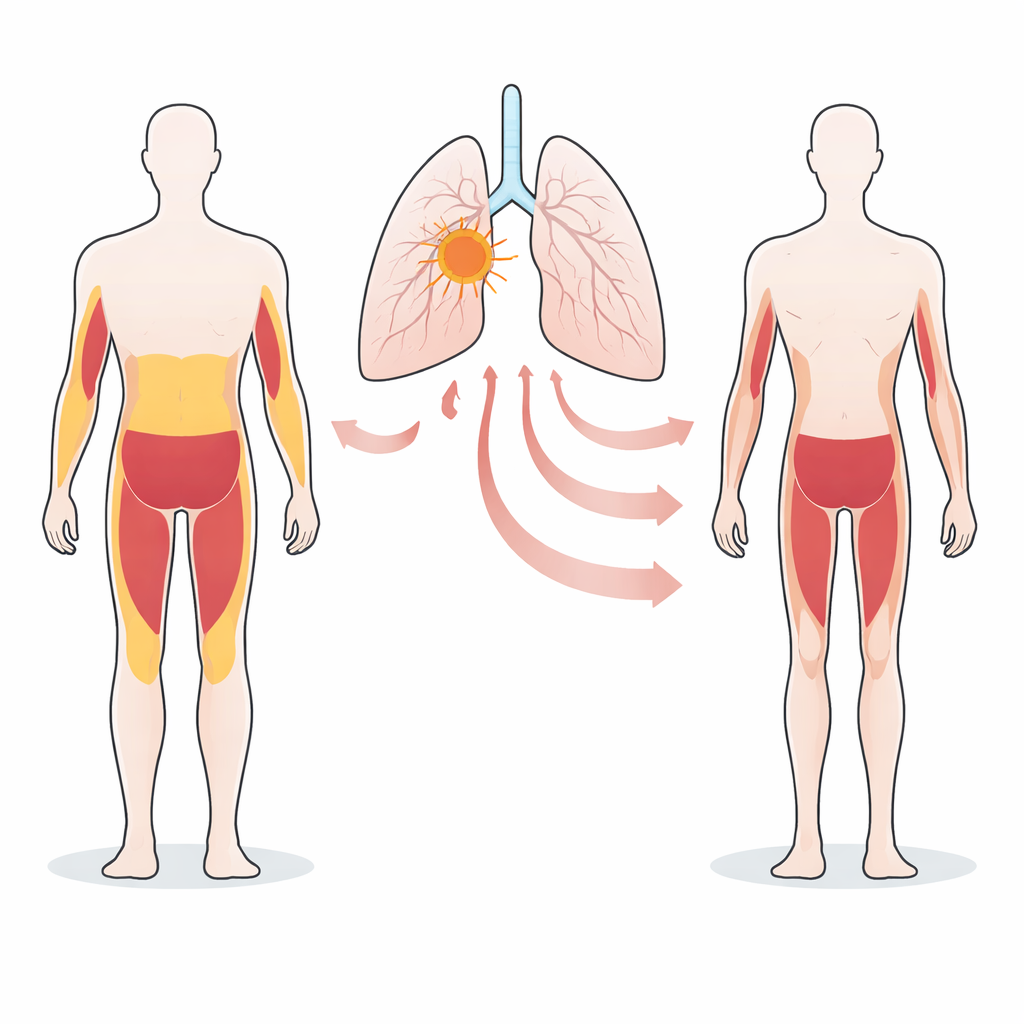
Ukryte powiązanie między genami guza a wyniszczeniem organizmu
Zespół skupił się na niedrobnokomórkowych rakach płuca noszących wadliwe wersje genu STK11/LKB1. Wcześniejsze prace wykazały, że guzy z tą wadą często idą w parze z dużą utratą wagi, tłuszczu i mięśni zarówno u myszy, jak i u pacjentów. Tutaj naukowcy porównali wiele ludzkich linii nowotworowych płuca, które albo wywoływały, albo nie wywoływały wyniszczenia po wszczepieniu do myszy. Stwierdzili, że guzy powodujące wyniszczenie z defektem STK11/LKB1 wytwarzały znacznie większe ilości białka o charakterze hormonu stresu, nazwanego GDF15, które przedostawało się do krwiobiegu. W przeciwieństwie do tego komórki gospodarza przyczyniały się w niewielkim stopniu do poziomu GDF15 we krwi, wskazując na sam guz jako główne źródło.
Dowód, że sygnał z guza napędza utratę masy, tłuszczu i mięśni
Aby sprawdzić, czy GDF15 pochodzący z guza rzeczywiście powoduje wyniszczenie, badacze użyli narzędzi genetycznych do wyłączenia GDF15 wyłącznie w komórkach nowotworowych, pozostawiając inne geny nietknięte. W kilku różnych liniach raka płuca z mutacją STK11/LKB1 wyłączenie GDF15 nie spowolniło wzrostu guza, ale skutecznie chroniło myszy przed utratą masy ciała, masy tłuszczowej, masy mięśniowej i siły chwytu. Ochrona ta występowała zarówno u samców, jak i samic oraz w modelach, gdzie guzy umieszczano pod skórą lub bezpośrednio w płucu, co sugeruje, że efekt wynika z czynników uwalnianych do krwi, a nie z lokalizacji guza. Nawet gdy guzy produkowały jedynie umiarkowane ilości GDF15, przerwanie tego sygnału nadal osłabiało wyniszczenie, pokazując, że stosunkowo niskie poziomy mogą mieć znaczenie biologiczne.
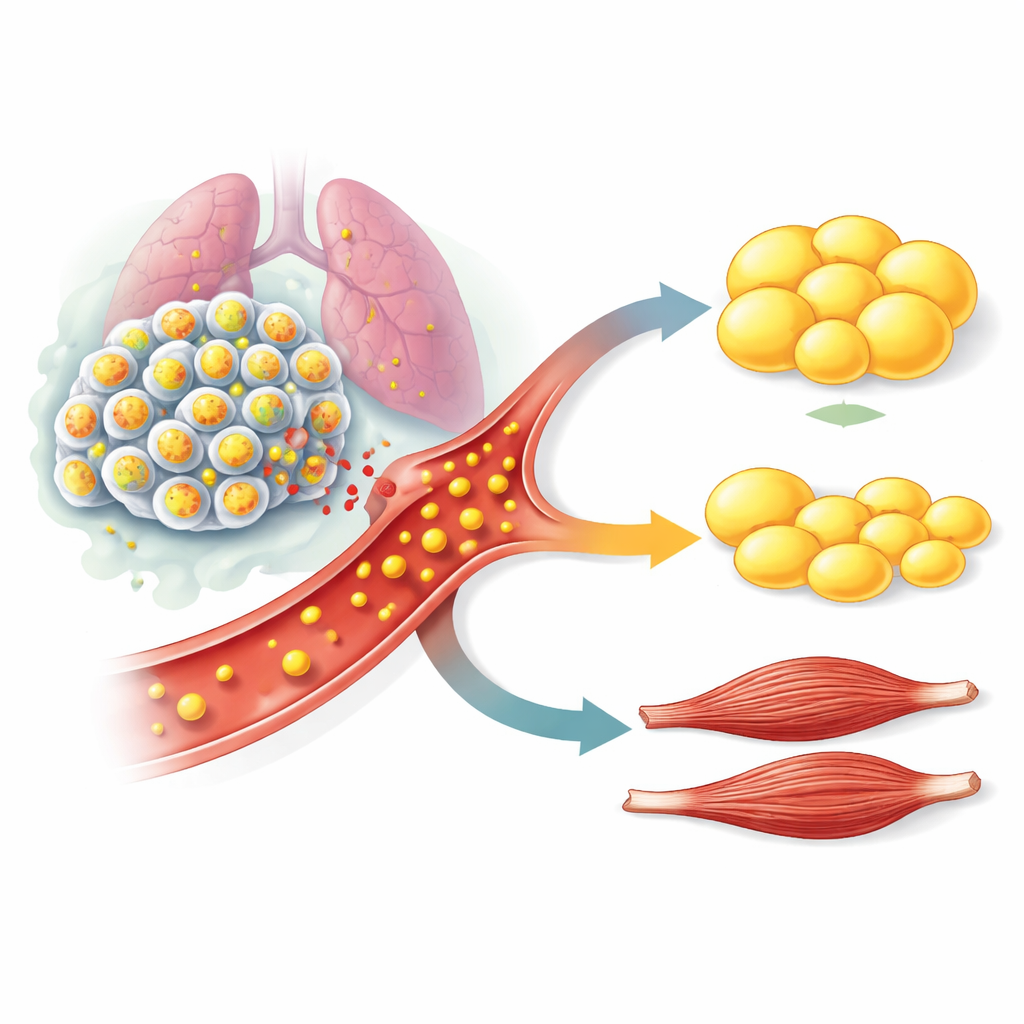
Przeciwciała blokujące sygnał dają obiecujące wyniki terapeutyczne
Ponieważ firmy farmaceutyczne już opracowują przeciwciała neutralizujące GDF15, zespół sprawdził, czy takie podejście może pomóc w ich modelach. Leczyli myszy z guzami z mutacją STK11/LKB1 przeciwciałem blokującym GDF15 podobnym do tego, które jest obecnie w badaniach klinicznych. Podawane wcześnie przeciwciało zapobiegało zwykłej utracie tłuszczu, mięśni i siły, nie wpływając na tempo wzrostu guza. Podawane później — po tym, jak zwierzęta już utraciły dużą część tłuszczu — to samo przeciwciało zatrzymywało dalszy spadek i częściowo przywracało zapasy energetyczne i masę mięśniową. Podobne rezultaty zaobserwowano w modelu raka płuca u myszy z intactnym układem odpornościowym, co sugeruje, że wyniki nie ograniczają się do zwierząt z upośledzonym układem odpornościowym.
Jak zestresowany guz włącza przełącznik wyniszczenia
Badanie bada również, dlaczego guzy z mutacją STK11/LKB1 wytwarzają tak dużo GDF15. Komórki używają wewnętrznego systemu alarmowego, zwanego odpowiedzią na stres, aby radzić sobie z niedoborem składników odżywczych i innymi zagrożeniami. W nowotworach pozbawionych STK11/LKB1 ten alarm jest przewlekle aktywny, zwiększając produkcję i przetwarzanie GDF15 do jego dojrzałej, wydzielanej formy. Gdy badacze przywrócili działający gen STK11/LKB1 do ludzkiej linii raka płuca, odpowiedź na stres ucichła. Poziomy GDF15 w guzie i we krwi gwałtownie spadły, poprawił się apetyt, a zwierzęta przestały rozwijać kacheksję, mimo że guzy nadal były obecne.
Co to oznacza dla pacjentów z rakiem płuca
Dla osób z niedrobnokomórkowym rakiem płuca z mutacjami STK11/LKB1 ta praca sugeruje, że sam guz może działać jak narząd dokrewny, uwalniając GDF15 do krwiobiegu i napędzając ogólnoustrojowe wyniszczenie. U myszy blokowanie GDF15 — zarówno przez usunięcie go z guza, jak i przez zastosowanie przeciwciała w krążeniu — znacznie zmniejszało utratę tłuszczu i mięśni bez bezpośredniego kurczenia guza. To rodzi możliwość, że u około 15 procent pacjentów z rakiem płuca z defektem STK11/LKB1 terapie przeciwko GDF15 mogłyby pomóc zachować siłę i masę ciała przy szerokim zakresie stężeń GDF15 we krwi. Innymi słowy, przyciszenie tego pojedynczego sygnału pochodzącego z guza może w przyszłości zaoferować praktyczny sposób złagodzenia jednego z najbardziej wyniszczających powikłań raka.
Cytowanie: Yu, J., Guo, T., Gupta, A. et al. Cancer cachexia in STK11/LKB1-mutated non-small cell lung cancer is dependent on tumor-secreted GDF15. Nat Commun 17, 2182 (2026). https://doi.org/10.1038/s41467-026-68702-y
Słowa kluczowe: kacheksja nowotworowa, niedrobnokomórkowy rak płuca, GDF15, mutacja STK11 LKB1, utrata mięśni i tłuszczu