Clear Sky Science · pl
Mikroskopia strukturalna o dużej szybkości przy ślepym odtworzeniu za pomocą nie nadzorowanego rozwijania algorytmu
Bardziej ostre filmy życia wewnątrz komórek
Nowoczesna biologia często opiera się na obserwowaniu żywych komórek w działaniu, jednak wiele kluczowych struktur jest po prostu zbyt małych i zbyt szybkich, by zwykłe mikroskopy mogły je wyraźnie zarejestrować. W artykule przedstawiono nowy sposób przekształcania rozmytych, szybko wykonywanych obrazów w ostre, wysoce szczegółowe filmy w czasie rzeczywistym, bez potrzeby idealnie skalibrowanego sprzętu. Metoda nazwana rozwiniętą ślepą mikroskopią oświetlenia strukturalnego (UBSIM) ma szansę uczynić zaawansowane, szybkobieżne obrazowanie komórek bardziej dostępnym dla typowych laboratoriów biologicznych.
Dlaczego zwykłe mikroskopy zawodzą
Tradycyjne mikroskopy optyczne ogranicza zjawisko dyfrakcji — podstawowa właściwość światła, która rozmazuje drobne detale mniejsze niż kilkaset nanometrów. Mikroskopia oświetleniem strukturalnym (SIM) przeciwdziała temu, oświetlając próbkę wzorem i wykorzystując powstałą interferencję do wydobycia dodatkowych szczegółów, co w przybliżeniu podwaja rozdzielczość. Jednak klasyczne SIM wymaga precyzyjnie znanych wzorców oświetlenia i starannej kalibracji, co bywa kosztowne i podatne na błędy. Nowsza odmiana, blind‑SIM, łagodzi te wymagania sprzętowe, pozwalając na przypadkowe wzory i jednoczesne odtwarzanie próbki oraz oświetlenia z danych. Wadą jest to, że proces rozwiązania takiego układu jest powolny i iteracyjny, zajmując od sekund do minut na klatkę — zdecydowanie za długo, by tworzyć filmy w czasie rzeczywistym z żywych komórek.
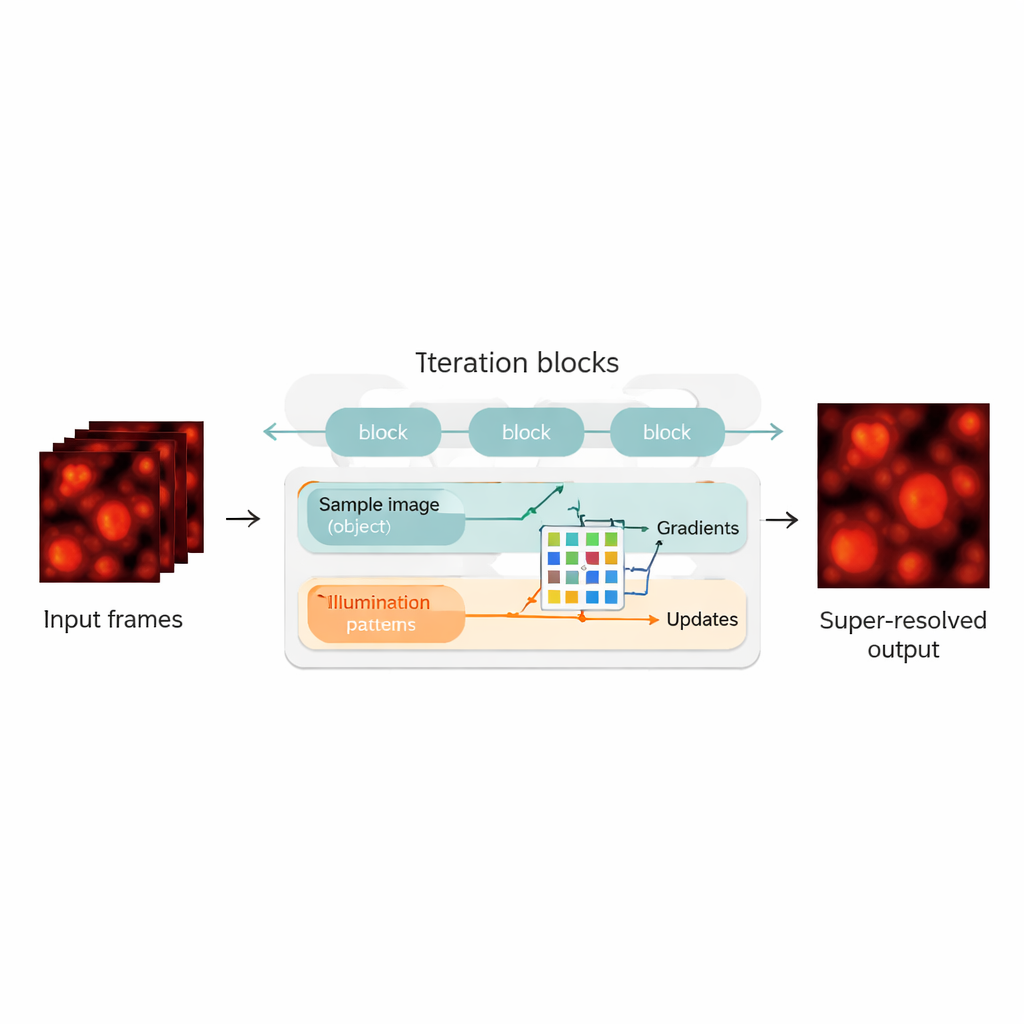
Połączenie fizyki z sieciami neuronowymi
Autorzy wypełniają tę lukę, przekształcając rekonstrukcję blind‑SIM w hybrydę między modelem opartym na fizyce a siecią neuronową. „Rozwijają” oryginalny algorytm iteracyjny — każda iteracja staje się warstwą w sieci neuronowej, tworząc łańcuch bloków aktualizacyjnych. W każdym bloku metoda ocenia, jak dobrze obecne przypuszczenie próbki i oświetlenia wyjaśnia zmierzone obrazy, oblicza gradienty (kierunki poprawy), a następnie przekazuje je do zwartej splotowej sieci neuronowej. Sieć ta uczy się wykonywać mądrzejsze kroki korekcyjne, pełniąc rolę automatycznie dostrajającego przyspieszacza dla pierwotnego algorytmu. Kluczowe jest to, że UBSIM jest trenowany w sposób nienadzorowany: zamiast wymagać perfekcyjnych obrazów jako prawdy odniesienia, potrzebny jest jedynie fizyczny model tego, jak światło przechodzi przez mikroskop. To zmniejsza ryzyko, że sieć „halucynuje” pozornie realistyczne, lecz błędne struktury.
Szybko, dokładnie i mniej pod wpływem zgadywania
Aby przetestować UBSIM, zespół najpierw użył symulowanych obrazów mikroskopowych, gdzie prawdziwe struktury są znane. Pokazali, że UBSIM odzyskuje około dwukrotnie lepszą rozdzielczość niż zwykłe obrazy szerokopolowe, porównywalną z klasycznym blind‑SIM, ale działa dwa do trzech rzędów wielkości szybciej — obraz 256×256 można zrekonstruować w około 10 milisekund zamiast w sekundach. Wyniki jakości obrazu, w tym błędy, miary podobieństwa i stosunku sygnału do szumu, poprawiły się znacząco w porównaniu z konwencjonalnymi obrazami. UBSIM okazał się także bardziej wiarygodny niż popularne sieci głębokiego uczenia do super‑rozdzielczości w konfrontacji z nieznanymi danymi. Podczas gdy standardowe sieci trenowane na jednym typie struktur miały skłonność do narzucania tego wzoru na nowe, różne próbki — wprowadzając subtelne, lecz mylące artefakty — UBSIM zachowywał spójność odwzorowania, ponieważ jest zakotwiczony w fizyce obrazowania, a nie tylko w przykładach wizualnych.
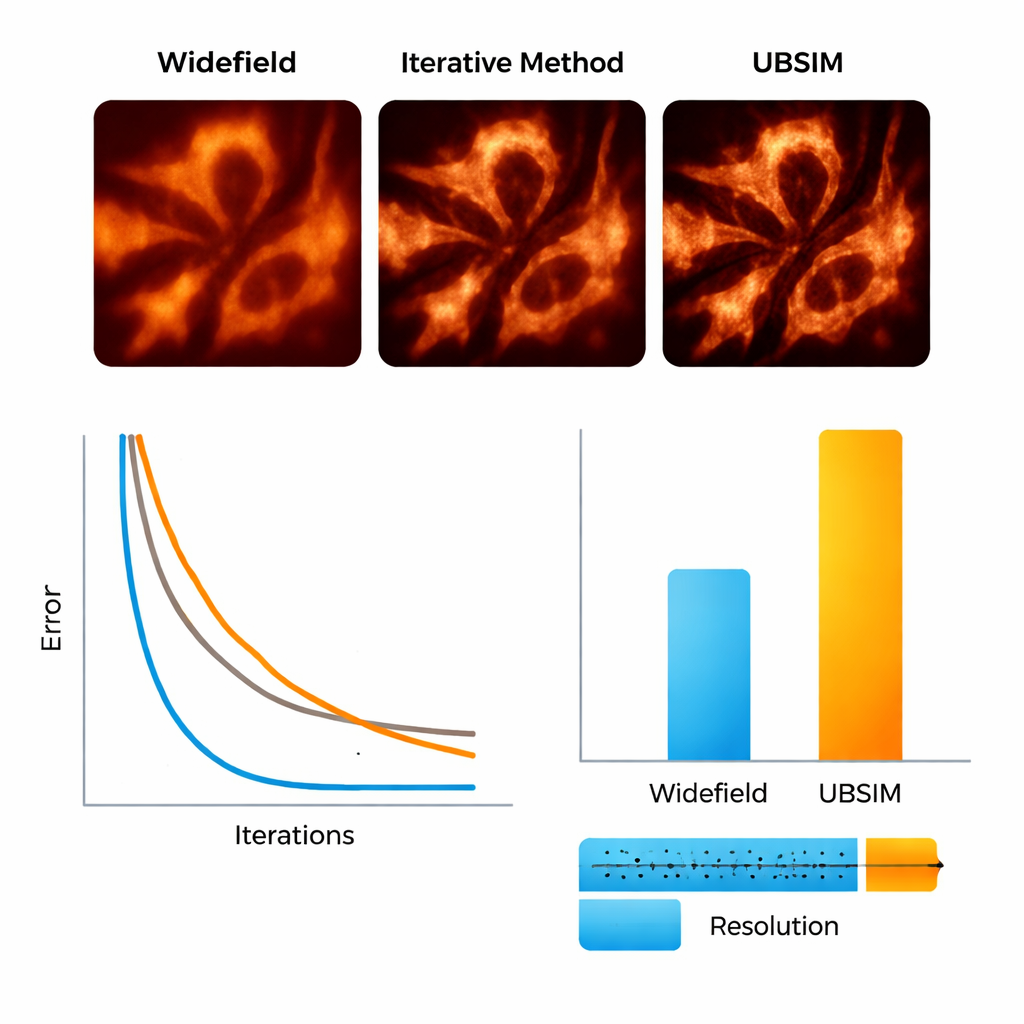
Obserwacja szkieletów i błon komórkowych w ruchu
Następnie badacze przeszli do prawdziwych próbek biologicznych. Korzystając z elastycznego układu rzutującego losowe wzory typu speckle na żywe komórki, zarejestrowali włókna aktyny — białkowy „ruszt” wewnątrz komórek — oraz retikulum endoplazmatyczne (ER), rozgałęzioną sieć błon zaangażowaną w produkcję białek i reakcję na stres komórkowy. Dzięki UBSIM włókna aktyny, które w zwykłych obrazach wyglądały jak rozmyte pasma, stały się wyraźnie oddzielonymi nitkami, przy czym rozdzielczość poprawiła się z około 300 nanometrów do około 150 nanometrów. Co najważniejsze, UBSIM umożliwił super‑rozdzielczość w tempie wideo: rejestrując surowe dane z prędkością do 100 klatek na sekundę i rekonstruując do 50 super‑rozdzielczych klatek na sekundę, zespół mógł obserwować wzrost, zapadanie się i reorganizację kanalików ER w czasie rzeczywistym. Te dynamiki, zachodzące w ułamkach sekundy do kilku sekund, są zwykle trudne do zwizualizowania z wystarczającą szczegółowością.
Co to oznacza dla przyszłego obrazowania komórek
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że UBSIM sprawia, iż znacznie praktyczniejsze staje się obserwowanie małych struktur komórkowych w ruchu, w czasie rzeczywistym, z klarownością przekraczającą normalne ograniczenia mikroskopów świetlnych — i to bez wymogu perfekcyjnej kalibracji sprzętu czy ogromnych zestawów treningowych. Łącząc niezawodność modeli opartych na fizyce z szybkością współczesnych sieci neuronowych, podejście to przekształca zestawy zaszumionych, wzorcowych obrazów w godne zaufania, ultracienkie filmy wystarczająco szybkie do rutynowych eksperymentów. W miarę dalszego udoskonalania metody i łączenia jej z lepszymi strategiami oświetleniowymi, może pomóc badaczom badać, jak organelle takie jak ER reagują na stres, jak szkielet komórkowy reorganizuje się podczas ruchu lub podziału oraz jak choroby wpływają na architekturę komórkową na poziomie nanometrycznym.
Cytowanie: Burns, Z., Zhao, J., Sahan, A.Z. et al. High-speed blind structured illumination microscopy via unsupervised algorithm unrolling. Nat Commun 17, 1967 (2026). https://doi.org/10.1038/s41467-026-68693-w
Słowa kluczowe: mikroskopia o nadrozdzielczości, oświetlenie strukturalne, uczenie maszynowe, obrazowanie żywych komórek, dynamika retikulum endoplazmatycznego