Clear Sky Science · pl
Funkcjonalne i strukturalne wglądy w interakcje między β-arrestyną 1 a Gαs lub Gαi1
Dlaczego to ma znaczenie dla zdrowia i medycyny
Wiele współczesnych leków — od tabletek przeciwalergicznych po leki sercowe czy terapie psychiatryczne — działa poprzez celowanie w dużą rodzinę powierzchniowych białek komórkowych zwanych receptorami sprzężonymi z białkami G (GPCR). Receptory te przekazują sygnały do wnętrza komórki przy pomocy dwóch głównych pomocników: białek G oraz białek zwanych beta-arrestynami. W tym badaniu przyjrzano się, jak jedna beta-arrestyna (beta-arrestyna 1) bezpośrednio „rozmawia” z dwoma typami białek G wewnątrz komórki. Zrozumienie tej ukrytej rozmowy może pomóc naukowcom zaprojektować precyzyjniejsze leki o mniejszych skutkach ubocznych, poprzez subtelne dostrojenie przepływu sygnałów wewnątrz naszych komórek.
Dwaj główni przekaźnicy we wnętrzu komórek
Kiedy hormon lub lek wiąże się z GPCR na powierzchni komórki, uruchamiane są dwa zasadnicze szlaki komunikacji. Jeden wykorzystuje białka G, które działają jak molekularne timery, przełączając się za pomocą wymiany jednego małego nukleotydu (GDP) na inny (GTP). Drugi wykorzystuje beta-arrestyny, które mogą zarówno wyłączać sygnalizację zależną od białek G, jak i uruchamiać własne szlaki sygnałowe. Przez długi czas badacze skupiali się głównie na tym, jak receptory oddzielnie komunikują się z białkami G lub z beta-arrestynami. Nowsze prace sugerowały jednak, że białka G i beta-arrestyny mogą też wzajemnie się wiązać, a nawet tworzyć duże „mega-kompleksy” z receptorem. Szczegóły tego, jak te białka łączą się ze sobą i co to oznacza dla sygnalizacji, pozostawały jednak niejasne.
Pomiary, kto z kim się wiąże
W tym badaniu zespół skupił się na beta-arrestynie 1 oraz na dwóch „alfa” podjednostkach białek G: Gαs, który zwykle stymuluje aktywność komórki, oraz Gαi1, który ją zazwyczaj tłumi. Zastosowano czułą technikę pomiaru wiązania, aby sprawdzić, jak silnie oczyszczona beta-arrestyna 1 wiąże się z każdym z białek G w różnych warunkach. Okazało się, że kluczowym czynnikiem nie jest to, czy białko G jest „włączone” czy „wyłączone”, lecz czy beta-arrestyna 1 znajduje się w bardziej aktywnej, elastycznej formie. Wersja beta-arrestyny 1 pozbawiona ogonka — zachowująca się jak luźny, aktywny zespół konformacji — wiązała się mocno zarówno z Gαs, jak i z Gαi1. Natomiast forma spoczynkowa beta-arrestyny 1, albo forma „zablokowana” przez peptyd przypominający ogonek receptora, wiązała się słabo lub wcale. Sugeruje to, że białka G preferencyjnie rozpoznają beta-arrestynę 1, gdy ta przyjmie kształty przypominające aktywne, które mogą występować po aktywacji receptora. 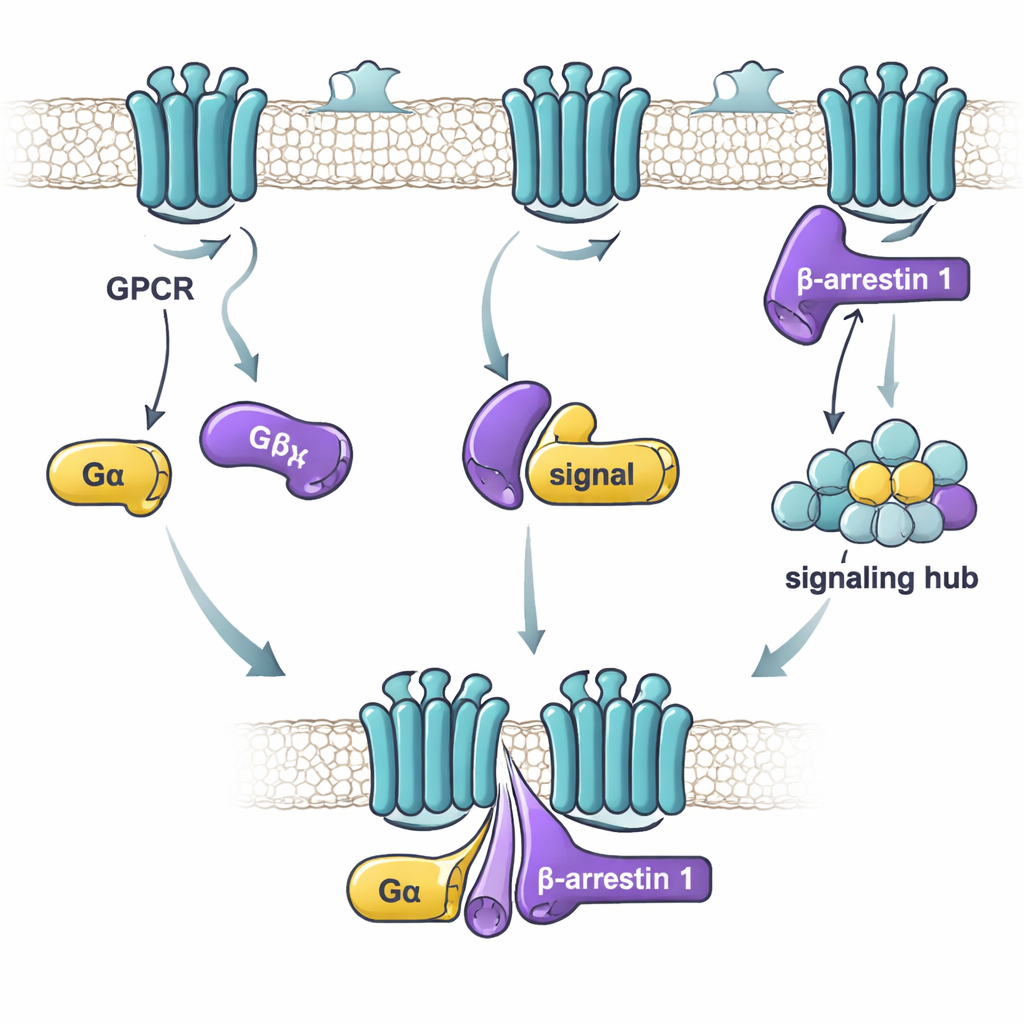
Obserwowanie subtelnych zmian kształtu
Aby zobaczyć, jak wiązanie wpływa na konformację białek, zespół użył metody śledzącej, jak szybko atomy wodoru w szkielecie białka wymieniają się na cięższy wodór z rozpuszczalnika. Wolniejsza wymiana zwykle oznacza, że dany region stał się bardziej chroniony lub sztywniejszy; szybsza wymiana wskazuje na większą elastyczność lub odsłonięcie. Gdy fragment beta-arrestyny 1 o konformacji przypominającej aktywną związał się z Gαs lub Gαi1, oba białka G wykazały wyraźne zmiany wzorców w kilku regionach, co wskazuje na przeorganizowanie wokół kompleksu. Natomiast sama beta-arrestyna 1 zmieniała się tylko nieznacznie, głównie w elastycznych pętlach. Pracując z izolowanymi domenami białek G, badacze wykazali też, że zarówno główna katalityczna część „podobna do Ras”, jak i otaczająca ją domena alfa-helikalna przyczyniają się do wiązania. W przypadku Gαs domena helikalna odgrywa szczególnie silną rolę; w przypadku Gαi1 obie domeny mają mniej więcej równy wkład.
Funkcja bez przełączania głównego włącznika
Następne pytanie brzmiało, czy ten bezpośredni kontakt zmienia sposób, w jaki białka G się aktywują. Zespół użył fluorescencyjnego sondy naśladującej GTP, która świeci, gdy białko G przełącza się z GDP na GTP — standardowy odczyt aktywacji. Ku zaskoczeniu, dodanie beta-arrestyny 1 nie zmieniało szybkości ani zakresu tej wymiany nukleotydu dla Gαs ani Gαi1. Innymi słowy, beta-arrestyna 1 nie działa jak klasyczny enzym „włączający” białka G. Zamiast tego jej wpływ ujawniał się na własnej strukturze. Przy użyciu sprytnie zaprojektowanej beta-arrestyny 1, której ruch ogonka można było śledzić za pomocą fluorescencji, stwierdzono, że aktywne Gαs, ale nie Gαi1, zwiększa uwalnianie ogonka C‑terminalnego beta-arrestyny, gdy obecny jest peptyd pochodzący z receptora. W komórkach żywych dodatkowe obrazowanie i sensory transferu energii potwierdziły, że Gαs i beta-arrestyna 1 zbliżają się do siebie po stymulacji hormonem i że Gαs pomaga przesunąć beta-arrestynę 1 w stronę bardziej aktywnej konformacji.
Nowa warstwa kontroli w sygnalizacji komórkowej
Sumując wyniki, badanie proponuje, że Gαs i Gαi1 wiążą się bezpośrednio z beta-arrestyną 1, ale w nieco odmienny sposób i z odmiennymi konsekwencjami. Żadne z białek G nie ma zmienionego głównego zachowania „włącz/wyłącz” wskutek tego kontaktu. Zamiast tego, szczególnie w przypadku Gαs, interakcja działa bardziej jak pokrętło do drobnego dostrojenia beta-arrestyny 1, popychając ją lub stabilizując w bardziej aktywnej formie z uwolnionym ogonkiem. To dodaje wcześniej niedocenianą warstwę do sygnalizacji GPCR: receptory mogą koordynować białka G i beta-arrestyny, ale białka G i beta-arrestyny mogą też bezpośrednio wzajemnie się modulować. W dłuższej perspektywie mapowanie tych subtelnych interakcji może pomóc projektantom leków prowadzić sygnalizację po korzystnych szlakach — wzmacniając pożądane ścieżki i unikając tych odpowiedzialnych za skutki uboczne.
Cytowanie: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
Słowa kluczowe: Receptory sprzężone z białkami G, beta-arrestyna, sygnalizacja białek G, mechanizmy sygnalizacji komórkowej, biologia strukturalna