Clear Sky Science · pl
Analiza epigenomu wykrywa metylację DNA pośredniczącą w ryzyku kardiometabolicznym związanym z leczeniem u osób, które przeżyły raka w dzieciństwie
Dlaczego następstwa raka utrzymują się w organizmie
Dzięki lepszym terapiom większość dzieci z rakiem dorasta. Jednak wielu z tych osób boryka się dekady później z nowymi problemami zdrowotnymi, takimi jak otyłość, nadciśnienie i zaburzenia przypominające cukrzycę. W tym badaniu postawiono ważne pytanie: w jaki sposób leczenie stosowane w dzieciństwie pozostawia tak długie ślady w układzie sercowo‑metabolicznym? Analizując chemiczne znaczniki na DNA w komórkach krwi, badacze odsłaniają wskazówki, że przebyta chemioterapia i radioterapia mogą „przeprogramowywać” organizm w sposób podnoszący długoterminowe ryzyko kardiometaboliczne.
Śledzenie ukrytych zagrożeń u dorosłych, którzy przeszli raka w dzieciństwie
Zespół przebadał prawie 3 000 dorosłych, którzy przeżyli raka w dzieciństwie i są objęci długoterminową kohortą St. Jude Lifetime Cohort. Osoby te jako dzieci otrzymywały różne terapie cytotoksyczne oraz radioterapię obejmującą głowę lub tułów (klatka piersiowa, brzuch, miednica), a następnie po latach wróciły na szczegółowe badania zdrowotne i badania krwi. Naukowcy skupili się na pięciu kluczowych problemach kardiometabolicznych, które zwiększają ryzyko chorób serca i przedwczesnej śmierci: otyłość, nieprawidłowa glikemia, podwyższone trójglicerydy, wysoki cholesterol i nadciśnienie. Porównując osoby z tymi zaburzeniami i bez nich, przeszukali miliony miejsc w genomie pod kątem różnic w metylacji DNA — drobnych chemicznych przełączników, które pomagają kontrolować, czy geny są włączane czy wyłączane.
Chemiczne znaczniki na DNA jako pamięć leczenia
W całym genomie badacze znaleźli niemal 1 900 miejsc metylacji DNA, których poziomy wiązały się z co najmniej jednym z pięciu problemów kardiometabolicznych. Większość tych miejsc odnosiła się do jednego konkretnie problemu, ale niewielka grupa wydawała się być „węzłami” powiązanymi z wieloma zaburzeniami. Pięć kluczowych miejsc, położonych blisko dwóch genów nazwanych CPT1A i LMNA, wiązało się jednocześnie ze wszystkimi pięcioma ryzykami kardiometabolicznymi. Wiadomo, że te geny wpływają na gospodarkę lipidową i strukturę komórek, co sugeruje, że leczenie może zakłócać wspólne szlaki metaboliczne i sercowo‑naczyniowe. Wiele zmian metylacyjnych pokrywało się z sygnałami wcześniej obserwowanymi w populacji ogólnej, szczególnie tymi związanymi z zapaleniem, ale inne wydawały się unikalne dla osób po chorobie nowotworowej — co sugeruje, że leczenie zostawia własny, wyróżniający się ślad biologiczny.
Łączenie terapii, zmian w DNA i choroby
Następnym krokiem było sprawdzenie, czy te zmiany metylacyjne rzeczywiście pośredniczą w przełożeniu leczenia na późniejszą chorobę, a nie tylko towarzyszą im. Badacze skupili się na nowych lub pogarszających się problemach kardiometabolicznych, które rozwinęły się dopiero po pobraniu próbki krwi, zachowując chronologię: leczenie → zmiana w DNA → choroba. Wykorzystując analizy mediacyjne statystycznie określili 24 miejsca metylacji, które łącznie wyjaśniały do około jednej czwartej związku między określonymi terapiami a późniejszymi problemami kardiometabolicznymi. Radioterapia głowy i tułowia wykazywała szczególnie silne wzorce: grupy miejsc metylacji wyjaśniały w przybliżeniu 10–20% wpływu tych radioterapii na nieprawidłową glikemię. Jedno wyróżniające się miejsce, blisko genu ANTXR2, wydawało się pośredniczyć w około 20% efektu radioterapii tułowia na późniejsze problemy z glukozą.
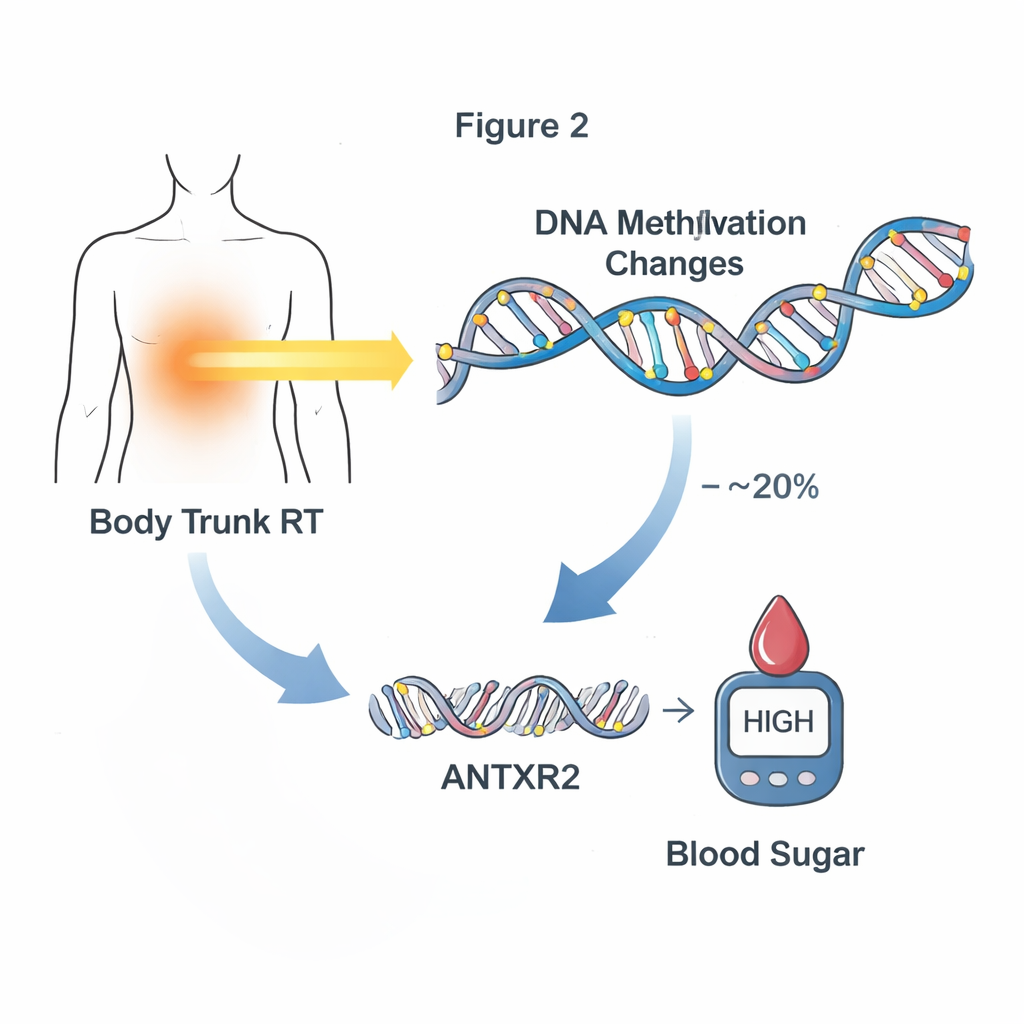
Od znaków na DNA do aktywności genów
Aby zrozumieć, jak te znaczniki metylacyjne mogą zmieniać biologię, zespół przeanalizował aktywność genów w podgrupie uczestników, którzy mieli dane zarówno DNA, jak i RNA z krwi. Znaleźli dziesiątki miejsc metylacyjnych, gdzie wyższy lub niższy poziom metylacji wiązał się ze zmianami w ekspresji pobliskich genów. Wśród nich było kluczowe miejsce mediacyjne blisko ANTXR2, gdzie poziomy metylacji silnie korelowały z ilością ekspresji tego genu, szczególnie u osób, które otrzymały radioterapię tułowia. ANTXR2 pomaga regulować naczynia krwionośne i otaczającą je strukturę tkankową — układy wpływające na to, jak glukoza i insulina przemieszczają się w organizmie. Ten wzorzec sugeruje łańcuch zdarzeń, w którym radioterapia zmienia metylację, co przesuwa aktywność genów, a to z kolei może skłaniać organizm ku nieprawidłowej glikemii.
Co to oznacza dla osób po leczeniu i opieki w przyszłości
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że leczenia raka w dzieciństwie nie tylko uszkadzają tkanki w danym momencie; mogą też pozostawić długotrwałe „notatki” na DNA, które kształtują zdrowie przez dekady. W tym badaniu niektóre z tych notatek — zmiany metylacji DNA — pomagają wyjaśnić, dlaczego niektórzy byli pacjenci częściej rozwijają otyłość, podwyższone stężenia lipidów we krwi czy zaburzenia glikemii związane z cukrzycą i chorobami serca. Choć te chemiczne znaczniki to tylko część historii, w przyszłości mogą służyć jako biomarkery we krwi do identyfikacji osób o najwyższym ryzyku i do testowania, czy zmiany stylu życia lub nowe terapie mogą bezpiecznie „przepisać” część tej epigenetycznej przeszłości. Praca przybliża opiekę nad osobami po chorobie nowotworowej do medycyny precyzyjnej: wykorzystania molekularnych śladów przebytego leczenia do wcześniejszego, bardziej dopasowanego zapobiegania chorobom serca i metabolicznym.
Cytowanie: Eulalio, T., Kim, Y., Meng, X. et al. Epigenome-wide analysis identifies DNA methylation mediators of treatment-related cardiometabolic risk in survivors of childhood cancer. Nat Commun 17, 1979 (2026). https://doi.org/10.1038/s41467-026-68689-6
Słowa kluczowe: osoby, które przeżyły raka w dzieciństwie, metylacja DNA, ryzyko kardiometaboliczne, radioterapia, epigenetyka