Clear Sky Science · pl
Okotranslacyjne określanie struktur czwartorzędowych w fabrykach chaperonowych
Jak komórkowe „linie montażowe” dbają o porządek w wielkich maszynach
W każdej z naszych komórek tysiące części białkowych muszą składać się w złożone maszyny molekularne — od silników kopiujących DNA po fabryki wytwarzające inne RNA. To badanie stawia pozornie proste pytanie o dalekosiężnych konsekwencjach: jak komórki decydują, w czasie rzeczywistym, które białkowe pomocniki będą towarzyszyć każdej nowej części podczas jej syntezy i jak utrzymują ten proces zorganizowany w chaotycznym, płynnym środowisku komórki?
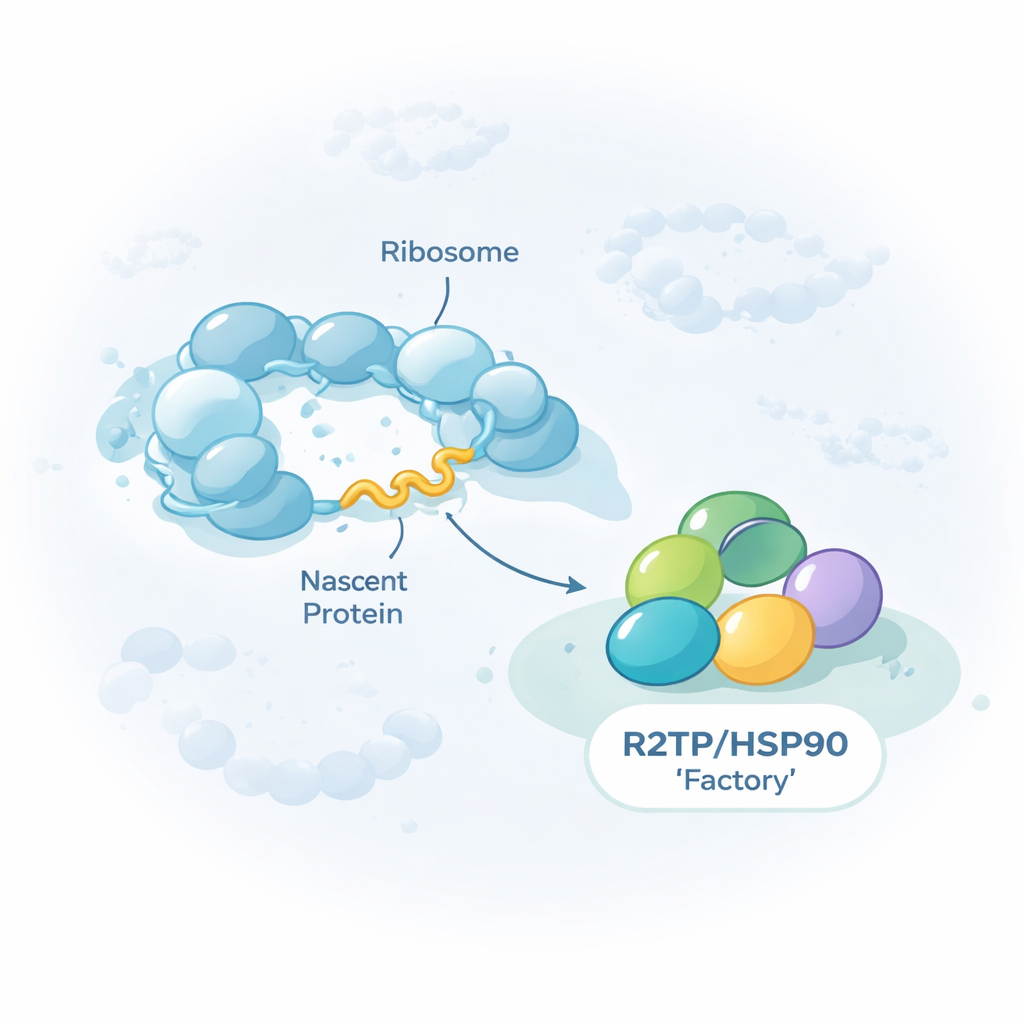
Uniwersalny pomocnik dla komórkowych mega-maszyn
Praca koncentruje się na grupie pomocniczych białek, chaperonów znanych jako HSP90/R2TP. Zamiast fałdować pojedyncze białka, ten chaperon wyspecjalizowany jest w składaniu olbrzymich kompleksów wieloczęściowych, w tym trzech jądrowych polimeraz RNA transkrybujących DNA na RNA, pewnych cząstek RNA–białko oraz dużych maszyn przebudowujących struktury DNA. Autorzy pokazują, że R2TP nie spotyka się z klientami dopiero po ich ukończeniu. Często przyłącza się już podczas ich syntezy na rybosomach, komórkowych maszynach wytwarzających białka. Pobierając R2TP z komórek ludzkich i sekwencjonując towarzyszące mu RNA, znaleźli około 150 mRNA, których kodowane białka są kontaktowane przez R2TP w trakcie własnego tłumaczenia.
Pomocnicy towarzyszący rosnącym łańcuchom białkowym
Aby sprawdzić, czy to wiązanie rzeczywiście zachodzi podczas syntezy białka, zespół użył leków, które zamrażają lub zaburzają translację. Gdy zastosowali związki odrywające rosnące łańcuchy białkowe od rybosomów, większość mRNA zniknęła z uchwytu R2TP. Natomiast gdy użyli leku, który tylko wstrzymuje ruch rybosomów, pozostawiając łańcuchy nowo syntetyzowane, wiązanie R2TP wzrosło. Zastosowanie skonstruowanych reporterów RNA potwierdziło to: jeśli translacja była sztucznie zatrzymana wcześnie, chaperon przestawał wiązać wiadomość. Razem te wyniki wskazują na jasną zasadę zaangażowania: R2TP rozpoznaje swoich klientów przede wszystkim przez pojawiający się łańcuch białkowy wychodzący z rybosomu, a nie przez sekwencję RNA samego mRNA.
„Fabryki” budowane przez chaperony, grupujące wybrane wiadomości
Wykorzystując zaawansowane obrazowanie pojedynczych cząsteczek, autorzy dokonali zaskakującego odkrycia. Zamiast zobaczyć wiele różnych wiadomości losowo rozproszonych, zaobserwowali, że niektóre kluczowe mRNA — szczególnie te kodujące główne podjednostki polimerazy RNA II oraz duży czynnik składania intronów PRPF8 — często gromadziły się w jasnych ogniskach w cytoplazmie. Te ogniska były wzbogacone w R2TP i jego partnera HSP90, a także w komponenty rybosomalne i same wytwarzane białka, co świadczyło o tym, że są to aktywne miejsca translacji. Kiedy translacja lub energetyczna aktywność ATPazy R2TP albo HSP90 była zablokowana, ogniska te się rozpuszczały. Autorzy nazywają te struktury „fabrykami R2TP”: wyspecjalizowanymi kondensatami, gdzie skoncentrowane są wybrane mRNA i chaperony, sprzyjając terminowemu, ochronnemu kontaktowi między wyłaniającymi się łańcuchami białkowymi a ich pomocnikami montażowymi.
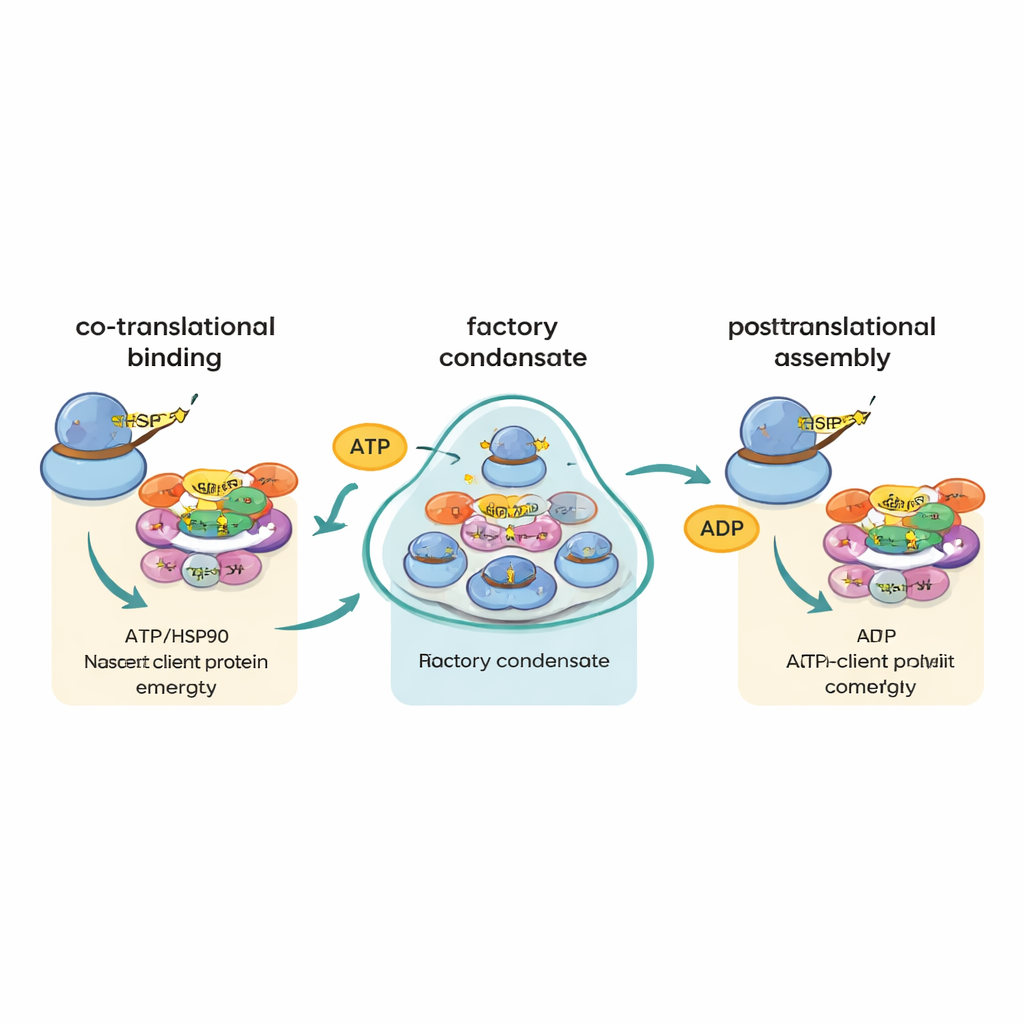
Kierowanie częściami bez dopasowywania ich planów
Jedna z wcześniejszych hipotez głosiła, że mRNA kodujące różne części tego samego kompleksu mogą odnajdywać się nawzajem i być tłumaczone obok siebie, co umożliwiłoby natychmiastowe składanie ich produktów białkowych. Nowa praca w dużej mierze wyklucza ten model „zlokalizowanego planu”. Nawet dla par białek znanych z dołączania do tej samej maszyny, ich mRNA rzadko pojawiały się razem. Zamiast tego dane wspierają inną strategię nazwaną przez autorów „okotranslacyjnym kanałowaniem chaperonowym”, czyli „cha-cha”. W tym schemacie, gdy każde duże lub podatne na składanie białko zaczyna wychodzić z rybosomu, R2TP i HSP90 przyczepiają się i decydują o jego losie, prowadząc je przez kolejne etapy montażu. Same fabryki nie łączą przede wszystkim dopasowanych wiadomości; raczej zwiększają prawdopodobieństwo, że wrażliwe nowe białka szybko spotkają odpowiedni chaperon.
Dlaczego ta ukryta organizacja ma znaczenie dla zdrowia i chorób
Ujawniając, że R2TP i HSP90 nie tylko chronią kruche części białkowe, ale także kształtują miejsce i sposób ich translacji, to badanie odsłania nieoczekiwany poziom organizacji wewnątrzkomórkowej. Mechanizm cha-cha pomaga wyjaśnić, jak komórki wiarygodnie budują ogromne kompleksy molekularne, mimo że mRNA dla ich składników rzadko dzielą to samo miejsce. Sugeruje też, dlaczego defekty chaperonów lub ich cykli energetycznych mogą destabilizować kluczowe maszyny, takie jak polimerazy RNA czy czynniki składania intronów, z konsekwencjami od zaburzeń rozwojowych po raka. W istocie praca pokazuje, że komórki polegają na dynamicznych „fabrykach” chaperonowych, które kierują świeżo powstałe części do właściwych zespołów, utrzymując swoje wewnętrzne mechanizmy zarówno wydajne, jak i uporządkowane.
Cytowanie: Philippe, M., Salloum, S., Slimani, F. et al. Co-translational determination of quaternary structures in chaperone factories. Nat Commun 17, 1978 (2026). https://doi.org/10.1038/s41467-026-68687-8
Słowa kluczowe: chaperony białkowe, okotranslacyjna składanie, maszyny molekularne, polimeraza RNA, komórkowa kontrola jakości