Clear Sky Science · pl
Iteracyjne odkrywanie silnych polimerowych antybiotyków za pomocą wieloetapowego i wielozadaniowego uczenia wobec oporności na antybiotyki
Dlaczego nowe antybiotyki mają znaczenie dla wszystkich
Infekcje oporne na leki rosną na całym świecie, przez co znane choroby stają się trudniejsze, a czasem niemożliwe do leczenia. W badaniu opisano nowy sposób szybkiego odkrywania innego rodzaju antybiotyku: maleńkich syntetycznych polimerów, które mogą zarówno zabijać odporne bakterie, jak i przywracać skuteczność starych leków, takich jak penicylina. Praca łączy zaawansowaną sztuczną inteligencję z chemią i testami na zwierzętach, aby przeszukać ogromną przestrzeń chemiczną, której nie dałoby się zbadać metodą prób i błędów.
Poszukiwanie nowych obrońców w zatłoczonym wszechświecie chemicznym
Tradycyjne antybiotyki zwykle celują w konkretne białka bakteryjne, przed którymi bakterie mogą się stopniowo uchronić. W przeciwieństwie do nich polimery opisane w tym badaniu naśladują nasze własne peptydy obronne, które mechanicznie uszkadzają błony bakteryjne i są mniej podatne na rozwój oporności. Wyzwanie polega na tym, że istnieją dziesiątki tysięcy możliwych struktur polimerowych, a ich zachowanie zależy od subtelnej równowagi ładunku dodatniego oraz części hydrofilowych i hydrofobowych. Ręczne przetestowanie wystarczająco wielu kandydatów, by znaleźć bezpieczne i silne, zajęłoby lata. Autorzy zbudowali bibliotekę kombinatoryczną liczącą około 100 000 powiązanych polimerów zwanych poli(β-aminowymi estrami), z których każdy zaprojektowano tak, by samoistnie tworzył nanocząstki zdolne silnie oddziaływać z powierzchnią komórek bakteryjnych.
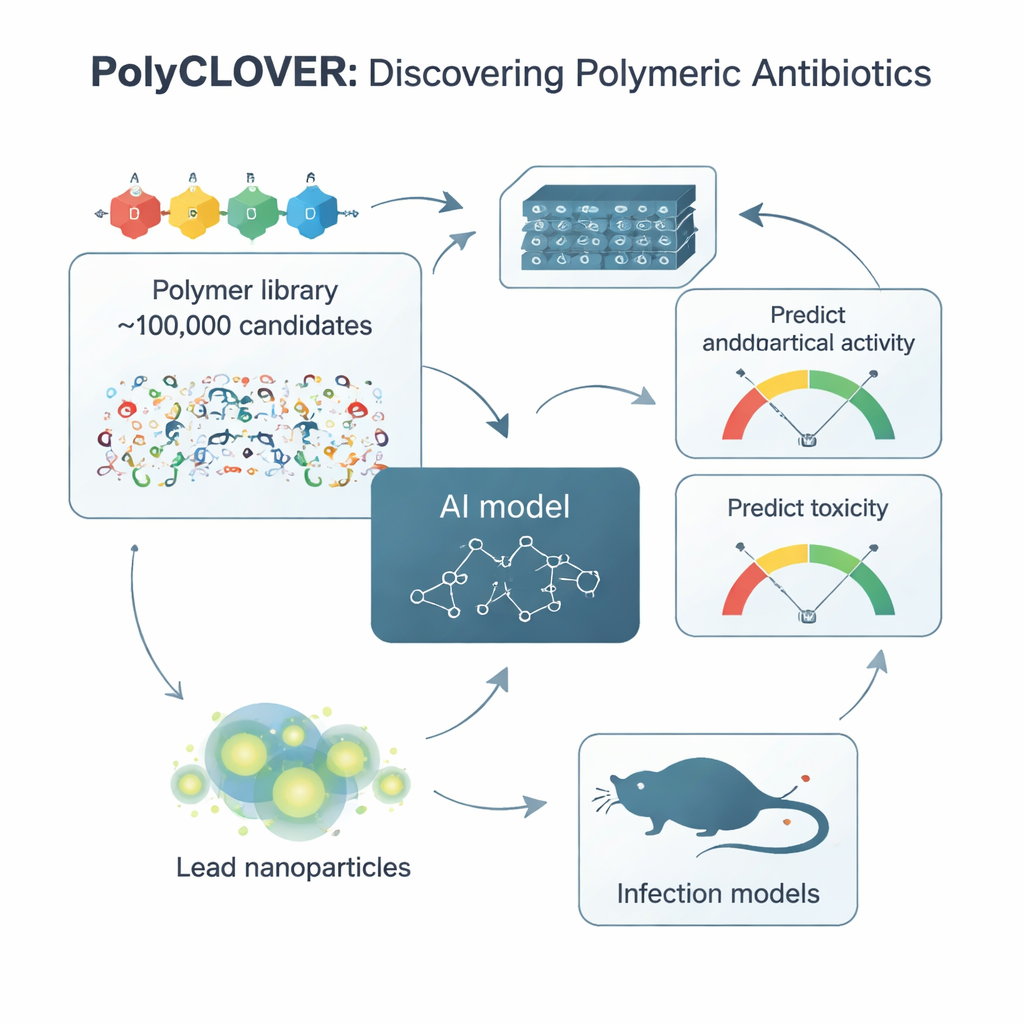
Nauczanie SI rozumienia „mowy ciała” polimerów
Aby poruszać się po tej bibliotece, zespół stworzył ramy nazwane PolyCLOVER. W jego centrum znajduje się sieć neuronowa oparta na grafach, która traktuje każdy polimer jak sieć połączonych atomów, pozwalając modelowi wyczuwać subtelne różnice w strukturze. Ponieważ było bardzo mało oznakowanych przykładów, które polimery są dobrymi lub złymi antybiotykami, badacze zastosowali wieloetapową strategię uczenia samonadzorowanego. Najpierw model trenowano na około milionie nieoznaczonych struktur polimerowych, by wychwycić ogólne wzorce chemiczne. Następnie dopracowano go na nieoznaczonej bibliotece 100 000 członków, a na końcu dostrojono na niewielkim zestawie 220 polimerów, które zostały zsyntezowane i przetestowane pod kątem zarówno siły przeciwbakteryjnej, jak i uszkodzeń czerwonych krwinek. Takie etapowe uczenie znacząco poprawiło zdolność modelu do przewidywania, które nowe polimery będą jednocześnie silne i bezpieczne.
Pozwalanie eksperymentom i algorytmom uczyć się nawzajem
PolyCLOVER nie zatrzymuje się na jednym cyklu przewidywań. Działa w pętli, w której SI proponuje najbardziej obiecujące i najbardziej informacyjne kandydujące struktury, chemicy je syntezują i testują w formacie wysokoprzepustowym, a nowe wyniki są zwracane, by udoskonalić model. Krok selekcji wykorzystuje podejście „górnej granicy ufności”, które równoważy eksploatację (preferowanie polimerów przewidywanych jako skuteczne) z eksploracją (badaniem niepewnych obszarów, gdzie model może najwięcej się nauczyć). W ciągu około czterech iteracyjnych rund sugerowane polimery stopniowo się poprawiały: stawały się bardziej aktywne wobec metycylinoopornego Staphylococcus aureus (MRSA) przy jednoczesnym utrzymaniu akceptowalnej toksyczności wobec czerwonych krwinek. W zaledwie 20 dni eksperymentów system skupił się na niewielkim zestawie wyróżniających się kandydatów.
Maleńkie samoorganizujące się cząstki, które przebijają bakterie
Trzy końcowe polimery wiodące, oznaczone H1, H2 i H3, samoistnie tworzyły dodatnio naładowane nanocząstki o średnicy około 100 nanometrów. W testach laboratoryjnych zabijały MRSA równie skutecznie jak standardowy antybiotyk streptomycyna, a robiły to znacznie szybciej — zmniejszając liczebność bakterii o kilka rzędów wielkości w ciągu minut do godzin, nawet w surowicy bogatej w białko. Mikroskopia elektronowa i sondy fluorescencyjne wykazały, że cząstki te szybko przyczepiają się do powierzchni bakterii i naruszają integralność błony oraz potencjał elektryczny, powodując wydostawanie się zawartości komórkowej. Co istotne, gdy MRSA eksponowano na te polimery przez prawie miesiąc, bakterie rozwinęły bardzo niewielką oporność, w kontraście do streptomycyny, dla której wymagana dawka dramatycznie wzrastała w tym samym okresie.
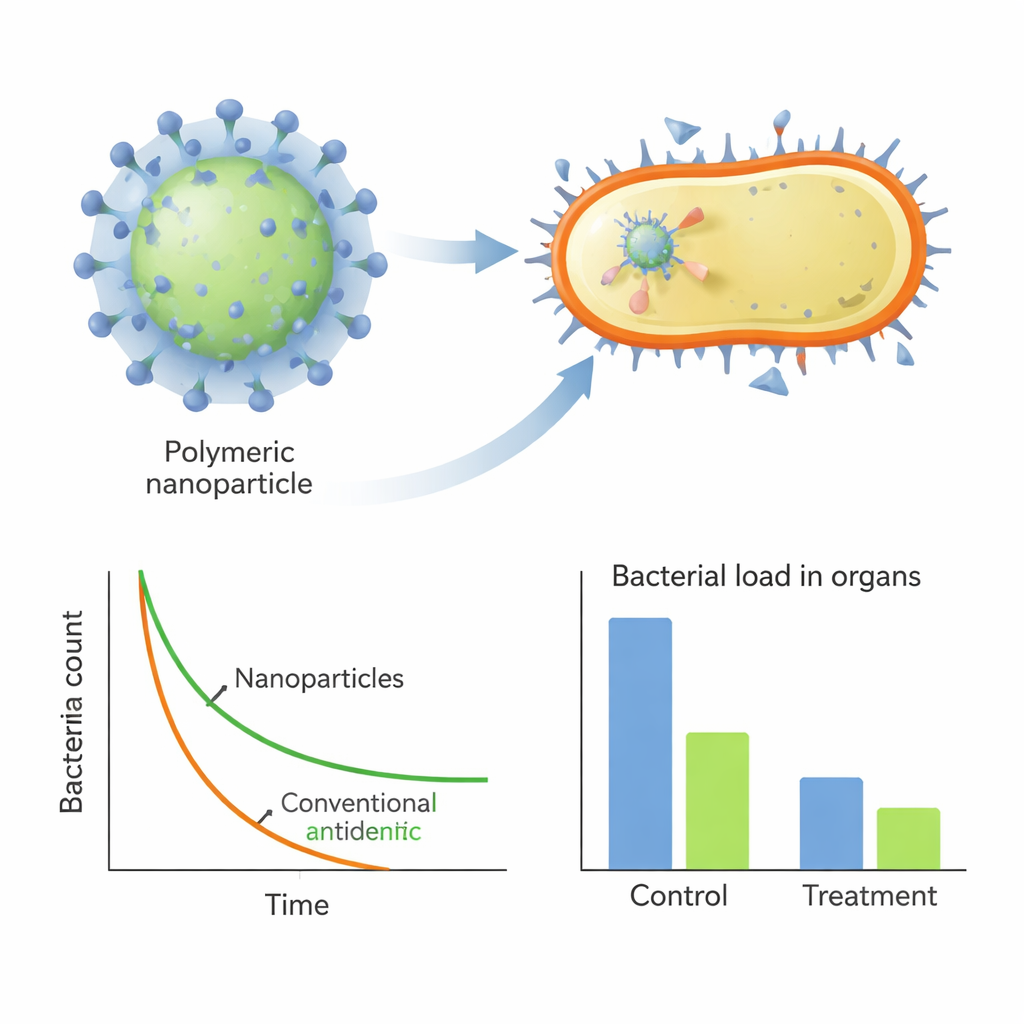
Przywracanie działania starych antybiotyków w infekcjach zwierzęcych
Oprócz działania samodzielnego, nanocząstki działały też jako potężne wsparcie dla tradycyjnych leków. W połączeniu z penicyliną G, na którą MRSA jest zwykle wysoko oporny, najlepszy polimer (H2) tworzył nanokompozyty, które uwięziły antybiotyk wewnątrz cząstki. Te kompozyty wykazywały silną synergię w testach in vitro, drastycznie obniżając dawkę penicyliny potrzebną do zahamowania MRSA. W modelach mysiaków z zapaleniem płuc i ciężką infekcją jamy brzusznej leczenie wiodącymi polimerami — zarówno samodzielnie, jak i w połączeniu z penicyliną — znacząco zmniejszało obciążenie bakteryjne w narządach, obniżało sygnały zapalne we krwi i ograniczało uszkodzenia tkanek, wszystko to bez oczywistej toksyczności.
Nowa instrukcja gry dla mądrzejszego odkrywania antybiotyków
Dla niespecjalistów najważniejszym wnioskiem jest to, że PolyCLOVER pokazuje, jak SI i zautomatyzowane eksperymenty mogą wspólnie odkrywać zupełnie nowe typy antybiotyków znacznie szybciej niż do tej pory. Zamiast polegać wyłącznie na przypadku i wolnym przesiewie, to podejście uczy się z każdej serii wyników, by trafniej dobierać polimery, które zarówno atakują bakterie odporne na leki, jak i skuteczniej dostarczają do nich konwencjonalne antybiotyki. Choć przed wprowadzeniem tych materiałów do kliniki potrzeba dalszych badań, badanie daje obiecującą drogę do uzupełnienia kurczącego się arsenału przeciwko infekcjom opornym i sugeruje ogólną strategię projektowania wielu innych inteligentnych biomateriałów.
Cytowanie: Wu, Y., Wang, C., Shen, X. et al. Iterative discovery of potent polymeric antibiotics via multi-stage and multi-task learning against antimicrobial resistance. Nat Commun 17, 1878 (2026). https://doi.org/10.1038/s41467-026-68682-z
Słowa kluczowe: oporność na antybiotyki, polimerowe antybiotyki, nanocząstki, uczenie maszynowe, oporne na leki bakterie