Clear Sky Science · pl
Różne zakłócenia błonowe przez antybiotyki lipopeptydowe: kolistyna i turnerkylamycyny
Dlaczego to ma znaczenie dla przyszłych antybiotyków
Infekcje oporne na leki mają zabijać dziesiątki milionów ludzi rocznie w połowie wieku, a jednymi z najbardziej śmiercionośnych sprawców są bakterie Gram-ujemne, które już ignorują wiele antybiotyków. Kolistyna jest jednym z nielicznych dostępnych leków, które wciąż mogą leczyć te zakażenia, ale jest toksyczna dla pacjentów, a bakterie coraz częściej uczą się jej unikać. To badanie rozkłada na czynniki pierwsze sposób działania kolistyny w porównaniu z nową rodziną naturalnych antybiotyków zwanych turnerkylamycynami, ujawniając, że drobne zmiany chemiczne mogą dawać bardzo różne mechanizmy zabijania bakterii — i potencjalnie bezpieczniejsze leki.
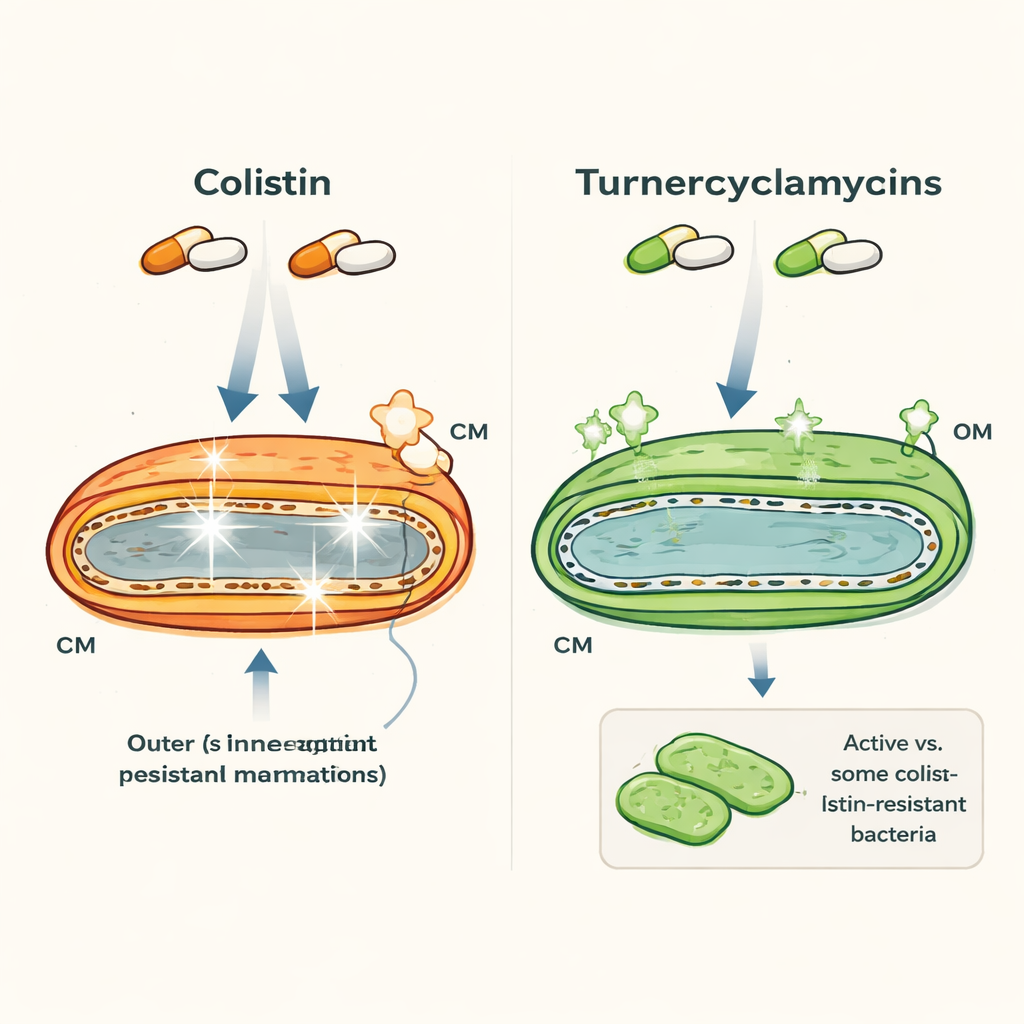
Dwa podobnie wyglądające leki o bardzo odmiennym zachowaniu
Kolistyna i turnerkylamycyny to oba lipopeptydy — cząsteczki łączące tłusty ogon z peptydowym pierścieniem — i oba celują w bakterie Gram-ujemne, takie jak Escherichia coli i Acinetobacter. Na pierwszy rzut oka wyglądają podobnie, lecz ich właściwości znacznie się różnią. Kolistyna to lek ostatniej szansy, działający szybko, lecz mogący uszkadzać nerki i układ nerwowy człowieka, a bakterie coraz częściej niosą geny oporności, takie jak mcr-1. Turnerkylamycyny, odkryte w bakteriach związanych z drewnojadami, są w stanie zabić wiele tych samych patogenów, w tym niektóre szczepy oporne na kolistynę, ale wykazują znacznie mniejszą toksyczność w testach laboratoryjnych. Co intrygujące, dwie wersje różniące się jedynie niewielkim wydłużeniem ogona tłuszczowego już wykazują różne wzorce oporności, co sugeruje, że bardzo subtelne cechy strukturalne mają znaczenie.
Jak kolistyna przebija dziury, a turnerkylamycyny działają powoli
Autorzy użyli barwników fluorescencyjnych, eksperymentów „time-kill” i mikroskopii elektronowej, aby obserwować, jak te leki wpływają na błony bakteryjne w czasie. Kolistyna szybko powoduje przepuszczalność zarówno błony zewnętrznej, jak i wewnętrznej (cytoplazmatycznej), prowadząc do gwałtownej śmierci komórek w ciągu kilku godzin. Natomiast turnerkylamycyny zabijają wolniej — zajmuje im to 6–10 godzin, aby całkowicie oczyścić hodowle — i głównie zakłócają błonę zewnętrzną. Barwniki, które świecą, gdy naruszona zostaje błona wewnętrzna, dawały silne sygnały dla kolistyny, lecz jedynie umiarkowane, opóźnione sygnały dla turnerkylamycyn, a obrazy o wysokiej rozdzielczości potwierdziły niewielkie widoczne uszkodzenia błony wewnętrznej nawet wtedy, gdy komórki umierały. Wskazuje to, że turnerkylamycyny nie zabijają klasyczną drogą tworzenia porów używaną przez wiele antybiotyków celujących w błony.
Bloki budulcowe lipidów jako ukryte regulatory
Obie rodziny leków ostatecznie zależą od bakteryjnego składnika zwanego lipopolisacharydem (LPS), który jest syntetyzowany w błonie wewnętrznej i zwykle eksportowany na zewnętrzną powierzchnię. Gdy badacze wyłączyli wczesne etapy biosyntezy LPS, zarówno kolistyna, jak i turnerkylamycyny traciły aktywność; ale gdy zablokowali mechanizm transportu przesuwający LPS na zewnątrz, leki nadal działały. Oznacza to, że istnienie prekursorów LPS jest niezbędne, ale ich ostateczne położenie nie. Kluczowa różnica pojawiła się przy bezpośrednim pomiarze wiązania: kolistyna silnie przylega do oczyszczonego LPS z powinowactwem w zakresie mikromolarów, podczas gdy turnerkylamycyny nie wykazały mierzalnego wiązania. Zamiast tego turnerkylamycyny były silnie modulowane przez inne lipidy błonowe. Niektóre fosfolipidy, zwłaszcza fosfatydyloglicerol, mogły osłabiać lub modulować ich aktywność, a leki były łatwo pochwycone przez pęcherzyki błony zewnętrznej — drobne lipidowe bańki zrzucane przez bakterie.
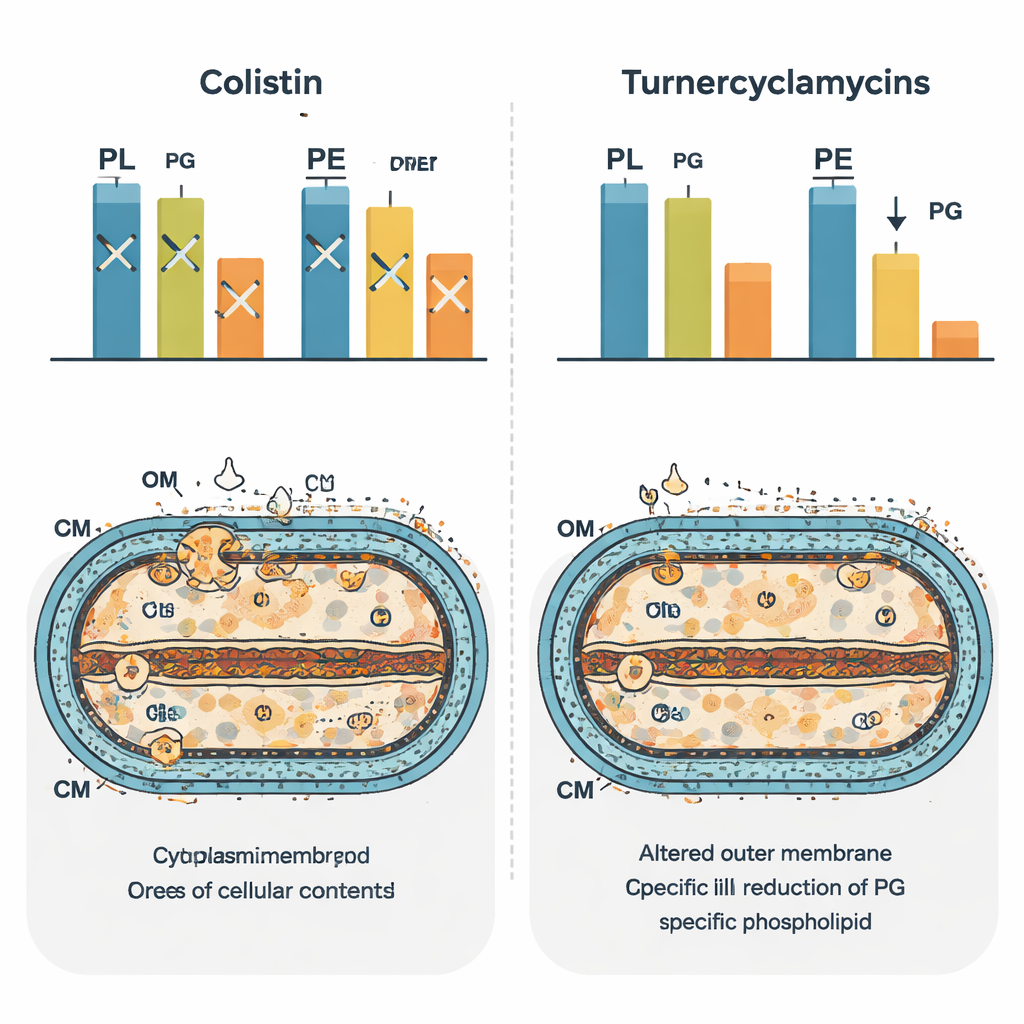
Przeprogramowywanie krajobrazu lipidowego bakterii
Aby zobaczyć szerszy wpływ na komórkę, zespół użył analiz masowej („fosfolipidomiki”), aby skatalogować setki gatunków lipidów po leczeniu. Kolistyna wywołała charakterystyczny wzór zmian odzwierciedlający jej szerokie zakłócenie homeostazy błon. Turnerkylamycyny wygenerowały inny sygnaturowy wzorzec, który przypominał bakterie pozbawione białka transportującego lipidy o nazwie MlaA. W tych komórkach pewne lipidy diacyloglicerynowe były zubożone, a formy monoacyloglicerynowe wzrosły, co sugeruje, że normalne cykling i przebudowa fosfolipidów między błonami zostały zaburzone. Co istotne, poziomy fosfatydyloglicerolu spadły w komórkach traktowanych turnerkylamycynami, co wzmacnia pogląd, że ten lipid jest bezpośrednio związany z ich skutecznością. Autorzy proponują, że turnerkylamycyny mogą działać jako molekularne strukturalne „imitatory”, które blokują szlaki łączące syntezę lub transport kwasów tłuszczowych, LPS i fosfatydyloglicerolu.
Co to znaczy dla projektowania lepszych leków
Mówiąc prosto, badanie pokazuje, że kolistyna zabija przez szybkie rozdarcie obu ochronnych warstw bakterii Gram-ujemnej, wspierane przez silne wiązanie z LPS, podczas gdy turnerkylamycyny działają raczej jak sabotażyści łańcucha dostaw lipidów komórkowych. Wnikają w błonę zewnętrzną, stopniowo zaburzają sposób wytwarzania i recyklingu określonych lipidów i ostatecznie powodują awarię osłony komórkowej — bez intensywnego niszczenia błony wewnętrznej. Ponieważ ten łagodniejszy, bardziej ukierunkowany mechanizm wiąże się z mniejszą toksycznością i odmiennym profilem oporności, jego zrozumienie daje mapę drogową do projektowania kolejnej generacji antybiotyków lipopeptydowych. Poprzez dopracowanie cech takich jak długość i stopień nasycenia ogona tłuszczowego, chemicy mogą zbudować leki, które oszczędzają tkanki ludzkie, utrzymują aktywność wobec szczepów opornych na kolistynę i pozostają krok przed bakteriami opornymi na antybiotyki.
Cytowanie: Lim, A.L., Miller, B.W., Fisher, M.A. et al. Differential membrane lipid disruption by lipopeptide antibiotics, colistin and turnercyclamycins. Nat Commun 17, 1880 (2026). https://doi.org/10.1038/s41467-026-68681-0
Słowa kluczowe: oporność na antybiotyki, bakterie Gram-ujemne, kolistyna, antybiotyki lipopeptydowe, lipidy błonowe